Generellitet
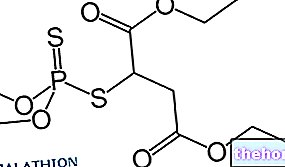
Hydrogensulfid - ellers kjent som hydrogensulfid eller dihydrogensulfid (H2S) - er et molekyl som er løselig i vann og etanol, som avgir en veldig sterk "råtten egg" lukt.

Dihydrogensulfid (H2S) er giftig og til og med dødelig for mennesker; utslipp til luft skjer hovedsakelig som følge av:
- Bakteriell eller enzymatisk spaltning av svovelholdige proteiner i stabiliserende bindinger, for eksempel disulfidbroer og i svovelaminosyrer
- Tilberedning av proteiner og denaturering av sekundære, tertiære og kvartære strukturer med disulfidbroer som brytes.
Hydrogensulfid (H2S) er sterkt tilstede i utpustene som kommer fra: luftlommer i undergrunnen, råolje og områder med høy putrescentaktivitet (som dammer, myrer og sumper); hydrogensulfid er en av de aromatiske komponentene som er mest tilstede i avføring og tarmgass men frigjøringen i store mengder skjer hovedsakelig i produksjonssyklusene i næringsmiddelindustrien, i rensing av vann med slam, i oljeraffinering, etc.
NB. Dihydrogensulfid (H2S) reagerer med sølv og danner overfladisk en svart patina av sølvsulfid, synlig på ringer, øredobber og halskjeder etter termiske bad.
Giftighet
Hydrogensulfid (H2S) er en gift som virker ved å hemme mitokondriell respirasjon, derfor påvirker dets toksiske virkning alle celler i kroppen som utnytter aerob metabolisme (praktisk talt alle, unntatt røde blodlegemer); den farligste egenskapen til hydrogensvovel (H2S) ved middels høye konsentrasjoner det er dens evne til å deaktivere den luktfulle sanseoppfatningen, som den eneste alarmklokken for tilstedeværelse av dihydrogensulfid (H2S) i luften. Ved lave konsentrasjoner derimot, gir hydrogensulfid (H2S) irritasjon i slimhinnene, hyperventilasjon og lungeødem, og langvarig eksponering fører til kronisk tretthet, tap av matlyst, hodepine, kognitiv og hukommelsessvikt.
Hydrogensulfid (H2S) er allerede merkbart i konsentrasjoner på 0,0047 deler per million (av 50% av menneskene), mens 10ppm representerer den nedre grensen for toksisitet uten risiko for helseskade etter eksponering for 8 påfølgende timer; med nivåer lik 1000ppm dihydrogensulfid (H2S) er det en umiddelbar kollaps selv etter et enkelt pust.
Konsentrasjoner i deler per million (ppm)
Effekt på den menneskelige organismen
0,0047 sider / min
Nedre grense for oppfatning for 50% av mennesker
<10 sider / min
Eksponeringsgrense uten helseskade i 8 timer om dagen
10-20 sider / min
Grense utover hvilken øynene er irritert av gassen
50-100 sider / min
Konsentrasjon som forårsaker celleskade
100-150 sider / min
Konsentrasjon som lammer luktnerven
320-530 sider / min
Konsentrasjon forårsaker lungeødem
530-1000 sider / min
Konsentrasjon som forårsaker hyperventilasjon
800 sider / min
Nedre grense for dødelighet for 50% av mennesker etter 5 "eksponering
> 1000 sider / min
Minimumskonsentrasjon forårsaker kvelningskollaps etter 1 pust
Hydrogensulfid i mat
Hydrogensulfid (H2S) kan produseres i matvarer som det frigjøres ved gassformig fordampning; hydrogensulfid (H2S) er et typisk derivat av noen kjemiske transformasjoner, for eksempel brudd på disulfidbroer og aggregering av hydrogenioner ( H +) etter "tilberedning av proteiner" (denaturering). Denne reaksjonen er godt merkbar i det hardkokte egget som produserer dihydrogensulfid (H2S) med utgangspunkt i svovel av albumen (som, selv om det er flyktig, beholdes av skall), i det øyeblikket den beskjæres frigjør den gassen umiddelbart og gjør den merkbar for nesen. Vi husker også at i kokt egg er hydrogensulfid (H2S) som frigjøres ved tilberedning av eggehviten ansvarlig for jernholdig (overfladisk) kelering av eggeplommen med produksjon av et salt kalt jernholdig sulfid (FeS), pluss to hydrogenioner; Den kjemiske reaksjonen er som følger:
H2S + Fe ++ → FeS + H2
NB. Ferrosulfid er en forbindelse som, mens kelatering av jernet i eggeplommen og delvis forhindrer metabolsk bruk, er ufarlig ved lave konsentrasjoner, men det skal ikke undervurderes ved høye doser.
Hydrogensulfid (H2S) er også en forbindelse som letter skillet mellom: mat av sunn animalsk opprinnelse sammenlignet med de som er i nedbrytningsprosessen; dette skjer i kraft av den nedbrytende bakterielle virkningen både mot sulfidbroene til proteinene og til svovel aminosyrer, med påfølgende frigjøring av svovel bestemt for syntese av dihydrogensulfid (H2S). NB. Denne prosessen er gjenkjennelig spesielt i nedbrytning av egg og fisk som er skadet av dårlig bevaring.