Denne artikkelen tar for seg alle mulige toksiske effekter forårsaket av farlige stoffer under reproduksjonssyklusen. Viktig å nevne er forskjellen mellom to vitenskapelige termer, som er teratologi og teratogenese.
Det spesialiserte området som studerer etiologien til den unormale utviklingen av embryoet er TERATOLOGI. TERATOGENESIS er derimot prosessen som er ansvarlig for medfødte effekter under utviklingen av embryoet og fosteret.
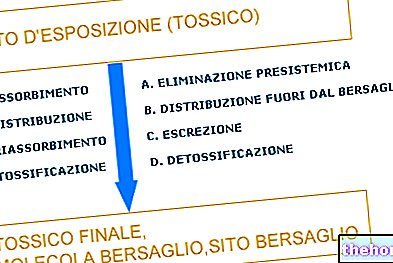
Effektene som et teratogen kan forårsake på unnfangelsesproduktet - uten at det skader moren - er hovedsakelig to:
- EMBRYO -EFFEKTER: Dette er konsekvenser som innebærer spontan abort, resorpsjon av eggcellen eller fødsel av døde fostre.I dette tilfellet overlever fosteret ikke.
- EMBRIOTOKSISKE EFFEKTER: Dette er konsekvenser som tillater utvikling av fosteret, men med strukturelle og / eller funksjonelle misdannelser. I dette tilfellet utvikler fosteret seg annerledes enn det forrige tilfellet.
Alle giftige stoffer, som kan komme i kontakt med moren, kan følgelig også gå over til fosteret. Det skal faktisk huskes at morkaken IKKE er en virkelig perfekt barriere, som er i stand til å fullstendig beskytte fosteret mot eksponering for giftige og potensielt teratogene stoffer.
Teratologi har flere studiemål, som er: mottakeligheten av teratogenet, de teratogene midlene med deres virkningsmekanismer, teratogenets egenskaper, teratogenets mål og til slutt teratogenets artsspesifikke effekt, derfor som farlig stoff virker på en bestemt art (talidomid forårsaket ikke farlige effekter på rotte, men på mennesker forårsaket det phocomelia hos det nyfødte).
Under fostrets vekst må tre grunnleggende kritiske perioder tas i betraktning, der - hvis moren kom i kontakt med teratogene stoffer - kunne fosteret lide alvorlig skade. De kritiske stadiene er: pre-differensieringsstadiet (pre-implantasjon og implantasjon av blastocysten i livmoren), organogenese (morfologiske endringer) og til slutt fosterstadiet (funksjonelle og morfologiske endringer og veksthemming).
Teratogene stoffer har forskjellige virkningsmekanismer på fosteret.De kan forhindre en regelmessig vekst av fosteret og / eller forårsake misdannelser av det. Nå skal vi beskrive mulige virkningsmekanismer.
- Det teratogene stoffet kan fremheve den apoptotiske virkningen på visse celletyper.I embryonfasen er det cellulære populasjoner som bare er nyttige for riktig utvikling av et organ, hvoretter - ikke lenger nødvendig - går mot cellulær apoptose Det kan skje at teratogenet forbedrer den apoptotiske virkningen av disse cellene, for å produsere overdreven celledød og mangel på utvikling av det aktuelle organet.
- PRODUKSJON AV OXYGEN FREE RADICALS og OXIDATIVE STRESS.
- Det er stoffer som kan forårsake endring av cellebevegelser. Det er celler som en gang er utviklet må bevege seg for å nå sin endelige plassering, for eksempel cellene i nevrale toppene. Disse cellene er en del av nevralrøret. Disse cellene løsner fra det nevrale rør og vandrer inn i organismen i formasjon, hvor de vil danne ryggraden ganglia, kraniale nerver og mesenkymale celler (som vil bli bein i skallen og ansiktet). Hvis disse nevrale kamcellene ikke migrerer riktig til sine endelige steder, vil de produsere misdannelser i utviklingen av skallen og ansiktsskjelettet. I tillegg er de også ansvarlige for en korrekt deling av hjertet, med produksjon av hjertesepta. Retinsyre og dets derivater i høye doser har effekten av misdannelse av skjelettet i hodeskallen, i ansiktet og en feil hjertedeling, fordi de forhindrer en korrekt migrering av disse cellene i den embryoniske perioden.
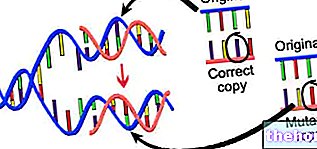
- Stoffer som valproinsyre, som er ansvarlig for spina bifida hos det ufødte barnet, gir en "FORANDRING I" UTTRYKKEN (tidsmessig og romlig) AV GENENE SOM KONTROLLERER EMBRYOUTVIKLINGEN.
- Stoffer som induserer en "HEMMELIG HANDLING AV ENZYMER.
- Stoffer som forårsaker ENDRINGER AV SIGNALT TRANSDUKSJONSSTIER. Hvis dette signalet blir modifisert og overført til cellen på en feil måte, vil sistnevnte utvikle seg på en unormal måte.
- Stoffer som forårsaker ENERGISupportmangel, derfor stoffer som virker på oksidativ fosforylering og cellulær respirasjon med påfølgende unormal utvikling av cellen på grunn av mangel på grunnleggende elementer for vekst (ATP).
Dosene som testes i de forskjellige testene for teratogenese er hovedsakelig maksimal tolerert dose (MTD), NOEL og mellomdosen mellom MTD og NOEL. Tester for akutt toksisitet og subakutt toksisitet må allerede ha blitt utført før disse testene ble utført. For å studere effekten på reproduksjon, utføres de forskjellige testene hovedsakelig i tre faser. Den første fasen evaluerer graden av fruktbarhet og reproduksjonsevne til dyret, den andre fasen gjelder fosterets utvikling og til slutt evaluerer den tredje fasen toksisiteten . før fødsel og etter fødsel.
FØRSTE FASE: STUDIE AV Fruktbarhet og reproduktiv kapasitet
Studietiden varer i 60 dager, og stoffet som skal testes administreres til både hunn- og hanndyr.
Hannyret behandles med teststoffet i minst to måneder, hvoretter det parres med hunnen. I disse 60 dagene forekommer modningen fra spermatogonium til sæd. Deretter vurderes det om teststoffet kan ha noen effekt på spermatozoa. Hos hunndyret utføres behandlingen med stoffet i 14 dager, noe som tilsvarer modningstiden til eggcellen. Mulige effekter indusert av teststoffet på modning av eggcellen vil bli bestemt.
Etter disse testene fortsetter vi parringen. På hunndyret fortsetter vi behandlingen med stoffet for hele graviditetsperioden og amming.
Poengene som tas i betraktning er:
- Koblingsindeks;
- Fruktbarhetsindeks;
- Svangerskapsindeks;
- Tap før implantasjon;
- Tap etter implantasjon;
- Svangerskapsvarighet;
- Vitalitetsindeks;
- Ammingsindeks.
ANDRE FASE: STUDIEUTVIKLING AV Fosteret
Den andre fasen går for å studere de teratogene effektene. I denne fasen er det kun gravide hunner som blir utsatt for teratogenesetester, behandlet med giftstoffet i organogeneseperioden. Organogenese hos rotter eller mus skjer fra den sjette til den femtende dagen av svangerskapet.
Poengene som tas i betraktning er:
- Antall ufødte barn;
- Tilstedeværelse av misdannelser (levendefødte);
- Tilstedeværelse av viscerale og skjelettmisdannelser (dødfødsler);
- Mors livmor.
Tredje fase studie av pre-postnatal giftighet
Gravide hunnmus eller rotter behandles fra den femtende svangerskapsdagen til dagen etter fødselen. Antall levendefødte, graviditetens varighet og fødsel, fødselsvekten, vurderingen av den fysiske modenheten til de levende fødselene og vurderingen av atferd.
Miljøgifter, kjemikalier og legemidler kan også finnes i generasjoner etter den som ble behandlet eller kom i kontakt med det teratogene stoffet. For å bestemme mulig overføring av teratogene effekter i flere generasjoner, kan flere generasjonelle studietester utføres, slik at de mulige effektene som blir funnet, for eksempel ytre, viscerale og skjelettmisdannelser, studeres i flere generasjoner. Morfologiske studier på påfølgende generasjoner inkluderer evalueringer av mulige strukturelle, viscerale og ytre misdannelser. Bestemmelsen av disse misdannelsene kan vurderes på både levende og døde dyr, akkurat som det ble sett i toksisitetstesting.
Er det mulig å tilpasse resultatene av de teratogene studiene på dyr og tilpasse de samme resultatene til mennesker? De oppnådde resultatene kan ikke overføres direkte til mennesker, men hvis et stoff i mange tilfeller er funnet å være teratogent for dyret er også teratogent for mennesker. Virkningene som stoffet gir på dyret, på godt eller vondt, gjengir dem også hos mannen. DYRPRØVNINGER MÅ ALDRI IKKE ALLTID TILBYDE VISNINGER OM SVARET SOM STOFFEN HAR PÅ MANN.
Alle disse effektene avhenger alltid av eksponeringstid og varighet, samt graden av individuell følsomhet.
Andre artikler om "Reproduktiv syklus toksikologi og teratogenese"
- Studie og evaluering av karsinogenese
- Giftighet og toksikologi
- Giftighet av plantevernmidler