
Frykten er at genmanipulering også kan brukes for å prøve å forbedre sportsprestasjoner; på denne måten har World Anti-Doping Agency (WADA) allerede tatt skritt, inkludert genetisk doping i listen over forbudte metoder og stoffer.
I teorien kan alle proteinnivåer i kroppen vår moduleres gjennom genterapi.
Konferansen om genetisk doping som ble holdt i mars 2002 av WADA [Pound R, WADA 2002], og "European Labour Congress on Harmonization and Future Developments of the Anti-Doping Policy" som fant sted i Arnhem, Holland, i samme år, ga forskere, leger, leger, myndigheter, antidopingorganisasjoner og farmasøytiske næringer muligheten til å utveksle informasjon om resultatene av forsknings- og deteksjonsmetoder angående denne nye dopingteknikken.
Siden 1. januar 2003 har Den internasjonale olympiske komité (IOC) inkludert genetisk doping på listen over forbudte stoffklasser og metoder [WADA, 2007]. Siden 2004 har WADA tatt ansvar for å publisere den internasjonale dopinglisten, som oppdateres årlig. Den genetiske dopingmetoden som er inkludert i denne listen er definert som ikke-terapeutisk bruk av celler, gener, genetiske elementer eller modulering av genuttrykk, med sikte på å forbedre atletisk ytelse.
Denne artikkelen tar sikte på:
- å avklare om det i sport faktisk er mulig å gjøre bruk av den økende kunnskapen fra genterapi, en ny og lovende gren av tradisjonell medisin;
- identifisere de mulige måtene som genterapi kan brukes for å øke ytelsen.
I denne "genetiske og genomiske tidsalderen, det vil være mulig å identifisere genene som bestemmer en persons genetiske disposisjon for en bestemt sport [Rankinen T et al., 2004]. Studien av gener i ung alder kan representere den beste måten å utvikle en flott idrettsutøver fra et barn og å lage et spesifikt personlig treningsprogram. Denne studien som brukes på idrettsutøvere kan også brukes til å identifisere spesifikke treningsmetoder med sikte på å øke den genetiske disposisjonen for den type trening [Rankinen T et al., 2004].
Men vil studere gener resultere i bedre idrettsutøvere?
Marion Jones og Tim Montgomery var begge 100 m hurtighetsmestere, de fikk en baby sommeren 2003. Steffi Graf og Andre Agassi (begge verdensmesterskapene i tennis) har også barn. Disse barna vil mest sannsynlig være favoritter. Sammenlignet med de andre, men Det er også andre faktorer, for eksempel miljømessige og psykologiske faktorer, som avgjør muligheten for at de blir mestere eller ikke.
Genterapi kan defineres som overføring av genmateriale til menneskelige celler for behandling eller forebygging av sykdom eller dysfunksjon. Dette materialet er representert av DNA, RNA eller av genetisk endrede celler. Genterapiprinsippet er basert på introduksjon i cellen til et terapeutisk gen for å kompensere for det manglende genet eller erstatte det unormale. Generelt brukes DNA, som koder for det terapeutiske proteinet og aktiveres når det når kjernen.
"De fleste idrettsutøvere tar medisiner" [De Francesco L, 2004].
En undersøkelse fra Drug Research Center konkluderte med at mindre enn 1% av den nederlandske befolkningen har tatt dopingprodukter minst én gang, til sammen om lag 100 000 mennesker. 40% av disse menneskene har brukt doping i årevis, og de fleste trener styrketrening eller kroppsbygging. Bruken av dopingstoffer i elitesport ser ut til å være høyere enn 1% angitt for befolkningen generelt, men det eksakte tallet er ikke kjent. Andelen eliteidrettsutøvere som tester positivt på dopingkontroll har svingt mellom 1%. 1,3% og 2.0% de siste årene [DoCoNed, 2002].
WADAs definisjon av genetisk doping gir rom for spørsmål
- Hva betyr egentlig ikke-terapeutisk?
- Vil de pasientene med muskeldysfunksjoner behandlet gjennom genterapi bli tatt opp i konkurransene?
Det samme hensynet gjelder kreftpasienter som har blitt behandlet med cellegift og som nå mottar EPO -genet som koder for erytropoietin for å fremskynde utvinningen av beinmargsfunksjonen.
Nåværende forskning på genterapi utføres også for å fremskynde helingsprosessen av et sår, eller for å lindre muskelsmerter etter trening; slik praksis kan ikke anses av alle som "terapeutiske", og deres ytelsesfremmende egenskaper kan stilles spørsmålstegn ved.
Fra et klinisk synspunkt ville det være mer hensiktsmessig å spesifisere definisjonen av genetisk doping bedre, spesielt i lys av feil bruk av genoverføringsteknologier.
WADA (seksjon M3 i Verdens antidopingkodeks (versjon 1. januar 2007) begrunnet forbudet mot genetisk doping gjennom følgende punkter:
- vitenskapelig bevis, påvist farmakologisk effekt eller erfaring, på at stoffene eller metodene som er inkludert på listen har evnen til å øke sportsprestasjoner;
- bruk av stoffet eller metoden forårsaker en reell eller antatt risiko for utøverens helse.
- bruk av doping krenker idrettens ånd. Denne ånden er beskrevet i innføringen av kodeksen med henvisning til en rekke verdier som etikk, fair play, ærlighet, helse, moro, lykke og overholdelse av reglene.
Det er mange usikkerheter om de langsiktige effektene av genmodifisering; Mange av disse effektene kan heller aldri bli oppdaget, enten fordi de ikke er grundig studert (på grunn av økonomiske problemer), eller fordi det er vanskelig å definere pålitelige prøver for å studere bivirkninger av helt nye metoder eller applikasjoner.
I motsetning til somatiske celleterapier er endringene av kimlinjene permanente og overføres også til avkomene. I dette tilfellet, i tillegg til mulig risiko for idrettsutøvere, er det også risiko overfor tredjeparter, for eksempel ettertiden, foreldre eller partnere.
Innen farmakogenetikk, hvis utvikling er avhengig av vitenskapens og legemiddelindustriens samlede innsats, er hovedmålet å utvikle medisin som er "skreddersydd" for hver av oss. Som det er kjent, har mange medisiner en helt annen avhengig på hvem som tar dem, skyldes dette at deres utvikling er generisk og ikke tar hensyn til individuelle genetiske egenskaper. Hvis farmakogenetikk skulle spre seg i sportens verden, kunne selve ideen om konkurranse mellom tilsynelatende like idrettsutøvere som forbereder seg på en mer eller mindre sammenlignbar måte bli foreldet.
De eksperimentelle kliniske dataene for genterapi har vist svært oppmuntrende resultater hos pasienter med alvorlig kombinert immunsvikt [Hacein-Bey-Abina S et al., 2002] og hemofili B [Kay MA, et al. 2000]. Videre har angiogen terapi gjennom vektorer som uttrykker vaskulær endotelial vekstfaktor for behandling av koronar hjertesykdom gitt gode resultater ved angina [Losordo DW et al., 2002].
Hvis overføring av gener som koder for vevsvekstfaktorer ble brukt [Huard J, Li Y, Peng HR, Fu FH, 2003], kan behandling av de ulike skadene forbundet med sportstrening, for eksempel brudd på leddbånd eller muskelrev, føre til teoretisk i bedre regenerering. Disse tilnærmingene evalueres nå på dyremodeller, men kliniske forsøk på mennesker vil sikkert også bli aktivert i de kommende årene.
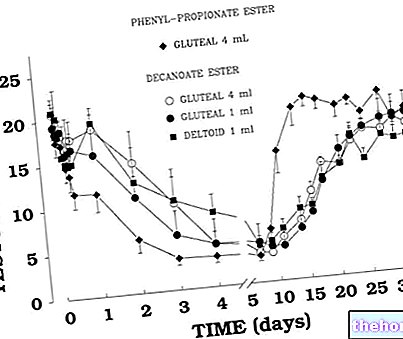
I 1964 gjorde den nordfinske skiløperen Eero Mäntyranta motstandernes innsats ubrukelig ved å vinne to OL -gull på lekene i Innsbruck, Østerrike. Etter noen år ble det vist at Mantyranta bar en sjelden mutasjon i genet for erytropoietinreseptoren som, ved å kompromittere den normale tilbakemeldingskontrollen på antall røde blodlegemer, forårsaker polycytemi med en påfølgende økning på 25-50% i oksygen transport kapasitet. Å øke mengden oksygen til vevet betyr økt motstand mot tretthet. Mäntyranta hadde det enhver idrettsutøver ønsker: EPO. Fremtidens idrettsutøvere kan kanskje introdusere et gen i kroppen som etterligner effekten av genmutasjonen som naturlig forekom i Mäntyranta og bidrar til ytelse.
Insulinlignende vekstfaktor (IGF-1) produseres av både lever og muskel, og konsentrasjonen avhenger av konsentrasjonen av humant veksthormon (hGH).
Trening, foreslår Sweeney, stimulerer muskelforløperceller, kalt "satellitter", til å være mer "mottakelige for IGF-I.
[Lee S. Barton ER, Sweeney HL, Farrar RP, 2004]. Å bruke denne behandlingen på idrettsutøvere vil bety å styrke tennisspillerens brakialmuskler, løperens kalv eller bokserens biceps. Slik terapi antas å være relativt tryggere enn EPO, siden effekten bare er lokalisert til målmusklen. Det er sannsynlig at denne tilnærmingen også vil bli brukt på folk allerede i de neste årene.
En isoform av insulinlignende vekstfaktor-1 (IGF-1), den mekaniske vekstfaktoren (MGF), aktiveres av mekaniske stimuli, som f.eks. muskeltrening. Dette proteinet, i tillegg til å stimulere muskelvekst, spiller en viktig rolle i reparasjonen av skadet muskelvev (som for eksempel skjer etter intensiv trening eller konkurranse).
MGF produseres i muskelvev og sirkulerer ikke i blodet.
VEGF representerer vekstfaktoren for det vaskulære endotelet og kan brukes for å lette veksten av nye blodkar VEGF -terapi ble utviklet for å produsere koronar bypass -podning hos pasienter med iskemisk hjertesykdom, eller for å hjelpe eldre mennesker med perifer arteriell sykdom. Gener at koden for VEGF kan fremme veksten av nye blodårer ved å tillate større tilførsel av oksygen til vevet.
Så langt har genterapi-eksperimenter blitt utført for sykdommer som hjerte-iskemi [Barton-Davis ER et al., 1998; Losordo DW et al., 2002; Tio RA et al., 2005] eller perifer arteriell insuffisiens [Baumgartner I et al., 1998; Rajagopalan S et al., 2003].
Hvis disse behandlingene også ble brukt på idrettsutøvere, ville resultatet være en økning i oksygen- og næringsinnholdet i vevet, men fremfor alt muligheten til å utsette utmattelsen av både hjerte- og skjelettmuskulatur.
Siden VEGF allerede brukes i mange kliniske studier, ville genetisk doping allerede være mulig.
Det normale differensiering av muskel -skjelettmassen det er av grunnleggende betydning for den korrekte funksjonaliteten til organismen; denne funksjonen er mulig takket være virkningen av myostatin, et protein som er ansvarlig for vekst og differensiering av skjelettmuskler.
Det fungerer som en negativ regulator, som hemmer spredning av satellittceller i muskelfibre.
Eksperimentelt brukes myostatin in vivo å hemme muskelutvikling i forskjellige pattedyrsmodeller.
Myostatin er aktiv både med en autokrin og parakrin mekanisme, både på muskuloskeletale og hjerte -nivå. Dens fysiologiske rolle er ennå ikke fullt ut forstått, selv om bruk av myostatinhemmere, som follistatin, forårsaker en dramatisk og utbredt økning i muskelmasse [Lee SJ, McPherron AC, 2001]. Slike hemmere kan forbedre den regenerative tilstanden hos pasienter som lider av alvorlige sykdommer som Duchenne muskeldystrofi [Bogdanovich S et al., 2002)].
Myostatin tilhører TGF beta-superfamilien og ble først avslørt av gruppen Se-Jin Lee [McPherron et al., 1997]. I 2005 påpekte Se-Jin Lee fra Johns Hopkins University at mus som er fratatt myostatin-genet (knock out mus) utvikler hypertrofisk muskulatur.
Disse supermusene var i stand til å gå trapper med tunge vekter festet til halen. I løpet av samme år viste tre andre forskningsgrupper at storfe-fenotypen som vanligvis kalles "dobbel-muskel" skyldtes en mutasjon i genet som koder for myostatin [Grobet et al., 1997; Kambadur et al., 1997; McPherron & Lee, 1997].
En mutasjon av den homozygote typen mstn - / - ble nylig oppdaget hos et tysk barn som har utviklet ekstraordinær muskelmasse. Mutasjonen har blitt referert til som effekten av å hemme myostatinuttrykk hos mennesker. Barnet utviklet muskler godt ved fødselen, men i oppveksten økte også muskelmassen, og i en alder av 4 klarte han allerede å løfte vekter på 3 kilo; han er sønn av en tidligere profesjonell idrettsutøver og besteforeldrene hans ble kjent som veldig sterke menn.
Genetiske analyser av mor og barn avslørte en mutasjon i myostatin -genet som resulterte i mangel på produksjon av proteinet [Shuelke M et al., 2004].
Både når det gjelder eksperimentene som ble utført på musen av Se-Jin Lee-gruppen og hos barnet, hadde muskelen vokst både i tverrsnittet (hypertrofi) og i antall myofibriller (hyperplasi) [McPherron et al. ., 1997].
Smerte er en ubehagelig sensorisk og emosjonell opplevelse forbundet med faktisk eller potensiell vevsskade og beskrevet i form av slik skade [iasp]. På grunn av dens ubehagelighet kan følelsen av smerte ikke ignoreres og induserer subjektet som prøver det for å unngå (skadelige) stimuli som er ansvarlig for det; dette aspektet konfigurerer smertens beskyttende funksjon.
I sport kan bruk av kraftige smertelindrende medisiner føre idrettsutøvere til å trene og konkurrere utover normal smerteterskel.
Dette kan forårsake betydelig helserisiko for utøveren, siden skaden kan forverres betraktelig og bli til en varig skade. Bruk av disse stoffene kan også føre utøveren til psyko-fysisk avhengighet av dem.
Et "alternativ til juridiske smertestillende midler kan være å bruke smertestillende peptider som endorfiner eller enkefaliner. Preklinisk dyreforsøk har vist at genene som koder for disse peptidene har en effekt på oppfatningen av inflammatoriske smerter [Lin CR et al., 2002; Smith O , 1999].
Genterapi for smertelindring er imidlertid fortsatt langt fra den kliniske anvendelsen.
, kjemikalier, virus, etc.) og det kodede transgenet.Klinisk forskning til nå har vært relativt trygg [Kimmelman J, 2005]. Mer enn 3000 pasienter er blitt behandlet, og bare en av disse døde av kronisk leversykdom og vektoroverdosering [Raper SE et al., 2003]. Hos tre andre pasienter behandlet for immunsviktssyndrom utviklet leukemi-lignende symptomer [Hacein-Bey-Abina S et al., 2002] og en av dem døde. Siden den gang har andre forskergrupper behandlet lignende pasienter med lignende terapeutiske resultater, uten noen bivirkninger [Cavazzana-Calvo M. Fischer A, 2004]. I dette tilfellet er forskning rettet mot å behandle pasienter med vektorer som aldri kan brukes til å øke ytelsen.
Personer som prøver å øke EPO -nivåene unaturlig øker også sannsynligheten for å oppleve hjerteinfarkt eller akutte hjerneepisoder. Økningen i røde blodlegemer bestemmer også en økning i blodtetthet som kan forårsake blodpropp; det er derfor ikke feil å tro at bivirkningene som sees hos pasienter, også kan oppstå hos friske idrettsutøvere. [Lage JM et al., 2002].
Hvis EPO ble introdusert genetisk, ville nivået og varigheten av erytropoietinproduksjonen være mindre kontrollerbar, slik at hematokrit ville gå videre på ubestemt tid til patologiske nivåer.
Det antas at behandling med IGF-1 kan føre til vekst av hormonavhengige svulster.
Det er derfor av avgjørende betydning at bruk av farmakogenetisk utvalgte vektorer har en velkjent og kontrollert genuttrykksmodell.
De eksakte metodene for å oppdage genetisk doping er ennå ikke etablert, også fordi DNA som overføres med genterapi er av menneskelig opprinnelse, derfor ikke forskjellig fra idrettsutøvere som bruker det.
Muskelterapier er begrenset til injeksjonsstedet eller til vevet i umiddelbar nærhet, derfor vil de fleste genteknologiene på musklene ikke kunne oppdages gjennom den klassiske antidopinganalysen av urin eller blodprøver; en muskelbiopsi ville være nødvendig, men det er for invasivt for å bli tenkt som et normalt middel for dopingkontroll.
Mange former for genetisk doping krever ikke direkte innføring av gener i ønsket organ; EPO -genet kan for eksempel injiseres i hvilken som helst del av kroppen og lokalt produsere proteinet som deretter kommer inn i sirkulasjonen. Å lete etter EPO -injeksjonsstedet ville være som å lete etter en nål i en høystakk.
I de fleste tilfeller vil imidlertid genetisk doping resultere i introduksjon av et gen som er en eksakt kopi av det endogene og som kan gi opphav til et protein som er helt identisk med det endogene i sine posttranslasjonelle modifikasjoner.
En fersk publikasjon indikerer at det er mulig å oppdage en forskjell mellom det medfødte proteinet og genterapiproduktet basert på det forskjellige mønsteret av glykosylering i forskjellige celletyper, det gjenstår å se om dette er tilfellet med alle typer genetisk doping [ Lasne F et al., 2004].
Offentlige myndigheter og idrettsorganisasjoner, inkludert Den internasjonale olympiske komité, har fordømt doping allerede på 1960 -tallet. Nylige fremskritt gjort med biologer vil ha stor innvirkning på arten av legemidler som er foreskrevet til pasienter, og vil også endre valg av legemidler som brukes til forbedre atletisk prestasjon.
Genterapi er utelukkende godkjent for klinisk testing av somatiske genterapiprodukter hos mennesker, og utelukker strengt tatt muligheten for å anse enhver form for human kimlinjeterapi som mulig.
Forbudet mot genetisk doping fra World Anti-Doping Agency (WADA) og internasjonale idrettsforbund gir et sterkt grunnlag for eliminering i idrett, men vil også avhenge av hvordan ulike forskrifter mottas av idrettsutøvere.
De fleste idrettsutøvere har ikke nok kunnskap til å fullt ut forstå den potensielle negative effekten av genetisk doping. Av denne grunn vil det være svært viktig at de og deres støtteapparat er godt opplært for å forhindre bruk. Idrettsutøvere må også være klar over risikoen forbundet med bruk av genetisk doping ved bruk i ukontrollerte anlegg, men uten kompromisser det uendelige potensialet som tilbys av offisiell genterapi for behandling av alvorlige patologier.
Legemiddelindustrien er godt klar over mulighetene og risikoene ved bruk av genetisk doping og ønsker å samarbeide om utvikling av forskning for påvisning av genprodukter som finnes i legemidlene. Den bør fortrinnsvis signere en kode der den forplikter seg til aldri å produsere eller selge, av en eller annen grunn, genetiske produkter for ikke-terapeutisk bruk.
Et begrenset antall mennesker fra forskjellige disipliner innen vitenskap og sport ble intervjuet, for å få en "ide om forestillingen og mulig innvirkning av genetisk doping på dem. Blant intervjuobjektene var det tre idrettsleger, en farmasøyt, fire eliteidrettsutøvere og fem forskere fra akademia og farmasøytisk industri; her er spørsmålene:
- Kjenner du til begrepet genetisk doping?
- Hva tror du dette begrepet betyr?
- Tror du på forbedret ytelse gjennom bruk av genetisk doping?
- Hva er etter din mening helserisikoen forbundet med bruk av genetisk doping?
- Er genetisk doping allerede brukt, eller vil det bare være i fremtiden?
- Blir det lett å oppdage genetisk doping?
Fra de forskjellige svarene er det klart at mennesker utenfor det vitenskapelige samfunnet har liten kunnskap om bruken av denne terapien; en vanlig frykt er at genterapi kan påvirke avkom, eller forårsake kreft. Genetisk doping vil være kompleks og forebyggende tiltak vanskelig. På den annen side insisterer alle på at genetisk doping vil bli brukt av idrettsutøvere så snart det er tilgjengelig, og at dette vil skje i løpet av de neste årene.
Fagfolk rundt eliteidrettsutøvere er svært bekymret for mulig bruk av genetisk doping og anbefaler utdanning av sine idrettsutøvere og deres medisinske støtteapparat, til støtte for utviklingen av forebyggende antidopingmåling. Disse fagpersonene er overbevist om at problemet med søknaden er av genetisk doping til idrettsutøvere vil oppstå i løpet av de neste årene, og at det vil bli ganske vanskelig å oppdage det.
Idrettens verden vil før eller siden stå overfor fenomenet genetisk doping; Det er vanskelig å anslå det eksakte antall år som må gå for at dette skal skje, men det kan antas at dette vil skje snart, i løpet av de neste årene (OL i Beijing 2008 eller senest i de påfølgende).
Fra sykling til vektløfting, svømming til fotball og ski, alle idretter kan ha nytte av genetisk manipulasjon: bare velg genet som forbedrer den nødvendige ytelsen! [Bernardini B., 2006].





















.jpg)



