For å kunne snakke på en forståelig måte om "hemoglobin (Hb), er det nyttig å ta vare på den første myoglobin (Mb) som er veldig lik hemoglobin, men er mye enklere. Mellom hemoglobin og myoglobin er det nære slektskapsforhold: begge er konjugerte proteiner og deres protetiske gruppe (ikke-proteindel) er gruppen heme.
Myoglobin er et globulært protein som består av en enkelt kjede på rundt hundre og femti aminosyrer (det avhenger av organismen) og dens molekylvekt er omtrent 18 Kd.
Som nevnt er den utstyrt med en hemagruppe som er satt inn i en hydrofob (eller lipofil) del av proteinet, bestående av folder som kan tilskrives a-helix-strukturene til de fibrøse proteinene.
Myoglobin består hovedsakelig av segmenter av α-helixer, tilstede i antall åtte og består nesten utelukkende av upolare rester (leucin, valin, metionin og fenylalanin) mens polare rester er praktisk talt fraværende (asparaginsyre, glutaminsyre, lysin og arginin); de eneste polare restene er to histidiner, som spiller en grunnleggende rolle for binding av oksygen til hemgruppen.
Hemgruppen er en kromoforgruppe (absorberes i det synlige) og er den funksjonelle gruppen til myoglobin.
Se også: glykert hemoglobin - hemoglobin i urinen
Litt kjemi

Bindingen mellom protoporfyrin og jern er en typisk binding av koordinasjonsforbindelser som er kjemiske forbindelser der et sentralt atom (eller ion) danner bindinger med andre kjemiske arter i et tall som er større enn dets oksidasjonsnummer (elektrisk ladning). Når det gjelder heme, er disse obligasjonene reversible og svake.
Koordinasjonstallet (antall koordinasjonsbindinger) til jern er seks: Det kan være seks molekyler rundt jernet som deler bindingselektronene.
For å danne en koordinasjonsforbindelse, krever det to orbitaler med riktig orientering: den ene er i stand til å "skaffe" elektroner og den andre er i stand til å donere dem.
I hem danner jern fire plane bindinger med de fire nitrogenatomer i midten av proto-porfyrinringen og en femte binding med et proksimalt histidinnitrogen; jern har den sjette frie koordinasjonsbindingen og det kan binde seg til oksygen.
Når jern er i form av et fritt ion, dets type orbitaler d de har alle den samme energien; i myoglobin er jernionen bundet til protoporfyrin og histidin: disse artene forstyrrer magnetisk orbitalene d litt jern; omfanget av forstyrrelsen vil være forskjellig for de forskjellige orbitalene d avhengig av deres romlige orientering og den forstyrrende arten. Siden orbitalenes totale energi må være konstant, forårsaker forstyrrelsen en energisk adskillelse mellom de forskjellige orbitalene: energien som er oppnådd av noen orbitaler tilsvarer energien tapt av de andre.
Hvis separasjonen som oppstår mellom orbitalene ikke er veldig stor, er et elektronisk arrangement med høyt spinn å foretrekke: bindingselektronene prøver å arrangere seg parallelle spinn i så mange undernivåer som mulig (maksimal multiplisitet); hvis forstyrrelsen derimot er veldig sterk og det er et stort skille mellom orbitalene, kan det være mer praktisk å koble bindingselektronene i orbitalene med lavere energi (lavt spinn).
Når jern binder seg til oksygen, antar molekylet et lavt spinnarrangement, mens når jern har den sjette koordinasjonsbindingen fri, har molekylet et høyt spinnarrangement.
Takket være denne spinnforskjellen, gjennom en spektral analyse av myoglobin, er vi i stand til å forstå om oksygen (MbO2) er bundet til det eller ikke (Mb).
Myoglobin er et typisk muskelprotein (men det finnes ikke bare i muskler).
Myoglobin ekstraheres fra spermhvalen der den er tilstede i store mengder og blir deretter renset.
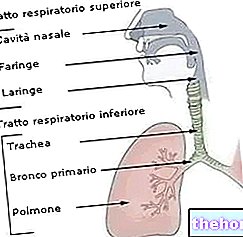
Hvaler har en åndedrett som mennesker: Å ha lunger må de absorbere luft gjennom respirasjonsprosessen; kaskelothvalen må bringe så mye oksygen som mulig inn i musklene som er i stand til å akkumulere oksygen ved å binde den til myoglobinet som er tilstede i dem; oksygenet frigjøres deretter sakte når hvalen senkes fordi stoffskiftet krever oksygen: jo større mengde oksygen som spermhvalen er i stand til å absorbere, og jo mer oksygen er tilgjengelig under dykket.
Myoglybin binder oksygen på en reversibel måte og er tilstede i perifere vev i en større prosentandel jo mer vev er vant til å arbeide med oksygenforsyninger som er fjerne i tid.
<--- Myoglobin er et protein som er tilstede i musklene, hvis funksjon nettopp er et oksygenreservoar.
Det som gjør kjøttet mer eller mindre rødt er innholdet av hemoproteiner (det er hemmen som gjør kjøttet rødt).
Hemoglobin har mange strukturelle likheter med myoglobin og er i stand til å binde molekylært oksygen på en reversibel måte; men mens myoglobin er begrenset til muskler og perifert vev generelt, finnes hemoglobin i erytrocytter eller røde blodlegemer (de er pseudoceller, det vil si at de ikke er virkelige celler) som utgjør 40% av blodet.
I motsetning til myoglobin er hemoglobins arbeid å ta oksygen i lungene, slippe det ut i cellene der det trengs, ta karbondioksid og slippe det ut i lungene der syklusen begynner igjen.
L "hemoglobin det er et tetrameter, det vil si at det består av fire polypeptidkjeder hver med en hemgruppe og identiske to og to (i et menneske er det to alfakjeder og to betakjeder).
Hovedfunksjonen til hemoglobin er transport av oksygen; en annen funksjon av blodet som hemoglobin er involvert i er transport av stoffer til vevet.
I veien fra lungene (rik på oksygen) til vevet, transporterer hemoglobin oksygen (samtidig når de andre stoffene vevene) mens det i den motsatte banen bærer det avfallet som samles inn av vevene, spesielt karbonet dioksid produsert i stoffskiftet.
I utviklingen av et menneske er det gener som bare uttrykkes i en viss periode; Av denne grunn er det forskjellige hemoglobiner: fostre, embryoner, hos den voksne mannen.
Kjedene som utgjør disse forskjellige hemoglobinene har forskjellige strukturer, men med noen likheter er faktisk funksjonen de utfører mer eller mindre den samme.
En forklaring på tilstedeværelsen av flere forskjellige kjeder er følgende: i løpet av organismenes evolusjonære prosess har til og med hemoglobin utviklet seg som spesialiserer seg på transport av oksygen fra områder som er rike på det til områder som er mangelfulle. I begynnelsen av evolusjonskjeden l "hemoglobin transporterte oksygen i små organismer; i løpet av evolusjonen nådde organismer større dimensjoner, derfor ble hemoglobinet modifisert for å kunne transportere oksygen til områder lenger unna punktet der det var rikt på det; til Gjør dette de har blitt kodet, i løpet av den evolusjonære prosessen, nye strukturer i kjedene som utgjør hemoglobin.
Myoglobin binder oksygen selv ved beskjedent trykk; i det perifere vevet er det et trykk (PO2) på omtrent 30 mmHg: myoglobin ved dette trykket frigjør ikke oksygen, så det ville være ineffektivt som en oksygenbærer. Hemoglobinet derimot , det har en mer elastisk oppførsel: det binder oksygen til høyt trykk og frigjør det når trykket synker.
Når et protein er funksjonelt aktivt, kan det endre formen litt; for eksempel har oksygenert myoglobin en annen form enn ikke-oksygenert myoglobin, og denne mutasjonen påvirker ikke naboene.
Situasjonen er annerledes når det gjelder assosierte proteiner som hemoglobin: når en kjede oksygner, blir den indusert til å endre form, men denne modifiseringen er tredimensjonal, så de andre kjedene i tetrameteret påvirkes også. Det faktum at kjedene er forbundet med hverandre., antyder at endringen av den ene påvirker de andre naboene, selv om den er i en annen grad; når en kjede oksygenerer, antar tetrameterets andre kjeder en "mindre fiendtlig holdning" til oksygen: vanskeligheten med en kjede den oksygenater reduseres når kjedene i nærheten av det oksygenereres igjen. Det samme gjelder deoksygenering.
Den kvartære strukturen til deoksyhemoglobin kalles T (spent) form mens oksyhemoglobin kalles R (frigjort) form; i den anspente tilstanden er det en rekke ganske sterke elektrostatiske interaksjoner mellom sure aminosyrer og basiske aminosyrer som fører til en stiv struktur av deoksyhemoglobin (dette er grunnen til den "spente formen"), mens når oksygen er koblet, er enheten til disse interaksjoner avtar (derav den "frigitte formen"). Videre, i fravær av oksygen, blir ladningen av histidinet (se struktur) stabilisert av den motsatte ladningen av asparaginsyren, mens det i nærvær av oksygen er en tendens fra proteinets side til å miste et proton; alt dette innebærer at oksygenert hemoglobin er en sterkere syre enn deoksygenert hemoglobin: bohr -effekt.
Avhengig av pH binder hemegruppen mer eller mindre lett til oksygen: i et surt miljø frigjør hemoglobin lettere oksygen (den spente formen er stabil), mens bindingen med oksygen i et grunnleggende miljø er vanskeligere.

Hvert hemoglobin frigjør 0,7 protoner per mol oksygen (O2) som kommer inn.
Bohr -effekten gjør at hemoglobin kan forbedre evnen til å transportere oksygen.
Hemoglobinet som beveger seg fra lungene til vevet må balansere seg selv som en funksjon av trykk, pH og temperatur.
La oss se effekten av temperaturen.
Temperaturen i lunge-alveolene er omtrent 1-1,5 ° C lavere enn den ytre temperaturen, mens temperaturen i musklene er omtrent 36,5-37 ° C; når temperaturen øker, faller metningsfaktoren (ved samme trykk): dette skjer fordi kinetisk energi øker og dissosiasjon favoriseres.

Det er andre faktorer som kan påvirke hemoglobins evne til å binde seg til oksygen, hvorav den ene er konsentrasjonen av 2,3 bisfosfoglyserat.
2,3 bisfosfoglyserat er en metabolsk tilstede i erytrocytter i en konsentrasjon på 4-5 mM (i ingen andre deler av organismen er den tilstede i en så høy konsentrasjon).
Ved fysiologisk pH er 2,3 bisfosfoglyserat deprotonert og har fem negative ladninger på seg; den er klemt mellom de to betakjedene til hemoglobin fordi disse kjedene har en høy konsentrasjon av positive ladninger. De elektrostatiske interaksjonene mellom betakjedene og 2,3 bisfosfoglyseratet gir systemet en viss stivhet: en spenst struktur oppnås som har liten affinitet for oksygen; under oksygenering blir 2,3 bisfosfoglyseratet deretter utvist.
I erytrocytter c "er et spesielt apparat som omdanner 1,3 bisfosfoglyserat (produsert ved metabolisme) til 2,3 bisfosfoglyserat slik at det når en konsentrasjon på 4-5 mM og derfor er hemoglobinet i stand til å utveksle" oksygen i vevet.
Hemoglobinet som kommer til et vev er i frigitt tilstand (bundet til oksygen), men i nærheten av vevet blir det karboksylert og går over til den spente tilstanden: proteinet i denne tilstanden har mindre tendens til å binde seg med oksygen, med respekt til frigjort tilstand, derfor frigjør hemoglobin oksygen til vevet; Videre er det ved reaksjon mellom vann og karbondioksid produksjon av H + -ioner, derfor ytterligere oksygen på grunn av bohr -effekten.
Karbondioksid diffunderer inn i erytrocyten som passerer gjennom plasmamembranen; siden erytrocytter utgjør omtrent 40% av blodet, bør vi forvente at bare 40% av karbondioksidet som diffunderer fra vevet kommer inn i dem, faktisk kommer 90% av karbondioksidet inn i erytrocytter fordi de inneholder et enzym som omdanner karbondioksid i kolsyre resulterer det i at den stasjonære konsentrasjonen av karbondioksid i erytrocytter er lav og derfor er inngangshastigheten høy.

Et annet fenomen som oppstår når en erytrocyt når et vev er følgende: ved gradient forlater "HCO3- (derivat av karbondioksid)" erytrocyt, og for å balansere utgangen av en negativ ladning har vi "oppføring av klorider som bestemmer en økning i osmotisk trykk: for å balansere denne variasjonen er det også vanninnføring som forårsaker hevelse av erytrocyt (HAMBURGER -effekt) Det motsatte fenomenet oppstår når en erytrocyt når lungealveolene: en deflasjon av erytrocytter (HALDANE -effekt) Derfor er de venøse erytrocytter (rettet mot lungene) rundere enn de arterielle.