Trypsin og kymotrypsin er to viktige enzymer i fordøyelsen av matproteiner. Begge blir produsert og utskilt som zymogener, dvs. i inaktiv form, av bukspyttkjertelen; zymogenforløperen til trypsin kalles trypsinogen, mens kymotrypsin kalles chymotrypsinogen.
Trypsin og kymotrypsin tilhører den store familien proteolytiske enzymer (involvert i fordøyelsen av proteiner) og undergruppen av endopeptidaser. Disse stoffene - inkludert gastrisk pepsin og bukspyttkjertelelastase - angriper peptidbindinger i aminosyrekjeden, noe som gir opphav til mindre molekylære fragmenter. Enzymene som tilhører den andre gruppen, eksopeptidasenes, fullfører arbeidet med trypsin og kymotrypsin og løsner enkelt aminosyrer fra endene av peptidkjeden; bukspyttkjertelen karboksypeptidaser (A1, A2 og B, som angriper karboksylenden), men også aminopeptidasene (som angriper den aminoterminale enden) og dipeptidaser, både produsert og utskilt av slimhinnen i tynntarmen, tilhører denne familien. karboksypeptidase, ligner det man har sett for trypsin (trypsinogen) og chymotrypsin (chymotrypsinogen), skilles ut av bukspyttkjertelen i en inaktiv form.I alle tre tilfellene er enzymet som er involvert i den enzymatiske aktiveringsprosessen enteropeptidase, et protein som produseres og utskilles av cellene av duodenalslimhinnen; nærmere bestemt er enteropeptidase spesifikk for trypsinogen, som en gang omdannet til trypsin også aktiverer de andre proteolytiske enzymene, inkludert det samme trypsinogenet.
La oss kort huske at tolvfingertarmen er den første delen av tynntarmen, og at ikke bare bukspyttkjertelsaft strømmer inn i den, men også leverjuice (galle), avgjørende for pH -korreksjon og lipidfordøyelse.

De funksjonelle forskjellene mellom trypsin og kymotrypsin angår ganske enkelt deres spesifisitet, det vil si evnen til å gjenkjenne og splitte bare bindingene dannet av spesifikke aminosyrer. Trypsin virker fremfor alt på peptidbindinger som engasjerer grunnleggende aminosyrer (som arginin og lysin), mens kymotrypsin hovedsakelig hydrolyserer bindinger som involverer tyrosin, fenylalanin, tryptofan, leucin og metionin.
Takket være de forskjellige proteolytiske enzymer, med bidrag fra magesyre, brytes proteiner i dietten - opprinnelig dannet av flere titalls aminosyrer - ned i dipeptider, tripeptider og frie aminosyrer, alle lett absorberbare stoffer som kommer fra kapillærene til tarmslimhinnen transportert til leveren.
Trypsin og kymotrypsin i avføringen
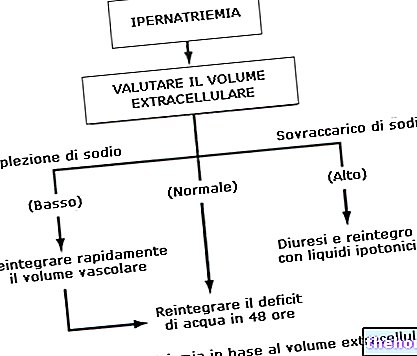
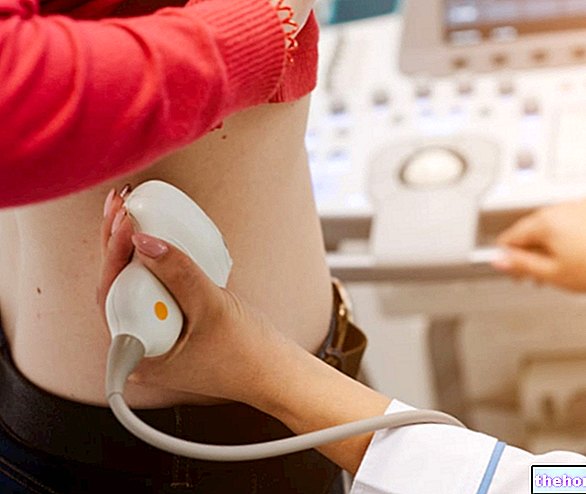
Bestemmelsen av kymotrypsin og trypsin i avføring brukes, og var det spesielt tidligere, som en indirekte test av funksjonell kapasitet til den eksokrine bukspyttkjertelen. Hvis noe på nivået av denne kjertelen ikke fungerer som det skal, er det logisk å forvente en redusert syntese av trypsin og kymotrypsin, som også vil være mangelfull i avføringen. Testen har god sensitivitet, men er belastet med den reelle risikoen for falske positive og falske negativer. Bruk av avføringsmidler, for eksempel, reduserer konsentrasjonen av enzymer i fekalt materiale, mens inntak av pankreas fordøyelsesekstrakter (som pankreatin) eller grønnsaker (som ananasstengel, papaya, papain og bromelain) forårsaker falske negative resultater. tarmfloraen påvirker også litt mengden trypsin og kymotrypsin som kommer uendret i avføringen; av denne grunn kan bruk av antibiotika gi falske negativer; tvert imot, i nærvær av divertikulose og andre forhold som favoriserer bakteriell spredning, kan det registreres falske positive resultater.
En klassisk anvendelse av trypsin- og kymotrypsinanalysen i avføring er påvisning av bukspyttkjertelinsuffisiens hos pasienter med cystisk fibrose.En av konsekvensene av denne sykdommen er nedsatt normal transport av trypsin og andre fordøyelsesenzymer fra bukspyttkjertelen. Til tolvfingertarmen. Av denne grunn, ved fødselen, er avføringen til barnet med cystisk fibrose spesielt kompakt for å forårsake tarmobstruksjon, og derfor er det spesielt små mengder kymotrypsin og trypsin i mekonium.