Aktive ingredienser: Betamethason, Tetrizoline (Tetrizoline hydrochloride)
BIORINIL 0,05% + 0,1% nesespray, suspensjon
Hvorfor brukes Biorinil? Hva er den til?
FARMAKOTERAPEUTISK KATEGORI
Preparat som inneholder et antiinflammatorisk steroid og en vasokonstriktor, tetrizolinhydroklorid.
TERAPEUTISKE INDIKASJONER
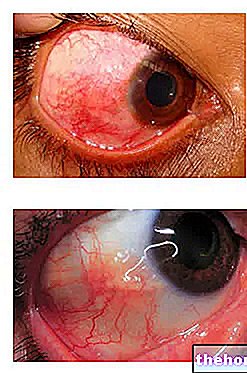
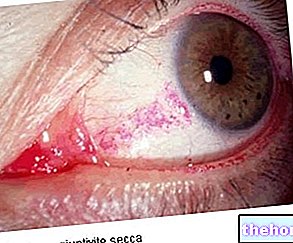
Akutt og subakutt rhinitt, bihulebetennelse, nasofaryngitt
Kontraindikasjoner Når Biorinil ikke skal brukes
Overfølsomhet overfor virkestoffene eller overfor noen av hjelpestoffene.
Glaukom, prostatahypertrofi, alvorlig hjertesykdom, hypertensjon, hypertyreose, alvorlig nyreinsuffisiens.
Ikke administrer under eller i to uker etter antidepressiv behandling.
Tuberkuløse, sopp- og virusinfeksjoner i slimhinnene som skal behandles.
Legemidlet kan ikke tas av barn under 12 år.
Forholdsregler for bruk Hva du må vite før du bruker Biorinil
Bruk, spesielt hvis det forlenges, av et produkt for lokal bruk kan gi opphav til sensibiliseringsfenomener.
Hos pasienter med hjerte- og karsykdommer og spesielt hos hypertensive pasienter, må bruk av nesedekongestanter underkastes legens vurdering fra tid til annen.
Langvarig bruk av preparater som inneholder vasokonstriktorer kan endre normal funksjon av neseslimhinnen og paranasale bihuler, og også forårsake avhengighet av stoffet. Gjentatte applikasjoner i lange perioder kan derfor være skadelig.
Imidlertid ikke bruk for mer enn fire dager på rad.
Benzalkoniumklorid (BAC) som et konserveringsmiddel i BIORINIL, spesielt når det brukes i lange perioder, kan forårsake hevelse i neseslimhinnen. Hvis det er mistanke om en slik reaksjon (vedvarende nesestopp), bør en BAC-fri nesemedisin brukes om mulig. Hvis slike nesemedisiner uten BAC ikke er tilgjengelige, bør en annen farmasøytisk form vurderes.
Det kan forårsake bronkospasme. Irriterer, kan forårsake lokale hudreaksjoner.
Det er viktig å ta dosen medisin som beskrevet i pakningsvedlegget eller som foreskrevet av legen din. Bare dosen anbefalt av legen din skal brukes; bruk av høyere eller lavere doser kan føre til forverring av symptomene.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Biorinil
På grunn av tilstedeværelsen av tetrizolin, bør produktet ikke administreres til pasienter under behandling med mono-amino-oksidasehemmere.
Fortell legen din dersom du bruker eller nylig har brukt andre legemidler, også reseptfrie.
Advarsler Det er viktig å vite at:
Bruk med forsiktighet hos pasienter med kardiovaskulære og metabolske endokrine lidelser.
Graviditet og amming
Hos gravide kvinner bør produktet administreres ved reelt behov, under direkte medisinsk tilsyn.
Rådfør deg med lege eller apotek før du tar medisiner.
Kjøring og bruk av maskiner
BIORINIL påvirker ikke evnen til å kjøre bil eller bruke maskiner.
Dose, metode og administrasjonstidspunkt Hvordan bruke Biorinil: Dosering
For nesespray (1 eller 2 spray per nesebor) tre eller fire ganger om dagen.
Hver spray gir 0,08 ml produkt.
Instruksjoner for bruk
- Rist flasken.
- Ved første gangs bruk, for å aktivere dispenseren, trykker du ned med indeksen og langfingeren til det kommer ut en spray.
- Lever produktet i neseborene.
Etter bruk, hold dispensertuten dekket med støvlokket.
Overdosering Hva du skal gjøre hvis du har tatt en overdose av Biorinil
Ved utilsiktet inntak av overdreven dose BIORINIL, må du varsle legen din umiddelbart eller gå til nærmeste sykehus.
Produktet, hvis det inntas ved et uhell eller hvis det brukes i store doser over en lengre periode, kan forårsake giftige fenomener.
Utilsiktet inntak av stoffet kan forårsake systemiske effekter forårsaket av systemisk absorpsjon av vasokonstriktoren, for eksempel hodepine, arteriell hypertensjon, modifisering av hjerterytmen, urinforstyrrelser, rastløshet og søvnløshet.
Absorpsjon av kortikosteroider kan også forårsake systemiske effekter (Cushings syndrom, hemming av hypofysen-binyreaksen) og, mer sjelden, en rekke psykologiske eller atferdsmessige effekter, inkludert psykomotorisk hyperaktivitet, søvnforstyrrelser, angst, depresjon eller aggresjon (spesielt hos barn).
Hvis dette skjer, er det nødvendig med passende nødstilfeller.
Bivirkninger Hva er bivirkningene av Biorinil
Lokalt kan sensitiviseringsreaksjoner og rebound -overbelastning oppstå.
Systemiske bivirkninger er ekstremt usannsynlige på grunn av både de lave dosene som brukes og administrasjonsveien; Imidlertid kan utseendet deres favoriseres av behandlinger som utføres i lengre perioder.
I dette tilfellet kan absorpsjon av sympatisk-mimetiske stoffer forårsake systemiske effekter som hodepine, arteriell hypertensjon, endring i hjerterytmen, urinforstyrrelser, rastløshet og søvnløshet. Absorpsjon av kortikosteroider kan også forårsake systemiske effekter (Cushings syndrom, hemning av hypofysen-binyreaksen).
Systemiske effekter kan oppstå med intranasale kortikosteroider, spesielt når det foreskrives i høye doser i lengre perioder.
Som alle andre legemidler kan BIORINIL forårsake bivirkninger, men ikke alle får det.
Overholdelse av instruksjonene i pakningsvedlegget reduserer risikoen for bivirkninger.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige, eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Utløpsdato: se utløpsdatoen som er trykt på pakken.
Den angitte utløpsdatoen refererer til produktet i intakt emballasje, riktig lagret.
Advarsel: ikke bruk medisinen etter utløpsdatoen som er angitt på pakningen.
Må ikke oppbevares over 25 ° C.
Legemidler skal ikke kastes i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Oppbevar dette legemidlet utilgjengelig for barn.
Deadline "> Annen informasjon
SAMMENSETNING
100 ml suspensjon inneholder:
Aktive prinsipper:
- Betametason 0,05 g
- Tetrizolin hydroklorid 0,1 g
Hjelpestoffer: Benzalkoniumklorid, Dinatriumedetat, Polysorbat 60, Polysorbat 80, Dinatriumfosfatdodecahydrat, Natriummonobasisk fosfatdihydrat, Natriumklorid, Renset vann.
Benzalkoniumklorid er irriterende og kan forårsake lokale hudreaksjoner.
LEGEMIDDELFORM OG INNHOLD
BIORINIL 0,05% + 0,1% nesespray, suspensjon - 1 flaske
10 ml nesesprayflaske med selvdoserende sprayventil.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN -
BIORINIL 0,05% + 0,1%
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING -
100 ml suspensjon inneholder:
Betametason 0,05 g
Tetrizolin hydroklorid 0,1 g.
For hjelpestoffer, se 6.1.
03.0 LEGEMIDDELFORM -
Nesespray, suspensjon
04.0 KLINISK INFORMASJON -
04.1 Terapeutiske indikasjoner -
Akutt og subakutt rhinitt, bihulebetennelse, nasofaryngitt.
04.2 Dosering og administrasjonsmåte -
For nesespray (1 eller 2 spray per nesebor) tre eller fire ganger om dagen.
Hver spray gir 0,08 ml produkt.
04.3 Kontraindikasjoner -
Overfølsomhet overfor virkestoffene eller overfor noen av hjelpestoffene.
Glaukom, prostatahypertrofi, alvorlig hjertesykdom, hypertensjon, hypertyreose, alvorlig nyreinsuffisiens.
Ikke administrer under eller i to uker etter antidepressiv behandling.
Tuberkuløse, sopp- og virusinfeksjoner i slimhinnene som skal behandles.
Legemidlet er kontraindisert hos barn under 12 år.
04.4 Spesielle advarsler og passende forholdsregler for bruk -
Systemiske effekter kan oppstå med intranasale kortikosteroider, spesielt når det foreskrives i høye doser over lengre perioder. Disse effektene er mindre sannsynlige enn ved oral kortikosteroidbehandling og kan variere hos individuelle pasienter og mellom forskjellige kortikosteroidpreparater. Mulige systemiske effekter inkluderer Cushings syndrom, Cushingoid -funksjoner, adrenal suppresjon, veksthemming hos barn og ungdom, redusert beinmineraltetthet, grå stær, glaukom og, mer sjelden, en rekke psykologiske eller atferdsmessige effekter, inkludert psykomotorisk hyperaktivitet, søvnforstyrrelser, angst, depresjon eller aggresjon (spesielt hos barn).
Bruk, spesielt hvis det forlenges, av et produkt for lokal bruk kan gi opphav til sensibiliseringsfenomener.
Hos pasienter med hjerte- og karsykdommer og spesielt hos hypertensive pasienter, må bruk av nesedekongestanter underkastes legens vurdering fra tid til annen.
Langvarig bruk av preparater som inneholder vasokonstriktorer kan endre normal funksjon av neseslimhinnen og paranasale bihuler, og også forårsake avhengighet av stoffet. Gjentatte applikasjoner i lange perioder kan derfor være skadelig.
Imidlertid ikke bruk for mer enn fire dager på rad.
Bruk med forsiktighet hos pasienter med kardiovaskulære og metabolske endokrine lidelser.
Oppbevares utilgjengelig for barn.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon -
På grunn av tilstedeværelsen av tetrizolin, bør produktet ikke administreres til pasienter under behandling med mono-amino-oksidasehemmere.
04.6 Graviditet og amming -
Hos gravide kvinner bør produktet administreres i tilfeller av reelt behov, under direkte tilsyn av legen.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner -
BIORINIL påvirker ikke evnen til å kjøre bil og bruke maskiner.
04.8 Bivirkninger -
Systemiske effekter kan oppstå med intranasale kortikosteroider, spesielt når det foreskrives i høye doser over lengre perioder.
Disse kan inkludere veksthemming hos barn og ungdom.
Lokalt kan sensitiviseringsreaksjoner og rebound -overbelastning oppstå.
Systemiske bivirkninger er ekstremt usannsynlige på grunn av både de lave dosene som brukes og administrasjonsveien; Imidlertid kan utseendet deres favoriseres av behandlinger som utføres i lengre perioder.
I dette tilfellet kan absorpsjon av sympatisk-mimetiske stoffer forårsake systemiske effekter som hodepine, arteriell hypertensjon, endring i hjerterytmen, urinforstyrrelser, rastløshet og søvnløshet. Absorpsjon av kortikosteroider kan også forårsake systemiske effekter (Cushings syndrom, hemning av hypofysen-binyreaksen).
04.9 Overdosering -
Det er ikke rapportert tilfeller av overdosering.
05.0 FARMAKOLOGISKE EGENSKAPER -
05.1 "Farmakodynamiske egenskaper -
Farmakoterapeutisk gruppe: preparat som inneholder et antiinflammatorisk steroid og en vasokonstriktor, tetrizolinhydroklorid.
ATC -kode: R01AD06.
De farmakologiske egenskapene kan utledes av egenskapene til de enkelte bestanddelene:
Betamethason: Betamethason og dets derivater er utstyrt for lokal administrasjon med høy antiinflammatorisk aktivitet, og dessuten tolereres administrering ved innånding godt.
Aktiviteten til dette steroidet, mye demonstrert i litteraturen, er estimert til å være omtrent 25 ganger høyere enn for kortisol og 8 ganger høyere enn for prednisolon.
Videre kan administrering ved innånding, ikke bare forhindre inhibering av hypothalamus-hypofyse-binyre-aksen, men fortsette å utføre en effektiv terapeutisk handling, tillate gjenoppretting av funksjonalitet hos personer som tidligere var deprimert ved systemisk steroidbehandling.
Tetrizoline hydrochloride: Sympatomimetisk legemiddel som utvikler nesedekongestant virkning på grunn av sin vasokonstriktive aktivitet.
05.2 "Farmakokinetiske egenskaper -
Ikke relevant.
05.3 Prekliniske sikkerhetsdata -
Farmakologiske studier, som tar sikte på å bestemme toleransen for en kombinasjon som inneholder lignende aktive ingredienser, har avdekket ikke-interferens mellom kortikosteroid og tetrizolin.
06.0 LEGEMIDDELOPPLYSNINGER -
06.1 Hjelpestoffer -
Benzalkoniumklorid, dinatriumedetat, polysorbat 60, polysorbat 80, dinatriumfosfatdodecahydrat, monobasisk natriumfosfatdihydrat, natriumklorid og renset vann.
06.2 Uforlikelighet "-
Ingen kjent før nå.
06.3 Gyldighetsperiode "-
2 år.
06.4 Spesielle forholdsregler ved lagring -
Må ikke oppbevares over 25 ° C.
06.5 Emballasje og innhold i emballasje -
10 ml ugjennomsiktig plast nesesprayflaske med automatisk doseringssprayventil.
06.6 Bruksanvisning og håndtering -
Ingen spesielle instruksjoner.
07.0 INNEHAVER AV "MARKEDSFØRINGSTILLATELSEN" -
THEA FARMA S.p.A. Via Giotto, 36 - 20145 Milan
08.0 MARKEDSFØRINGSTILLATELSESNUMMER -
A.I.C. nr 019133038
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN -
Mai 1966 / mai 2010
10.0 DATO FOR REVISJON AV TEKSTEN -
Mai 2012