Aktive ingredienser: Epoetin zeta
Retacrit 1 000 IE / 0,3 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
Retacrit 2000 IE / 0,6 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
Retacrit 3000 IE / 0,9 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 4000 IE / 0,4 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 5000 IE / 0,5 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 6000 IE / 0,6 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
Retacrit 8 000 IE / 0,8 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 10 000 IE / 1 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 20 000 IE / 0,5 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Retacrit 30 000 IE / 0,75 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
Retacrit 40 000 IE / 1 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
Indikasjoner Hvorfor brukes Retacrit? Hva er den til?
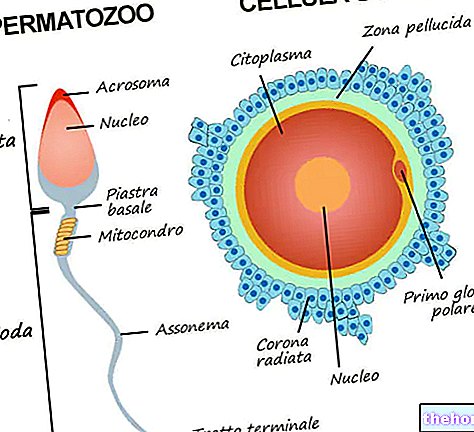
Retacrit inneholder et protein kalt epoetin zeta som stimulerer benmargen til å lage flere røde blodlegemer i blodet som bærer hemoglobin (et stoff som binder oksygen). Epoetin zeta er en kopi av det humane proteinet erytropoietin og fungerer på samme måte.
Retakrit brukes:
- hos voksne, barn og unge pasienter som gjennomgår hemodialyse, for behandling av symptomatisk anemi (redusert antall røde blodlegemer) forbundet med kronisk nyresvikt (nyresykdom);
- hos voksne pasienter som gjennomgår peritonealdialyse, for behandling av symptomatisk anemi assosiert med kronisk nyresvikt (nyresykdom);
- hos voksne pasienter med nyreinsuffisiens som ennå ikke er under dialyse, for behandling av alvorlig anemi assosiert med nyresykdom ledsaget av kliniske symptomer;
- hos voksne pasienter som får cellegift mot solide svulster, malignt lymfom (kreft i lymfesystemet) eller myelomatose (kreft i benmargen) for å behandle anemi og redusere behovet for blodoverføringer, hvis legen bestemmer eksistensen av høy risiko for trenger transfusjoner; - hos pasienter med moderat anemi som er kandidater til kirurgi for bloddonasjon før operasjonen, slik at de kan motta eget blod under eller etter operasjonen (autolog predonasjon);
- hos moderat anemiske voksne pasienter planlagt for større ortopedisk (bein) kirurgi (f.eks. hofte- eller kneutskiftningsterapi) for å redusere behovet for blodoverføringer.
Kontraindikasjoner Når Retacrit ikke skal brukes
Ikke bruk Retacrit:
- dersom du er allergisk mot erytropoietiner eller noen av de andre innholdsstoffene i dette legemidlet (listet opp i avsnitt 6)
- hvis du har utviklet en sykdom som kalles 'Pure Red Cell Aplasia' (PRCA) etter behandling med alle typer erytropoietin
- hvis du har høyt blodtrykk som ikke kan kontrolleres tilstrekkelig med spesifikke medisiner som senker blodtrykket
- hvis du ikke kan ta medisiner for å tynne blodet
- hvis du donerer blod før operasjonen og:
- har hatt hjerteinfarkt eller hjerneslag i måneden før behandling
- lider av ustabil angina pectoris (nylig eller økende brystsmerter)
- er i fare for at det dannes blodpropper i venene (dyp venetrombose); for eksempel hvis du tidligere har lidd av trombose.
- Hvis du skal gjennomgå en større ortopedisk kirurgi som hofte- eller kneutskiftning, og:
- har alvorlige hjerte- eller blodsirkulasjonsproblemer i vener eller arterier
- nylig har hatt hjerteinfarkt eller hjerneslag.
Forholdsregler for bruk Hva du må vite før du bruker Retacrit
Fortell legen din før du bruker Retacrit hvis du vet at du har lidd eller lider av en av følgende sykdommer:
- Beslag
- leversykdom
- svulster
- anemi på grunn av andre årsaker
- hjertesykdom (for eksempel angina pectoris)
- blodsirkulasjonsforstyrrelser som forårsaker prikkende følelser i ekstremiteter, kalde hender eller føtter eller muskelkramper i bena
- trombose eller koagulasjonssykdommer
- nyresykdom.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Retacrit
Fortell legen din eller apoteket dersom du bruker eller nylig har brukt andre legemidler.
Spesielt hvis du tar et legemiddel som inneholder virkestoffet cyklosporin, for å hemme immunsystemet etter en nyretransplantasjon, kan legen din beordre spesifikke tester for å måle konsentrasjonen av cyklosporin i blodet under behandling med Retacrit.
Å ta jerntilskudd og andre blodstimulerende midler kan øke effekten av Retacrit. Legen din vil avgjøre om du skal fortsette å ta disse stoffene eller ikke.
Advarsler Det er viktig å vite at:
Under behandling med Retacrit
Legen din vil kontrollere at hemoglobinet ditt ikke overskrider et visst nivå, ettersom høye konsentrasjoner av hemoglobin kan utgjøre en risiko for helsen til hjertet eller blodårene og kan øke risikoen for hjerteinfarkt, hjerneslag og død.
Leger bør prøve å holde hemoglobinnivået mellom 10 og 12 g / dl. Hemoglobinnivået bør ikke overstige 12 g / dl.
Legen din vil kontrollere blodtrykket ditt jevnlig mens du bruker Retacrit. Hvis du opplever hodepine, spesielt plutselig, dunkende migrene, eller hvis du begynner å føle deg forvirret eller får anfall, må du fortelle det til lege eller sykepleier umiddelbart.
Disse symptomene kan faktisk være advarselstegnene for en plutselig økning i blodtrykket, en situasjon som vil kreve akutt terapeutisk inngrep.
En økning i blodplatene (celler som bidrar til blodpropp) kan oppstå under behandling med dette legemidlet. Dette fenomenet bør bli bedre i løpet av behandlingen. Vi anbefaler at du sjekker antall blodplater regelmessig i løpet av de første 8 ukene av behandlingen.
Hvis du gjennomgår en medisinsk undersøkelse på et sykehus eller en privat klinikk, eller tar blodprøver, husk å informere legen din om Retacrit -behandlingen du følger, da dette legemidlet kan endre tilstanden og testresultatene.
Vær spesielt oppmerksom på andre produkter som stimulerer produksjonen av røde blodlegemer:
Retacrit er en av en gruppe produkter som stimulerer produksjonen av røde blodlegemer, det samme gjør det humane proteinet erytropoietin. Helsepersonellet vil alltid registrere det eksakte navnet på produktet de bruker.
Pasienter med nyresykdom
Sjeldne tilfeller av Pure Red Cell Aplasia (PRCA) har blitt rapportert etter måneder eller år med behandling med andre erytropoietinholdige medisiner; denne muligheten kan ikke utelukkes med Retacrit.
Spesifikk rød celle aplasi innebærer mangel på benmarg til å produsere nok røde blodlegemer. I dette tilfellet kan det oppstå en alvorlig anemistilstand, hvis symptomer er: uvanlig tretthet, svimmelhet eller kortpustethet. Røde celleaplasi kan skyldes produksjon av antistoffer rettet mot det injiserte erytropoietinet og deretter mot erytropoietinet produsert av den samme organismen.
Diskuter denne informasjonen med legen din. Hvis denne aplasien, men sjelden sykdom, skulle oppstå, vil behandlingen med Retacrit bli avbrutt, og legen vil bestemme hva han skal gjøre for å behandle anemien på den mest effektive måten.Du bør vite at hvis denne komplikasjonen, men sjelden, skulle oppstå, du må slutte å ta Retacrit og få regelmessige, og muligens livslange, blodoverføringer for behandling av anemi. Fortell legen din umiddelbart hvis du plutselig føler deg veldig trøtt eller føler deg kortpustet. Legen din vil avgjøre hvor effektiv Retacrit er for deg og stoppe behandlingen om nødvendig.
Pasienter med kronisk nyresvikt som behandles med erytropoietin må gjennomgå tester med jevne mellomrom for å måle nivået av hemoglobin (den delen av de røde blodcellene som bærer oksygen) til et konstant nivå er nådd, og deretter med intervaller. Periodisk, for å minimere risiko for økt blodtrykk.
Hvis du har kronisk nyresvikt, og spesielt hvis du ikke svarer tilstrekkelig på Retacrit, vil legen din sjekke dosen Retacrit du får fordi, hvis du ikke reagerer på behandling, kan gjentatte doser av Retacrit øke risikoen for problemer i hjertet eller blodårene og kan øke risikoen for hjerteinfarkt, hjerneslag og død.
En økning i kaliumnivået i blodet har blitt observert i isolerte tilfeller. Hos pasienter med kronisk nyresvikt kan korreksjon av anemi føre til økt appetitt og absorpsjon av kalium og protein. Hvis du er i dialysebehandling når Retacrit -behandlingen starter, må du kanskje justere dialyseparametere for å beholde urea, kreatinin- og kaliumnivåer innenfor ønsket område, og legen din vil bestemme.
Hos pasienter med kronisk nyresvikt bør serumelektrolytter (stoffer som finnes i blodet) overvåkes. Hvis serumkaliumverdier er høye (eller økende), bør det vurderes å avbryte administrering av Retacrit til disse verdiene er korrigert.
Under behandling med Retacrit er det ofte nødvendig under hemodialyse å øke dosen av heparin, et bestemt blodfortynnende stoff, for å minimere risikoen for blodpropper.Hvis denne dosen heparin ikke er optimal, er det mulig at en okklusjon oppstår i dialysatoren.
Kreftpasienter
Kreftpasienter er mer sannsynlig å få trombose hvis de tar erytropoietinlignende legemidler som Retacrit (se avsnitt 4.) Du bør derfor snakke med legen din om fordelene med Retacrit, spesielt hvis du er overvektig eller tidligere har hatt problemer med trombose. . eller blodproppssykdommer.
Kreftpasienter som behandles med erytropoietin må gjennomgå laboratorietester med jevne mellomrom for å måle nivået av hemoglobin (den delen av de røde blodcellene som bærer oksygen) til et konstant nivå er nådd, og deretter med tidsfrister. Periodisk.
Hvis du har kreft, bør du være oppmerksom på at Retacrit kan fungere som en vekstfaktor for blodceller, og at det i noen tilfeller kan ha negative effekter på kreften. Avhengig av den spesifikke situasjonen kan en blodtransfusjon være å foretrekke. Diskuter dette med legen din.
Graviditet og amming
Rådfør deg med lege eller apotek før du bruker dette legemidlet hvis du er gravid eller ammer eller tror du er gravid, eller planlegger å bli gravid.
Hvis du er gravid eller ammer, bør Retacrit bare brukes hvis de potensielle fordelene oppveier den potensielle risikoen for barnet.
Spør legen din om råd før du tar medisiner.
Kjøring og bruk av maskiner
Retacrit har ingen eller svært liten innflytelse på evnen til å kjøre bil eller bruke maskiner.
Retacrit inneholder fenylalanin
Denne medisinen inneholder fenylalanin, et stoff som kan være farlig for personer med fenylketonuri (en enzymmangel av genetisk opprinnelse som forårsaker en økning i eliminering av et kjemisk stoff (fenylketon) i urinen og kan forårsake lidelser i nervesystemet).
Retacrit inneholder natrium
Dette legemidlet inneholder mindre enn 1 mmol natrium (23 mg) per dose, noe som betyr at det regnes som 'natriumfritt'.
Dosering og bruksmåte Hvordan bruke Retacrit: Dosering
Retakritbehandling startes vanligvis under medisinsk tilsyn. Retacrit -injeksjoner kan gis av lege, sykepleier eller annet helsepersonell.
Hvis Retacrit injiseres under huden (subkutant), etter at du har sett hvordan du gjør det, kan du også injisere løsningen selv. Bruk alltid dette legemidlet nøyaktig slik legen din har fortalt deg. Hvis du er usikker, snakk med legen din.
Doseinformasjon
Dosering er basert på kroppsvekt i kilo. Legen din vil bestille tester, for eksempel blodprøver, for å avgjøre om du trenger å ta Retacrit og vil vurdere den nøyaktige dosen av Retacrit, hvor lenge du trenger å gjennomgå behandlingen og hvordan medisinen vil bli gitt. Disse avgjørelsene vil avhenge av årsaken til anemi. Legen din vil bruke den laveste effektive dosen for å kontrollere symptomene på anemi. Hvis du ikke svarer tilstrekkelig på Retacrit, vil legen din sjekke dosen du får, og vil informere deg om han endrer den.
Du kan få jerntilskudd både før og under behandling med Retacrit, for større effektivitet av behandlingen.
Bruk hos pasienter med nyresykdom
Retacrit må administreres enten under huden (subkutant) eller ved injeksjon enten i en vene eller gjennom et kateter plassert i en vene.
Bruk av Retacrit hos voksne pasienter som får hemodialyse
Legen vil holde hemoglobinkonsentrasjonen mellom 10 og 12 g / dl (6,2 - 7,5 mmol / l).
Retacrit kan administreres under dialyseøkten eller på slutten av økten.
Den anbefalte startdosen er 50 IE / kg (internasjonale enheter per kilo), gitt 3 ganger per uke. Hvis løsningen administreres i en vene, skal den injiseres i løpet av 1 til 5 minutter.
Avhengig av hvordan din anemi reagerer på behandlingen, kan denne dosen justeres omtrent hver fjerde uke til situasjonen er under kontroll.Legen din vil foreskrive blodprøver som skal utføres regelmessig for å sikre at medisinen fortsetter å ha ønsket effekt. Når situasjonen er under kontroll, vil du fortsette å ta Retacrit i vanlige doser 2 eller 3 ganger per uke. Disse dosene er kanskje ikke så høye som de som opprinnelig ble mottatt.
Bruk av Retacrit hos barn og ungdom
(≤18 år) som behandles med hemodialyse Hos barn vil legen holde hemoglobinkonsentrasjonen mellom 9,5 og 11 g / dl.
Retacrit bør gis til pasienten på slutten av dialyseøkten.
Dosering for barn og ungdom er basert på kroppsvekt i kilo. Den anbefalte startdosen er 50 IE / kg, gitt 3 ganger i uken ved injeksjon i en vene (over en varighet på 1-5 minutter).
Avhengig av hvordan anemi reagerer på behandlingen, kan denne dosen justeres omtrent hver fjerde uke til situasjonen er under kontroll.Legen din vil bestille blodprøver med jevne mellomrom for å sikre at dette skjer.
Bruk av Retacrit hos voksne pasienter som gjennomgår peritonealdialyse
Legen vil holde hemoglobinkonsentrasjonen mellom 10 og 12 g / dl.
Den anbefalte startdosen er 50 IE / kg, som skal administreres to ganger i uken.
Avhengig av hvordan anemi reagerer på behandlingen, kan denne dosen justeres omtrent hver fjerde uke til situasjonen er under kontroll.
Legen din vil bestille blodprøver med jevne mellomrom for å sikre at medisinen fortsetter å ha ønsket effekt.
Bruk av Retacrit hos voksne pasienter med nyresykdom, men som ikke gjennomgår dialyse
Den anbefalte startdosen er 50 IE / kg, gitt 3 ganger per uke.
Denne startdosen kan justeres av legen din til situasjonen er under kontroll.Når situasjonen er under kontroll, vil du fortsette å ta Retacrit i vanlige doser (3 ganger i uken, eller hvis det gis under huden (subkutant) kan det også gis en gang i uken eller annenhver uke). Maksimal dose bør ikke overstige 150 IE / kg 3 ganger i uken, 240 IE / kg (opptil maksimalt 20.000 IE) en gang i uken, eller 480 IE / kg (opptil maksimalt 40.000 IE) en gang i uken. annenhver uke.
Legen din vil bestille blodprøver med jevne mellomrom for å sikre at medisinen fortsetter å ha ønsket effekt.
Hvis du blir behandlet med lengre doseintervaller (større enn en gang i uken), er det ikke sikkert du klarer å opprettholde Hb -nivået ditt tilstrekkelig, og du må kanskje øke dosen Retacrit eller administrasjonsfrekvensen.
Bruk av Retacrit hos voksne pasienter som får cellegift
Legen din kan starte Retacrit hvis hemoglobinnivået ditt er 10 g / dl eller mindre.
Etter behandlingsstart vil legen holde hemoglobinkonsentrasjonen mellom 10 og 12 g / dl.
Den anbefalte startdosen er 150 IE / kg, som skal administreres 3 ganger per uke ved subkutan injeksjon. Alternativt kan legen din anbefale en startdose på 450 IE / kg en gang i uken. Legen din kan justere startdosen din basert på din anemi -respons på behandlingen; du vil fortsette å ta Retacrit i 1 måned etter avsluttet cellegift.
Bruk hos voksne pasienter som deltar i et autologt predonasjonsprogram
Den anbefalte startdosen er 600 IE / kg, gitt to ganger i uken ved injeksjon i en vene. Retacrit vil bli gitt deg i 3 uker før operasjonen. Du vil også ta jerntilskudd før og under behandling med Retacrit for å øke effektiviteten av dette legemidlet.
Bruk hos voksne pasienter planlagt for større ortopedisk (bein) kirurgi
En dose på 600 IE / kg gis ved injeksjon under huden en gang i uken i 3 uker før operasjonen og på operasjonsdagen. I tilfeller der det er nødvendig å redusere tiden før intervensjonen, administreres en dose på 300 IE / kg i løpet av de ti dagene før intervensjonen, intervensjonsdagen og i de fire påfølgende dagene. Hvis blodprøvene før intervensjonen viser for høyt hemoglobinnivå, vil behandlingen bli stoppet.
Det er også viktig at jernnivået i blodet er normalt under behandlingen med Retacrit. Om nødvendig vil du motta jern gjennom munnen daglig, helst allerede før du starter behandling med Retacrit.
Informasjon om administrasjon
Den ferdigfylte sprøyten i Retacrit er klar til bruk. Hver sprøyte er kun til én injeksjon. Retacrit injeksjonsvæske, oppløsning bør ikke ristes eller blandes med andre oppløsninger.
Hvis Retacrit injiseres under huden, bør mengden som injiseres på et enkelt sted ikke overstige 1 ml. Øvre lår og mage vekk fra navlen er gode injeksjonssteder. Bytt injeksjonssted hver dag.
Når du bruker Retacrit, må du alltid følge disse instruksjonene:
- Ta den forseglede blisterpakningen som inneholder sprøyten og la den nå romtemperatur før du bruker den. For dette vil det ta 15 til 30 minutter.
- Fjern sprøyten fra blisterpakningen og kontroller at oppløsningen er klar, fargeløs og praktisk talt fri for synlige partikler.
- Fjern nåldekselet og la luften komme ut av nålen og sprøyten ved å holde sprøyten oppreist og skyve stempelet forsiktig opp.
- Injiser oppløsningen i henhold til instruksjonene legen din har gitt deg. Spør lege eller apotek hvis noe ikke er klart for deg.
Ikke bruk Retacrit hvis:
- blisteren er åpen eller på annen måte skadet;
- løsningen er ikke fargeløs eller inneholder synlige partikler i suspensjon;
- c "væske har lekket ut fra den ferdigfylte sprøyten eller kondens er synlig inne i blemmen som fortsatt er forseglet;
- du vet at medisinen ved et uhell har blitt frosset ned, eller du tror at dette kan ha skjedd.
Bytte fra intravenøs til subkutan administrasjon
Når situasjonen er under kontroll, vil du fortsette å ta Retacrit med vanlige doser. Legen din kan bestemme at Retacrit skal gis ved injeksjon under huden (subkutant) i stedet for i en vene (intravenøst).
Når du bytter fra den ene administrasjonsmåten til den andre, trenger ikke dosen endres.Legen din kan da bestille blodprøver for å sjekke om det er nødvendig med dosejustering.
Gi deg selv en injeksjon av Retacrit under huden
Ved starten av behandlingen gis Retacrit vanligvis av en lege eller sykepleier, og deretter kan legen foreslå at du eller din omsorgsperson lærer hvordan du injiserer under huden (subkutan).
- Ikke prøv å injisere deg selv hvis legen din eller sykepleieren ikke har fortalt deg hvordan.
- Bruk alltid Retacrit som beskrevet av legen din eller sykepleier.
- Bruk bare medisinen hvis den er lagret riktig (se avsnitt 5).
- Før bruk, fjern sprøyten fra kjøleskapet og la den nå romtemperatur. Det tar vanligvis 15-30 minutter.
Bruk en enkelt dose Retacrit fra hver sprøyte.
Når medisinen administreres under huden (subkutant), er volumet normalt ikke mer enn 1 ml for hver enkelt injeksjon.
Retacrit må administreres alene og ikke blandes med andre injeksjonsvæsker.
Ikke rist de ferdigfylte sprøyter. Langvarig og kraftig risting kan skade medisinen. Ikke bruk medisinen hvis den har blitt rystet kraftig.
Hvordan injisere deg selv med de ferdigfylte sprøyter
- Fjern sprøyten fra kjøleskapet. Væsken må nå romtemperatur. Ikke fjern sprøytenålens deksel når det når romtemperatur.
- Kontroller sprøyten for å kontrollere at den er riktig dose, at den ikke har gått ut, at den ikke er skadet og at væsken er klar og ikke frossen
- Velg injeksjonsstedet. De mest egnede injeksjonsstedene er øvre lår og mage, bortsett fra området rundt navlen. Bytt injeksjonssted hver gang.
- Vask hendene. Bruk en antiseptisk tørk for å desinfisere injeksjonsstedet.
- Hold sprøyten i kroppen med nålen dekket opp.
- Ikke hold sprøyten i stempelhodet, stemplet eller nåledekselet.
- Trekk aldri stempelet mot deg.
- Ikke fjern kanylehetten på den ferdigfylte sprøyten før du er klar til å injisere Retacrit.
- Fjern lokket fra sprøyten ved å holde fatet og trekke forsiktig i lokket uten å vri det. Ikke skyv stempelet, berør nålen eller rist sprøyten.
- Ta en hudfold mellom tommelen og pekefingeren uten å klemme den for mye.
- Skyv nålen helt inn. Legen din eller sykepleieren vil ha vist deg hvordan.
- Skyv stempelet med tommelen helt inn for å injisere hele mengden væske. Skyv det sakte og jevnt, og hold huden klemt.
- Når stempelet presses til grensen, trekker du ut nålen og slipper huden.
- Når nålen fjernes fra huden, kan det lekke noe blod fra injeksjonsstedet. Dette er normalt. Du kan desinfisere injeksjonsstedet ved å trykke på den antiseptiske tørken i noen sekunder etter injeksjonen.
- Legg den brukte sprøyten i en beholder for skarpe gjenstander. Ikke prøv å sette beskyttelseshetten tilbake på nålen.
- Kast aldri brukte sprøyter i husholdningsavfallsbeholdere.
Bruk av nålbeskyttelsesenheten
Den ferdigfylte sprøyten kan utstyres med en sikkerhetsinnretning for nålen som beskytter mot utilsiktet nålestift.
- Utfør injeksjonen i henhold til teknikken beskrevet ovenfor.
- Mens du holder sprøyten med fingrene hvilende på støttekanten, må du trykke på stempelet til injeksjonen av hele dosen er fullført. Nålbeskyttelsessystemet vil IKKE aktiveres hvis FULL dose ikke er administrert.
- Fjern nålen fra huden din, slipp deretter stempelet og sprøyten vil bevege seg fremover til skjoldet dekker nålen og klikker på plass.
Dersom du har glemt å bruke Retacrit
Ikke bruk en dobbel dose for å gjøre opp for en glemt tidligere dose.
Dersom du slutter å ta Retacrit
Ikke avslutt behandlingen uten først å sjekke med legen din.
Spør legen din hvis du har ytterligere spørsmål om bruk av Retacrit.
Overdosering Hva du skal gjøre hvis du har tatt for mye Retacrit
Retacrit har en stor sikkerhetsmargin, og det er usannsynlig at bivirkninger fra overdosering av dette legemidlet vil forekomme. Fortell legen din eller sykepleieren umiddelbart hvis du tror du har for mye injisert Retacrit.
Bivirkninger Hva er bivirkningene av Retacrit
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Fortell legen din umiddelbart hvis du har hodepine, spesielt hvis det er plutselig, skarp, migrenelignende hodepine, hvis du føler deg forvirret eller hvis du har anfall. Disse symptomene kan være advarselstegn på en plutselig økning. Blodtrykk, som krever nødstilfelle behandling.
Fortell legen din eller sykepleier hvis du merker noen av effektene på denne listen.
Svært vanlige bivirkninger
Disse kan påvirke mer enn 1 av 10 personer behandlet med Retacrit.
- Influensalignende symptomer, hodepine, leddsmerter, følelse av svakhet, tretthet og svimmelhet.
- Hos pasienter med nyresykdom som ennå ikke er under dialyse, er det rapportert overbelastning i luftveiene, som tett nese og ondt i halsen.
Vanlige bivirkninger
Disse kan ramme opptil 1 av 10 personer behandlet med Retacrit.
- Økt blodtrykk. Økningen i blodtrykket kan kreve behandling med medisiner (eller justering av medisinene du allerede behandles for høyt blodtrykk). Legen din vil kontrollere blodtrykket ditt med jevne mellomrom under behandling med Retacrit, spesielt under behandling med Retacrit. " start av terapi.
- Brystsmerter, kortpustethet, smertefull hevelse i beina som kan være et symptom på blodpropp (lungeemboli, dyp venetrombose).
- Hjerneslag (utilstrekkelig blodtilførsel til hjernen, som kan forårsake manglende evne til å bevege en eller flere lemmer på den ene siden av kroppen, manglende evne til å forstå eller snakke, eller manglende evne til å se den ene siden av synsfeltet).
- Utslett og hevelse rundt øynene (ødem), som kan være forårsaket av en allergisk reaksjon.
- Koagulasjon i den kunstige nyren.
Uvanlige bivirkninger
Disse kan ramme opptil 1 av 100 personer som behandles med Retacrit.
- Hjerneblødning.
Sjeldne bivirkninger
Disse kan ramme opptil 1 av 1 000 personer som behandles med Retacrit.
- Overfølsomhetsreaksjoner.
Svært sjeldne bivirkninger
Disse kan ramme opptil 1 av 10 000 personer som behandles med Retacrit.
- Det kan være økninger i blodplatene, som normalt er involvert i dannelsen av blodpropper. Legen vil sjekke disse verdiene.
Bivirkninger med frekvens ikke kjent
Hyppigheten av disse bivirkningene kan ikke beregnes ut fra tilgjengelige data.
- Hevelse, spesielt i øye- og leppeområdet (Quinckes ødem) og sjokklignende allergiske reaksjoner med symptomer som prikking, rødhet, kløe, rødme og rask puls.
- Vaskulære og trombotiske hendelser (blodpropper) i blodkar som hindret blodtilførsel til hjernen, retinal trombose, hindret blodtilførsel til hjertet, hjerteinfarkt, arteriell trombose, utvidelse av blodkarvegger (aneurisme).
- Red Series Aplasia (PRCA) PRCA har blitt rapportert hos pasienter etter måneder til år med subkutan (injeksjon under huden) behandling av erytropoietin. PRCA betyr manglende evne til å produsere et tilstrekkelig antall røde blodlegemer i beinmargen (se avsnittet "Advarsler og forsiktighetsregler").
- Kløe.
Andre bivirkninger
Pasienter med nyresykdom
- Økning i blodtrykk, som kan kreve legemiddelbehandling eller justering av doseringen av medisiner du allerede tar for høyt blodtrykk. Legen din kan måle blodtrykket ditt regelmessig mens du bruker Retacrit, spesielt ved starten av behandlingen.
- En okklusjon av forbindelsen mellom arterie og vene (shunttrombose) kan oppstå spesielt hvis du har lavt blodtrykk eller hvis du har komplikasjoner av arteriovenøs fistel.Legen din vil kunne kontrollere shunten og foreskrive medisin for å forhindre trombose.
Pasienter med ondartede svulster
- Blodpropp (vaskulære trombotiske hendelser) (se avsnittet "Advarsler og forsiktighetsregler").
- Økt blodtrykk. Av denne grunn bør hemoglobinnivåer og blodtrykk overvåkes.
Fortell legen din, apoteket eller sykepleieren hvis du opplever noen bivirkninger. Dette gjelder også bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Rapportering av bivirkninger
Snakk med legen din dersom du får bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også rapportere bivirkninger direkte via det nasjonale rapporteringssystemet som er oppført i vedlegg V. Ved å rapportere bivirkninger kan du hjelpe til med å gi mer informasjon om sikkerheten til dette legemidlet.
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Ikke bruk dette legemidlet etter utløpsdatoen som er angitt på etiketten og esken ("EXP" / "EXP").
Utløpsdatoen refererer til den siste dagen i måneden.
Oppbevares i kjøleskap (2 ° C - 8 ° C). Ikke frys.
Sprøyten kan fjernes fra kjøleskapet og stå ved romtemperatur i en enkelt periode på opptil 3 dager (men ikke over 25 ° C).
Oppbevar den ferdigfylte sprøyten i ytteremballasjen for å beskytte medisinen mot lys.
Ikke kast medisiner via avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Deadline "> Annen informasjon
Sammensetning av Retacrit
Den aktive ingrediensen er epoetin zeta (produsert ved rekombinant DNA -teknikk i ovariecellelinjer fra kinesisk hamster).
Retacrit 1 000 IE / 0,3 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,3 ml injeksjonsvæske, oppløsning inneholder 1000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 3333 IE epoetin zeta per ml.
Retacrit 2000 IE / 0,6 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,6 ml injeksjonsvæske, oppløsning inneholder 2000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 3333 IE epoetin zeta per ml.
Retacrit 3000 IE / 0,9 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,9 ml injeksjonsvæske, oppløsning inneholder 3000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 3333 IE epoetin zeta per ml.
Retacrit 4000 IE / 0,4 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,4 ml injeksjonsvæske, oppløsning inneholder 4000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 10 000 IE epoetin zeta per ml.
Retacrit 5000 IE / 0,5 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,5 ml injeksjonsvæske, oppløsning inneholder 5000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 10 000 IE epoetin zeta per ml.
Retacrit 6000 IE / 0,6 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,6 ml injeksjonsvæske, oppløsning inneholder 6000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 10 000 IE epoetin zeta per ml.
Retacrit 8 000 IE / 0,8 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,8 ml injeksjonsvæske, oppløsning inneholder 8000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 10 000 IE epoetin zeta per ml.
Retacrit 10 000 IE / 1 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 1,0 ml injeksjonsvæske, oppløsning inneholder 10 000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 10 000 IE epoetin zeta per ml.
Retacrit 20 000 IE / 0,5 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,5 ml injeksjonsvæske, oppløsning inneholder 20 000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 40 000 IE epoetin zeta per ml.
Retacrit 30 000 IE / 0,75 ml injeksjonsvæske, oppløsning i en ferdigfylt sprøyte
1 ferdigfylt sprøyte med 0,75 ml injeksjonsvæske, oppløsning inneholder 30 000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 40 000 IE epoetin zeta per ml.
Retacrit 40 000 IE / 1 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte
1 ferdigfylt sprøyte med 1,0 ml injeksjonsvæske, oppløsning inneholder 40 000 internasjonale enheter (IE) epoetin zeta (rekombinant humant erytropoietin). Løsningen inneholder 40 000 IE epoetin zeta per ml. Andre innholdsstoffer er dinatriumfosfatdihydrat, monobasisk natriumfosfatdihydrat, natriumklorid, kalsiumkloriddihydrat, polysorbat 20, glycin, leucin, isoleucin, treonin, glutaminsyre, fenylalanin og vann til injeksjonsvæsker, natriumhydroksid (for justering av pH), saltsyre (for å justere pH).
Hvordan Retacrit ser ut og innholdet i pakningen
Retacrit er en klar og fargeløs injeksjonsvæske, oppløsning i klare, fargeløse glasssprøyter med en fast nål.
De ferdigfylte sprøyter inneholder 0,3 ml til 1 ml oppløsning, avhengig av innholdet i epoetin zeta (se avsnitt "Retacrit inneholder").
En pakke inneholder 1 eller 4 eller 6 ferdigfylte sprøyter med eller uten nålebeskytter.
Multipakker inneholder 4 (4 pakninger med 1) eller 6 (6 pakninger med 1) ferdigfylte sprøyter.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN -
RETACRIT 1000 IE / 0,3 ML LØSNING FOR INJEKSJON I FORFYLDT SPRØYTE
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING -
En ferdigfylt sprøyte med 0,3 ml injeksjonsvæske, oppløsning inneholder 1000 internasjonale enheter (IE) epoetin zeta * (rekombinant humant erytropoietin). Løsningen inneholder 3333 IE epoetin zeta per ml.
* Produsert ved rekombinant DNA -teknikk i cellelinjer fra kinesisk hamster eggstokk (CHO).
Hjelpestoff med kjent effekt:
Hver ferdigfylte sprøyte inneholder 0,15 mg fenylalanin.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM -
Injeksjonsvæske, oppløsning i ferdigfylt sprøyte.
Klar og fargeløs løsning.
04.0 KLINISK INFORMASJON -
04.1 Terapeutiske indikasjoner -
• Behandling av symptomatisk anemi assosiert med kronisk nyresvikt (CRI) hos voksne og barn:
• Behandling av anemi assosiert med kronisk nyresvikt hos voksne og pediatriske pasienter på hemodialyse og hos voksne pasienter på peritonealdialyse (se pkt. 4.4).
• Behandling av alvorlig anemi av nyreopprinnelse med kliniske symptomer hos voksne pasienter med nyreinsuffisiens som ennå ikke er under dialyse (se pkt. 4.4).
- Behandling av anemi og reduksjon av transfusjonskrav hos voksne pasienter som gjennomgår cellegiftbehandling for solide svulster, malignt lymfom eller myelomatose og med risiko for blodtransfusjon som indikert av pasientens generelle tilstand (kardiovaskulær situasjon, anemi som allerede eksisterer ved starten av cellegift) .
- Retacrit kan brukes til å øke mengden autologt blod hos pasienter som er en del av et predonasjonsprogram. Bruk i denne indikasjonen bør evalueres i lys av de rapporterte risikoene for tromboemboliske hendelser.Behandling bør bare forbeholdes pasienter med moderat anemi (i mangel av jernmangel) hvis blodbevaringsprosedyrer ikke er tilgjengelige eller utilstrekkelige når den planlagte større valgfrie operasjonen krever et stort volum blod (4 eller flere enheter blod for kvinner, 5 eller flere enheter for menn).
-Retacrit kan brukes for å redusere eksponeringen for allogene blodtransfusjoner hos ikke -jernmangel voksne pasienter som antas å ha høy risiko for transfusjonskomplikasjoner før større elektiv ortopedisk kirurgi Begrens bruk for pasienter med moderat anemi (Hb 10-13 g / dl ) er ikke en del av et autologt predonasjonsprogram og som forventes moderat blodtap (fra 900 til 1 800 ml).
04.2 Dosering og administrasjonsmåte -
Retakritbehandling bør startes under oppsyn av medisinsk personell med erfaring i behandling av pasienter med indikasjonene beskrevet ovenfor.
Dosering
Behandling av symptomatisk anemi hos voksne og barn med kronisk nyresvikt
Retacrit bør administreres enten subkutant eller intravenøst.
Ønsket hemoglobinkonsentrasjon er mellom 10 og 12 g / dl (6,2-7,5 mmol / l), unntatt hos barn, der hemoglobinkonsentrasjonen må være mellom 9,5 og 11 g / dl (5,9-6,8 mmol / l). Den øvre grensen for mål hemoglobinkonsentrasjon bør ikke overskrides. Symptomer og følger av anemi kan variere med alder, kjønn og generell sykdomsbyrde; det er nødvendig at det kliniske forløpet og tilstanden til den enkelte pasient blir evaluert av legen. Retacrit bør administreres enten subkutant eller intravenøst for å oppnå hemoglobinverdier som ikke overstiger 12 g / dl (7,5 mmol / l). På grunn av variasjon i pasienten kan enkelte hemoglobinverdier over og under ønsket hemoglobinkonsentrasjon av og til observeres hos en pasient. Variasjon i hemoglobin bør håndteres gjennom dosejustering, med henvisning til et målhemoglobinområde mellom 10 g / dl (6,2 mmol / l) og 12 g / dl (7,5 mmol / l).
Et forlenget hemoglobinnivå over 12 g / dl (7,5 mmol / l) bør unngås; instruksjoner for passende dosejustering for når hemoglobinverdier over 12 g / dl (7,5 mmol / l) observeres er gitt nedenfor. En økning i hemoglobin på mer enn 2 g / dl (1,25 mmol / l) over en fire ukers periode bør unngås. Hvis dette skjer, bør passende dosering justeres som angitt.
Pasienter bør overvåkes nøye for å sikre at den laveste autoriserte effektive dosen Retacrit brukes til å kontrollere symptomene på anemi tilstrekkelig ved å opprettholde en hemoglobinkonsentrasjon på mindre enn eller lik 12 g / dl (7,5 mmol / l).
Forsiktighet bør utvises ved å øke dosene Retacrit hos pasienter med kronisk nyresvikt Hos pasienter med dårlig hemoglobinrespons på Retacrit bør alternative forklaringer på denne dårlige responsen vurderes (se pkt. 4.4 og 5.1) Hos pasienter med utilstrekkelig kronisk nyresykdom. og kliniske tegn på iskemisk hjertesykdom eller kongestiv hjertesvikt, bør vedlikeholdshemoglobinkonsentrasjonen ikke overskride maksimal målkonsentrasjonsgrense.
Voksne pasienter på hemodialyse
Retacrit bør administreres enten subkutant eller intravenøst.
Behandlingen er delt inn i to faser:
1. Korrigeringsfase: 50 IE / kg, 3 ganger i uken. Hvis dosejustering er nødvendig, bør dette gjøres gradvis, med intervaller på minst 4 uker. For hver justering bør dosen økes eller reduseres med 25 IE / kg, 3 ganger per uke.
2. Vedlikeholdsfase: Dosejustering rettet mot å opprettholde ønsket nivå av hemoglobin (Hb), mellom 10 og 12 g / dl (6,2-7,5 mmol / l). Den anbefalte totale ukedosen varierer fra 75 til 300 IE / kg.
Tilgjengelige kliniske data indikerer at pasienter med et veldig lavt hemoglobinnivå (8 g / dl eller> 5 mmol / l).
Pediatriske pasienter på hemodialyse
Behandlingen er delt inn i to faser.
1. Korrigeringsfase 50 IE / kg, 3 ganger per uke intravenøst. Hvis dosejustering er nødvendig, bør dette gjøres i trinn på 25 IE / kg 3 ganger per uke, med intervaller på minst 4 uker, til målet er nådd.
2. Vedlikeholdsfase Dosejustering tar sikte på å opprettholde ønsket nivå av hemoglobin (Hb), mellom 9,5 og 11 g / dl (5,9-6,8 mmol / l).
Vanligvis krever barn og ungdom som veier mindre enn 30 kg høyere vedlikeholdsdoser enn barn som veier mer enn 30 kg og voksne. I kliniske studier ble for eksempel følgende vedlikeholdsdoser observert etter 6 måneders behandling:
Tilgjengelige kliniske data indikerer at pasienter med et meget lavt innledende hemoglobinnivå (6,8 g / dl eller> 4,25 mmol / l).
Voksne pasienter på peritonealdialyse
Retacrit bør administreres enten subkutant eller intravenøst.
Behandlingen er delt inn i to faser.
1. Korrigeringsfase: Startdosen er 50 IE / kg vekt, to ganger i uken.
2. Vedlikeholdsfase: Dosejustering rettet mot å opprettholde ønsket nivå av hemoglobin (Hb), (mellom 10 og 12 g / dl [6,2-7,5 mmol / l]. Vedlikeholdsdosen er mellom 25 og 50 IE / kg 2 ganger pr. uke, delt inn i 2 like store doser.
Voksne pasienter med nedsatt nyrefunksjon som ennå ikke er i dialyse
Retacrit bør administreres enten subkutant eller intravenøst.
Behandlingen er delt inn i to faser.
1. Korrigeringsfase: En startdose på 50 IE / kg 3 ganger per uke, etterfulgt om nødvendig av en økning i trinn på 25 IE / kg (3 ganger per uke) til ønsket mål er nådd (økningen bør skje gradvis, med minst fire ukers mellomrom).
2. Vedlikeholdsfase: Under vedlikeholdsfasen kan Retacrit administreres 3 ganger per uke, og ved subkutan administrasjon en gang i uken eller en gang annenhver uke. Dose- og doseringsintervallene må justeres riktig for å opprettholde ønsket hemoglobinnivå (Hb), (mellom 10 og 12 g / dl [6,2-7,5 mmol / l].
Forlengelse av doseringsintervallet kan kreve en doseøkning.
Maksimal dose bør ikke overstige 150 IE / kg 3 ganger i uken, 240 IE / kg (opptil maksimalt 20.000 IE) en gang i uken eller 480 IE / kg (opptil maksimalt 40.000 IE) en gang i uken. 2 uker.
Behandling av pasienter med kjemoterapi-indusert anemi
Retacrit bør administreres subkutant til anemiske pasienter (f.eks. Med hemoglobinkonsentrasjon ≤ 10 g / dl (6,2 mmol / l). Symptomene og konsekvensene av anemi kan variere avhengig av alder, kjønn og alvorlighetsgrad. Generell sykdom; en individuell vurdering av det kliniske forløp og tilstand for hver enkelt pasient kreves av legen.
På grunn av variasjonen mellom pasientene kan enkelte hemoglobinverdier over og under ønsket hemoglobinnivå av og til påvises hos en pasient. Variasjon i hemoglobin bør håndteres gjennom dosejustering i forhold til et målhemoglobinområde på 10 g / dl (6,2 mmol / l) til 12 g / dl (7,5 mmol / l). Et forlenget hemoglobinnivå over 12 g / dl (7,5 mmol / l) bør unngås; instruksjoner for passende dosejustering for når hemoglobinverdier over 12 g / dl (7,5 mmol / l) observeres er gitt nedenfor.
Pasienter bør overvåkes nøye for å sikre at den laveste autoriserte dosen Retacrit brukes for å kontrollere symptomene på anemi tilstrekkelig.
Retakritterapi bør fortsette i ytterligere en måned etter avsluttet cellegift. Startdosen er 150 IE / kg, 3 ganger per uke subkutant. Alternativt kan Retacrit administreres subkutant i en startdose på 450 IE / kg en gang i uken. Hvis hemoglobinet etter 4 ukers behandling har økt med minst 1 g / dL (0,62 mmol / L) eller retikulocyttallet har økt med ≥ 40 000 celler / μl fra baseline, bør dosen forbli på 450 IE / kg en gang i uken eller 150 IE / kg 3 ganger i uken. Hvis hemoglobinøkningen er
Det anbefalte doseringsregimet er vist i tabellen nedenfor:
Når det terapeutiske målet for den enkelte pasient er nådd, bør dosen reduseres med 25 til 50% for å opprettholde hemoglobin på dette nivået. Riktig dosetitrering bør vurderes.
Dosejustering
Hvis økningen i hemoglobin er større enn 2 g / dl (> 1,25 mmol / l) per måned, bør dosen Retacrit reduseres med omtrent 25-50%. Hvis hemoglobinverdien overstiger 12 g / dl (7,5 mmol / L ), avslutt behandlingen til den går tilbake til eller faller under 12 g / dL (7,5 mmol / L), og fortsett deretter Retacrit -behandlingen med en 25% lavere dose enn den forrige dosen.
Behandling av voksne pasienter som er kandidater til kirurgiske inngrep som inngår i autologe predonasjonsprogrammer
Retacrit må administreres intravenøst.
På tidspunktet for bloddonasjon må Retacrit administreres etter at donasjonsprosedyren er fullført.
Mildt anemiske pasienter (hematokrit 33-39%) som krever et depot på ≥ 4 enheter blod bør behandles med 600 IE / kg Retacrit 2 ganger per uke i 3 uker før operasjonen.
Gjennom hele behandlingen med Retacrit bør alle pasienter få tilstrekkelig jerntilskudd (f.eks. 200 mg daglig oralt elementært jern). Administrering av jern bør startes så snart som mulig, selv flere uker før du utfører det autologe depotet, for å øke jernlagrene før du starter behandling med Retacrit.
Behandling av voksne pasienter planlagt for større elektiv ortopedisk kirurgi
Retacrit bør administreres subkutant.
En dose på 600 IE / kg kroppsvekt bør gis en gang i uken i tre uker (dag 21, 14 og 7) før operasjonen og på operasjonsdagen (dag 0). I tilfeller der det er nødvendig å redusere tiden før operasjonen til mindre enn tre uker, bør en daglig dose på 300 IE / kg kroppsvekt administreres i 10 påfølgende dager før operasjonen, på operasjonsdagen og i de fire dagene umiddelbart følgende.Hvis hemoglobinnivået når eller overstiger 15 g / dl som en del av hematologiske tester utført i den preoperative perioden, bør Retacrit seponeres og påfølgende doser bør ikke administreres.
Jernmangel må behandles før behandling med Retacrit startes. I tillegg bør en tilstrekkelig mengde jern gis til alle pasienter behandlet med Retacrit (f.eks. 200 mg jernioner oralt per dag) for hele behandlingsvarigheten med Retacrit. Jernadministrasjon før Retacrit -terapi for å oppnå tilstrekkelige avleiringer.
Administrasjonsmåte
Intravenøs injeksjon
Administrasjonen bør ta minst 1-5 minutter, avhengig av den totale dosen. Hos pasienter med hemodialyse er det mulig å administrere bolusdosen under dialysesessionen fra en passende venøs tilgang til dialysekretsen. Alternativt kan stoffet injiseres på slutten av dialysesessionen gjennom fistelen og etterfulgt av 10 ml 9 mg / ml (0,9%) NaCl fysiologisk løsning for å vanne kretsen og sikre en tilfredsstillende introduksjon av produktet i sirkulasjonen. Hos pasienter som reagerer på behandling med influensalignende symptomer, er det å foretrekke en tregere administrasjon.
Retacrit må ikke administreres som intravenøs infusjon.
Retacrit må ikke blandes med andre legemidler (se pkt. 6.2).
Subkutan injeksjon
Generelt bør maksimalt volum på 1 ml per injeksjonssted ikke overskrides.Ved større volumer er det nødvendig å velge flere administrasjonssteder.
Injeksjoner gis i lemmer eller i den fremre bukveggen.
For instruksjoner om håndtering av legemidlet før administrering, se pkt. 6.6.
04.3 Kontraindikasjoner -
- Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene listet opp i pkt.6.1.
- Pasienter med ren rødcelleaplasi (PRCA) etter behandling med erytropoietin bør ikke gjennomgå behandling med Retacrit eller andre typer erytropoietin (se pkt. 4.4).
- Ukontrollert hypertensjon.
- I indikasjonen "økning i mengden autologt blod": hjerteinfarkt eller hjerneslag i måneden før behandling, ustabil angina pectoris, økt risiko for dyp venetrombose, for eksempel historie med venøs tromboembolisk sykdom.
- Ved indikasjon på større elektiv ortopedisk kirurgi: alvorlig koronar, perifer arteriell, carotis eller cerebral vaskulær sykdom, inkludert pasienter med nylig hjerteinfarkt eller cerebrovaskulær ulykke.
- Pasienter som av en eller annen grunn ikke kan få "tilstrekkelig antitrombotisk profylakse.
04.4 Spesielle advarsler og passende forholdsregler for bruk -
Generell informasjon
Som hos alle pasienter som får erytropoietin, kan det oppstå en økning i blodtrykket under behandling med Retacrit. Blodtrykket bør overvåkes nøye og tilstrekkelig kontrolleres før, ved oppstart og under behandling med Retacrit, både hos alle pasienter som behandles med epoetin for første gang og hos pasienter som allerede er behandlet. Det kan være nødvendig å etablere eller styrke -hypertensiv behandling Hvis blodtrykket ikke kan kontrolleres, bør behandling med Retacrit stoppes.
Retacrit bør også brukes med forsiktighet i nærvær av epilepsi og kronisk leversvikt.
En moderat doseavhengig økning i antall blodplater innenfor det normale området kan oppstå under behandling med erytropoietin. Dette fenomenet går tilbake med fortsettelsen av terapien. Det anbefales at antall blodplater kontrolleres regelmessig i løpet av de første 8 ukene av behandlingen.
Alle andre årsaker til anemi (jernmangel, hemolyse, blodtap, vitamin B12 eller folatmangel) bør evalueres og behandles før og under behandling med Retacrit. I de fleste tilfeller reduseres serumferritinverdiene samtidig som hematokritverdiene øker.For å sikre optimal respons på erytropoietin må tilstrekkelige jernlagre sikres:
-hos pasienter med kronisk nyresvikt og serumferritinnivåer under 100 ng / ml jerntilskudd anbefales, for eksempel 200-300 mg / dag oralt (100-200 mg / dag hos pediatriske pasienter);
- Hos alle kreftpasienter med transferrinmetningsverdier under 20%anbefales et muntlig jerntilskudd på 200-300 mg / dag.
Alle disse faktorene som bidrar til utbruddet av anemi må også vurderes nøye før du bestemmer deg for å øke erytropoietindosen hos kreftpasienter.
En paradoksal nedgang i hemoglobin og utvikling av alvorlig anemi assosiert med lave retikulocyttall bør varsle dem om å avbryte behandling med epoetin og utføre antireytropoietin-antistofftester. Tilfeller er rapportert hos pasienter med hepatitt C behandlet med interferon og ribavirin, når epoetiner. har blitt brukt i kombinasjon. Epoetiner er ikke godkjent for behandling av anemi assosiert med hepatitt C.
For å forbedre sporbarheten til erytropoiesis stimulerende midler (Erythropiesis stimulerende midler (ESA), må navnet på ESA som er foreskrevet, være tydelig registrert (eller angitt) i pasientens journal.
God prosedyre for blodbehandling bør alltid brukes i operasjonen.
Pasienter planlagt for større valgfri ortopedisk kirurgi
Hos pasienter som er planlagt for større elektiv ortopedisk kirurgi, bør årsakene til anemi fastslås og behandles, muligens før behandling med Retacrit startes. Trombotiske hendelser kan utgjøre en risiko for denne pasientpopulasjonen, og dette bør vurderes nøye i forhold til den forventede nytten av behandlingen. Pasienter bør få "tilstrekkelig antitrombotisk profylakse, da trombotiske og vaskulære hendelser kan forekomme hos kirurgiske pasienter, spesielt hos pasienter med underliggende kardiovaskulær sykdom. I tillegg bør det utvises spesiell forsiktighet hos pasienter som er disponert for å utvikle dyp venetrombose (DVT). Videre i pasienter med baseline hemoglobin> 13 g / dl, muligheten for at Retacrit -behandling kan være forbundet med en økt risiko for postoperative trombotiske / vaskulære hendelser, kan derfor ikke brukes til pasienter med baseline hemoglobin> 13 g / dl .
Pasienter med kronisk nyresvikt
Hemoglobinkonsentrasjon
Hos pasienter med kronisk nyresvikt bør vedlikeholdshemoglobinkonsentrasjonen ikke overskride den øvre grensen for målhemoglobinkonsentrasjonen anbefalt i pkt.4.2. Økt dødsrisiko, alvorlige kardiovaskulære hendelser og cerebrovaskulære hendelser inkludert hjerneslag har blitt observert i kliniske studier da ESA ble administrert for å oppnå hemoglobinverdier større enn 12 g / dl (7,5 mmol / l).
Kontrollerte kliniske studier har ikke vist noen signifikant fordel ved administrering av epoetiner når hemoglobinkonsentrasjonen har overskredet nivåene som er nødvendige for å kontrollere symptomene på anemi og unngå blodtransfusjon.
Hemoglobinnivået bør måles med jevne mellomrom til det når en konstant verdi, og deretter med jevne mellomrom. Økningen i hemoglobin bør være omtrent 1 g / dl (0,62 mmol / l) per måned og bør ikke overstige 2 g / dl (1,25 mmol / l) per måned for å minimere risikoen for å utvikle hypertensjon eller forverring.
Pasienter med kronisk nyresvikt som behandles med Retacrit subkutant, bør monitoreres periodisk for tap av effekt, definert som ikke-respons eller redusert respons på Retacrit-behandling hos pasienter som tidligere har svart på slik behandling. Dette er preget av et vedvarende fall i hemoglobin til tross for en økning i dosen av Retacrit.
Noen pasienter behandlet med epoetin alfa med lengre doseringsintervaller (større enn én gang i uken) kan ikke opprettholde tilstrekkelige hemoglobinnivåer (se pkt.5.1) og kan kreve doseøkning. Hemoglobinnivået bør overvåkes regelmessig.
Det bør utvises forsiktighet ved økende doser Retacrit hos pasienter med kronisk nyresvikt, da høye kumulative doser epoetin kan være forbundet med økt risiko for dødelighet og alvorlige kardiovaskulære og cerebrovaskulære hendelser.Pasienter med dårlig hemoglobinrespons på epoetiner, Alternative forklaringer på dette dårlig respons bør vurderes (se pkt. 4.4 og 5.1).
Mangel på respons på erytropoietinbehandling må umiddelbart undersøke de ansvarlige faktorene. Disse inkluderer: jern-, folat- eller vitamin B12 -mangel, aluminiumforgiftning, mellomliggende infeksjoner, inflammatoriske eller traumatiske episoder, okkult blodtap, hemolyse, beinmargsfibrose av enhver opprinnelse.
Tilfeller av antistoff-mediert PRCA er svært sjelden rapportert hos pasienter med kronisk nyresvikt administrert subkutant erytropoietin. Hos pasienter som viser et "plutselig tap av effekt, demonstrert av en reduksjon i hemoglobin (1-2 g / dl per måned) med et økt behov for transfusjoner, bør det utføres et retikulocyttall og typiske årsaker til å forhindre respons på behandling (f.eks. jern-, folat- eller vitamin B12 -mangel, aluminiumforgiftning, infeksjon eller betennelse, blodtap, hemolyse). Hvis det ikke er funnet noen årsak, bør det vurderes å utføre en blodprøve beinmarg for å diagnostisere en PRCA.
Hvis PRCA er diagnostisert, bør Retacrit-behandlingen avbrytes umiddelbart, og en test for tilstedeværelse av anti-erytropoietin-antistoffer bør vurderes. Pasienter bør ikke omdirigeres til behandling med et annet legemiddel, gitt kryssreaktivitet mellom anti-erytropoietin-antistoffer og andre erytropoietiner Andre årsaker til PRCA må utelukkes og passende terapi iverksettes.
Periodisk overvåking av retikulocyttallet anbefales for å oppdage tap av terapeutisk effekt hos pasienter med kronisk nyresvikt.
Hyperkalemi er observert i isolerte tilfeller. Hos pasienter med kronisk nyresvikt kan korreksjon av anemi føre til økt appetitt og absorpsjon av kalium og protein. Foreskrevne parametere for dialyse kan trenge periodisk justering for å holde urea, kreatinin og kalium innenfor ønskede verdier. Hos pasienter med kronisk nyresviktsserum elektrolytter bør overvåkes. Hvis det observeres forhøyede (eller stigende) serumkaliumverdier, bør det vurderes å avbryte administrasjonen av erytropoietin til hyperkalemi er korrigert.
En økning i heparindosen er ofte nødvendig under behandling med erytropoietin på grunn av en økning i hematokritverdien. Okklusjon av dialysesystemet kan oppstå hvis heparinisering ikke er optimal.
Basert på dataene som er tilgjengelige hittil, akselererer ikke korreksjon av anemi med erytropoietin hos voksne pasienter med nyreinsuffisiens som ennå ikke er under dialyse, utviklingen av nyreinsuffisiens.
Voksne kreftpasienter med symptomatisk anemi ved cellegift
Hos kreftpasienter som får cellegift, bør intervallet på 2-3 uker mellom administrasjon og utseende av erytropoietininduserte erytrocytter vurderes ved vurdering av hensiktsmessigheten av Retacrit-behandling (pasienter med risiko for transfusjon). Hos kreftpasienter som gjennomgår cellegift, hvis hemoglobinet øker mer enn 2 g / dl (1,25 mmol / l) per måned, eller hvis nivået overstiger 12 g / dl (7,5 mmol / l), er det Dosejusteringsprosedyren angitt i avsnitt 4.2 må utføres nøye for å redusere potensialet risikofaktorer for trombotiske hendelser (se pkt.4.2).
Siden det er observert økt forekomst av tromboemboliske hendelser hos kreftpasienter som gjennomgår behandling med erytropoietiske midler (se pkt.4.8), bør denne risikoen veies nøye i lys av fordelene med behandling (med Retacrit), spesielt hos kreftpasienter som presenterer en økt tromboembolisk risiko, for eksempel overvektige personer eller med en historie med trombotiske og vaskulære hendelser (dyp venetrombose, lungeemboli).
Voksne pasienter som er kandidater til kirurgi som er en del av et autologt predonasjonsprogram
Alle advarsler og spesielle forholdsregler knyttet til autologe predonasjonsprogrammer må overholdes, spesielt ved å gjenopprette blodmengden som vanlig.
Onkogent potensial
Epoetiner er vekstfaktorer som først og fremst stimulerer produksjonen av erytrocytter. Erytropoietinreseptorer kan uttrykkes på overflaten av en rekke neoplastiske celler. Som med alle vekstfaktorer er det tvil om at epoetiner kan stimulere veksten av alle ondartede svulster.I flere kontrollerte kliniske studier har dette ikke vært Epoetins har vist seg å forbedre total overlevelse eller redusere risikoen for kreftprogresjon hos pasienter med kreftassosiert anemi.
Flere kontrollerte kliniske studier der epoetiner ble administrert til pasienter med en rekke vanlige maligniteter, for eksempel plateepitelkarsinom i hode- og nakkeområdet, lungekreft og brystkreft, har vist en uforklarlig økning i dødeligheten. I kontrollerte kliniske studier viste bruk av epoetin alfa og andre erytropoiesestimulerende midler (ESA):
• En reduksjon i tid til tumorprogresjon hos pasienter med avansert kreft i hode og nakke behandlet med strålebehandling ved administrering for å oppnå hemoglobinverdier større enn 14 g / dl (8,7 mmol / l),
• en reduksjon i total overlevelse og en økning i dødsfall som skyldes tumorprogresjon etter 4 måneder hos pasienter med metastatisk brystkreft behandlet med cellegift ved administrering for å oppnå hemoglobinverdier på 12-14 g / dl (7,5-8,7 mmol / l) ,
• økt risiko for død ved administrering for å oppnå hemoglobinverdier på 12 g / dl (7,5 mmol / l) hos pasienter med aktive maligniteter, som ikke er behandlet med cellegift eller strålebehandling. Bruk av ESA er ikke indisert i denne pasientpopulasjonen.
Basert på det ovennevnte, under noen kliniske tilstander bør blodtransfusjon være den foretrukne behandlingen for behandling av anemi hos kreftpasienter Beslutningen om å administrere rekombinante erytropoietiner bør være basert på en vurdering av nytte-risiko-forholdet med involvering av den enkelte pasient og bør ta hensyn til den spesifikke kliniske konteksten. Faktorer som skal vurderes i denne vurderingen bør omfatte krefttype og stadium, anemi, forventet levetid, miljøet der pasienten behandles og pasientens preferanser (se avsnitt 5.1).
Denne medisinen inneholder fenylalanin, et stoff som kan være farlig for personer med fenylketonuri.
Dette legemidlet inneholder mindre enn 1 mmol natrium (23 mg) per dose, noe som betyr at det regnes som lite natriumfattig.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon -
Behandling med erytropoietin har ikke vist seg å endre metabolismen av andre legemidler. Siden cyklosporin binder seg til erytrocytter, kan det imidlertid være mulighet for en "interaksjon med andre legemidler. Hvis erytropoietin administreres samtidig med cyklosporin, bør blodnivået av cyklosporin overvåkes og dosen av dette legemidlet må korrigeres på grunnlaget for økningen i hematokritverdien.
Det er ingen bevis som indikerer en "interaksjon mellom epoetin alfa og G-CSF eller GM-CSF med hensyn til hematologisk differensiering eller spredning i tumorbiopsiprøver. in vitro.
04.6 Graviditet og amming -
Det er ingen tilstrekkelige og godt kontrollerte studier på gravide. Dyrestudier har vist reproduksjonstoksisitet (se pkt. 5.3). Det er ikke kjent om eksogent epoetin zeta skilles ut i morsmelk. Derfor bør erytropoietin generelt bare brukes under graviditet og amming hvis de potensielle fordelene oppveier de potensielle risikoene for fosteret.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner -
Retacrit har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner.
04.8 Bivirkninger -
Oppsummering av sikkerhetsprofilen
Resultatene av kliniske studier med Retacrit er i tråd med sikkerhetsprofilen til andre autoriserte erytropoietiner. Basert på resultatene av kliniske studier med andre lisensierte erytropoietiner, forventes omtrent 8% av pasientene som er behandlet med erytropoietin å oppleve bivirkninger Bivirkninger under behandling med erytropoietin observeres hovedsakelig hos pasienter med kronisk nyresvikt eller underliggende maligniteter og de er hovedsakelig representert ved hodepine og en doseavhengig økning i blodtrykket Hypertensive kriser med symptomer som ligner på "encefalopati" kan forekomme. Det bør utvises forsiktighet ved plutselig akutt migrene-lignende hodepine, som kan være et advarselsskilt.
Overbelastning i luftveiene, inkludert hendelser med overbelastning i øvre luftveier, nesestopp og nasofaryngitt, har blitt rapportert i noen studier på voksne pasienter med nyreinsuffisiens som ennå ikke er under dialyse behandlet med forlengede doseringsintervaller.
Hos pasienter behandlet med erytropoietiske midler har trombotiske / vaskulære hendelser som myokardiskemi, hjerteinfarkt, cerebrovaskulære ulykker (hjerneblødning og hjerneinfarkt), forbigående iskemiske anfall, dyp venetrombose, arteriell trombose, lungeemboli, aneurisme, retinal trombose koagulasjon i den kunstige nyre.
Antistoff-mediert erytroblastopeni (PRCA) har blitt observert etter måneder eller år med behandling med epoetin alfa. Antistoffer mot erytropoietiner er observert hos de fleste av disse pasientene (se pkt. 4.3 og 4.4).
Utskrift av uønskede hendelser
Denne delen definerer frekvensen av bivirkninger som: Svært vanlige (> 1/10); vanlig (> 1/100 til 1/1 000 til 1/10 000 a
Innenfor hver frekvensklasse presenteres bivirkninger i synkende alvorlighetsrekkefølge.
Frekvensen kan variere avhengig av indikasjonen
Voksne og pediatriske hemodialysepasienter, voksne pasienter som gjennomgår peritonealdialyse og voksne pasienter med nedsatt nyrefunksjon som ennå ikke er i dialyse
Den hyppigste bivirkningen ved behandling med epoetin alfa er doseavhengig blodtrykksforhøyelse eller forverring av eksisterende hypertensjon. Denne økningen i blodtrykket kan behandles farmakologisk. I tillegg anbefales det å overvåke blodtrykket. Spesielt ved begynnelsen av terapien. Følgende reaksjoner har også oppstått i isolerte tilfeller av pasienter med normalt eller lavt blodtrykk: hypertensiv krise med symptomer som ligner på encefalopati (hodepine og forvirringstilstand) og generaliserte tonikokloniske anfall, som krever øyeblikkelig medisinsk inngrep og intensiv behandling. Du bør være spesielt oppmerksom til plutselig akutt migrene-lignende hodepine, som kan være et advarselsskilt.
Shunttrombose kan forekomme, spesielt hos pasienter med tendens til hypotensjon eller med komplikasjoner av arteriovenøse fistler (stenose, aneurismer, etc.). Hos disse pasientene anbefales tidlig revisjon av shunten og antitrombotisk profylakse, for eksempel med acetylsalisylsyre. .
Voksne kreftpasienter på cellegiftbehandling med symptomatisk anemi
Hypertensjon kan forekomme hos pasienter behandlet med epoetin alfa. Følgelig bør nøye overvåking av hemoglobin og blodtrykk utføres.
En økt forekomst av vaskulære trombotiske hendelser har blitt observert hos pasienter behandlet med erytropoietiske midler (se pkt. 4.4 og pkt. 4.8 - Generelle hensyn).
Pasientkandidater for kirurgi
Uavhengig av behandling med erytropoietin, kan det oppstå tromboemboliske hendelser etter gjentatte flebotomier hos kirurgiske pasienter med underliggende kardiovaskulær sykdom.
Derfor bør slike pasienter rutinemessig gjennomgå erstatning av det innsamlede blodvolumet. Hos pasienter med baseline hemoglobin> 13 g / dl, kan ikke muligheten for at Retacrit -behandling kan være forbundet med en økt risiko for postoperative trombotiske / vaskulære hendelser.
Rapportering av mistenkte bivirkninger
Rapportering av mistenkte bivirkninger som oppstår etter godkjenning av legemidlet er viktig ettersom det muliggjør kontinuerlig overvåking av nytte / risiko -balansen for legemidlet Helsepersonell bes rapportere alle mistenkte bivirkninger via det nasjonale rapporteringssystemet.
04.9 Overdosering -
Det terapeutiske vinduet for erytropoietin er veldig bredt. Overdosering av erytropoietin kan gi effekter som er forlengelser av hormonets farmakologiske effekter. Hvis det oppstår for høye hemoglobinnivåer, kan en flebotomi utføres. Om nødvendig bør det gis ytterligere støttende behandling.
05.0 FARMAKOLOGISKE EGENSKAPER -
05.1 "Farmakodynamiske egenskaper -
Farmakoterapeutisk gruppe: Andre antianemika, erytropoietin
ATC -kode: B03XA01
Retacrit er et biosimilært legemiddel. Detaljert informasjon er tilgjengelig på Det europeiske legemiddelkontorets nettsted http://www.ema.europa.eu
Farmakodynamiske effekter
Erythropoietin er et glykoprotein som, som en mitosestimulerende faktor og differensieringshormon, stimulerer produksjonen av erytrocytter fra forløperne til stamkammeret. Den tilsynelatende molekylvekten til erytropoietin er 32.000-40.000 dalton. Proteinfraksjonen av molekylet utgjør omtrent 58% av dets totale molekylvekt og består av 165 aminosyrer. De fire karbohydratkjedene er knyttet til proteinet med tre N-glykosidbindinger og en oglykosidbinding. Sett fra aminosyresekvensen og karbohydratkomposisjonen er epoetin zeta identisk med endogent humant erytropoietin isolert fra urinen til anemiske pasienter. Den biologiske effekten av erytropoietin har blitt demonstrert i forskjellige dyremodeller in vivo (normale og anemiske rotter, polycytemiske mus). Etter administrering av erytropoietin øker antallet erytrocytter, hemoglobinverdier og retikulocyttall sammen med 59Fe -inkorporeringshastigheten. I tester in vitro (mus-miltcellekultur), økt inkorporering av 3H-tymidin i kjernede erytroidceller i milten ble observert etter inkubasjon med erytropoietin.
Gjennom cellekulturer av menneskelig benmarg har det blitt vist at erytropoietin spesifikt stimulerer erytropoiesis uten å endre leukopoiesis. Ingen cytotoksisk aktivitet av erytropoietin ble observert på benmargsceller.
På samme måte som andre hematopoietiske vekstfaktorer har erytropoietin blitt vist in vitro å ha stimulerende egenskaper til menneskelige endotelceller.
Voksne pasienter med nedsatt nyrefunksjon som ennå ikke er i dialyse
I 2 studier med utvidet doseintervall av erytropoietin (3 ganger per uke, en gang i uken, en gang hver 2. uke og en gang hver fjerde uke) opprettholdt noen pasienter med lengre doseområder ikke tilstrekkelige hemoglobinnivåer og protokollkravene for seponering definert av hemoglobinet verdien er oppfylt (0% ved dosering en gang i uken, 3,7% ved dosering hver annen uke og 3,3% i grupper hver 4. uke).
Klinisk effekt og sikkerhet
Tre placebokontrollerte studier involverte 721 kreftpasienter som fikk platinafri cellegift, inkludert 389 med hematologiske maligniteter (221 med myelomatose, 144 med non-Hodgkins lymfom og 24 med andre hematologiske maligniteter) og 332 med solide svulster (172 bryst, 64 gynekologiske , 23 lunge-, 22 prostata-, 21 gastrointestinale og 30 andre). To store åpne studier inkluderte 2 697 kreftpasienter som fikk platinafri cellegift, inkludert 1 895 med solide svulster (683 bryst, 260 lunge, 174 gynekologiske, 300 gastrointestinale og 478 andre) og 802 med hematologiske maligniteter.
I en prospektiv, randomisert, dobbeltblind, placebokontrollert studie utført på 375 anemiske pasienter med forskjellige ikke-myeloide neoplasmer og som mottok platina-fri cellegift, en signifikant reduksjon i følgetilfellene forbundet med anemi (som tretthet, asteni og reduksjonsaktivitet ), målt ved hjelp av følgende vurderingsverktøy: den generelle vurderingsskalaen FACT-An (Functional Assessment of Cancer Therapy-Anemia), utmattelsesvurderingsskalaen FACT-An og Cancer Linear Analogue Scale (CLAS). To andre randomiserte, placebokontrollerte studier med færre pasienter viste ikke signifikant forbedring i livskvalitetsparametere som ble vurdert med henholdsvis EORTC-QLQ-C30 og CLAS.
Erytropoietin er en vekstfaktor som først og fremst stimulerer produksjonen av erytrocytter.Erytropoietinreseptorer kan uttrykkes på overflaten av forskjellige typer tumorceller.
Overlevelse og tumorprogresjon ble analysert i fem store kontrollerte studier, som inkluderte totalt 2.833 pasienter, inkludert fire dobbeltblinde, placebokontrollerte studier og en åpen studie. Disse studiene inkluderte pasienter som fikk cellegift (to studier) eller pasientpopulasjoner der erytropoiesestimulerende midler ikke er indikert: kreftpasienter med anemi som ikke gjennomgår cellegift og pasienter med hode- og nakkekreft., Som gjennomgikk strålebehandling. I to studier, målhemoglobin konsentrasjonen var> 13 g / dL; i de resterende studiene var den 12-14 g / dL. I den åpne studien ble det ikke funnet noen forskjell i total overlevelse mellom pasienter behandlet med rekombinant humant erytropoietin kontra kontroller. I de fire placebo- kontrollerte studier, fareforholdet (fareforhold) for total overlevelse var mellom 1,25 og 2,47, til fordel for kontroller. Sammenlignet med kontroller observerte disse studiene en statistisk signifikant, konstant og uforklarlig økning i dødelighet hos pasienter med anemi assosiert med flere vanlige maligniteter og behandlet med rekombinant humant erytropoietin. De samlede overlevelsesresultatene av studiene kunne ikke tilfredsstillende forklares med forskjellene i forekomst av trombose og tilhørende komplikasjoner hos personer behandlet med rekombinant humant erytropoietin og hos kontrollpersoner.
Det ble også utført en systematisk gjennomgang av over 9000 kreftpasienter som deltok i 57 kliniske studier. Metaanalyse av generelle overlevelsesdata ga et estimert fareforhold på 1,08 til fordel for kontroller (95% KI: 0,99, 1,18; 42 studier og 8 167 pasienter). En økt relativ risiko for tromboemboliske hendelser ble observert hos pasienter behandlet med rekombinant humant erytropoietin (RR 1,67, 95% KI: 1,35, 2,06, 35 studier og 6 769 pasienter). Det er en økt risiko for tromboemboliske hendelser hos kreftpasienter behandlet med rekombinant humant erytropoietin, og en negativ effekt på total overlevelse kan ikke utelukkes. Det er ikke kjent i hvilken grad disse dataene kan tilskrives administrering av rekombinant humant erytropoietin til kreftpasienter som får cellegift for å oppnå hemoglobinkonsentrasjoner under 13 g / dl, ettersom bare noen få pasienter med de beskrevne egenskapene ble inkludert i de gjennomgåtte dataene.
Det ble også utført en enkelt pasientdataanalyse på over 13 900 kreftpasienter (kjemoradio-, chemoradium- eller ingen terapi) som deltok i 53 kontrollerte kliniske studier med forskjellige epoetiner. Samlet overlevelse genererte et fareforhold på 1,06 til fordel for kontroller (95% KI: 1,00, 1,12: 53 studier og 13 933 pasienter) og for kreftpasienter som fikk cellegift, var det totale overlevelsesrisikoforholdet 1,04 (95% KI: 0,97, 1,11; 38 forsøk og 10 441 pasienter). -analyse støtter også en konsekvent og signifikant økt relativ risiko for tromboemboliske hendelser hos kreftpasienter behandlet med rekombinant humant erytropoietin (se pkt. 4.4).
I en randomisert, dobbeltblind, placebokontrollert studie av 4038 ikke-dialyserte CRF-pasienter med type 2 diabetes og hemoglobinverdier ≤ 11 g / dl, ble pasientene behandlet med enten darbepoetin alfa for å oppnå hemoglobinnivåer på 13 g / dl. eller placebo (se pkt. 4.4). Studien oppfylte ikke noen av de primære målene med å demonstrere å redusere risikoen for dødelighet, kardiovaskulær sykelighet og utvikling av nyresykdom i sluttstadiet (ESRD). Analyser av de enkelte komponentene i de sammensatte endepunktene viste en HR (95% CI): død 1,05 (0,92, 1,21), hjerneslag 1,92 (1,38, 2,68), kongestiv hjertesvikt (CHF) 0,89 (0,74, 1,08), hjerteinfarkt (MI) 0,96 (0,75, 1,23), sykehusinnleggelse for myokardiskemi 0,84 ( 0,55, 1,27), ESRD 1,02 (0,87, 1,18).
Samlede analyser av post-hoc-data fra kliniske studier med ESA utført hos pasienter med CRF (på dialyse, ikke på dialyse, med eller uten diabetes) ble utført. Det var en trend mot økende risikostimater for alle dødsårsaker og kardiovaskulære og cerebrovaskulære hendelser assosiert med de høyeste kumulative dosene av ESA uavhengig av diabetes eller dialysestatus (se pkt. 4.2 og 4.4).
05.2 "Farmakokinetiske egenskaper -
Intravenøs administrasjonsvei
Måling av erytropoietin etter gjentatt intravenøs administrering viste en "halveringstid på ca. 4 timer hos friske frivillige og en" noe lengre halveringstid hos pasienter med nyreinsuffisiens (ca. 5 timer). En halveringstid på omtrent 6 timer er rapportert hos barn.
Rute for subkutan administrasjon
Etter subkutan injeksjon er serum erytropoietinnivåer mye lavere enn intravenøse nivåer, øker sakte og toppes mellom 12 og 18 timer etter administrering. Denne toppen er alltid godt under det som nådde intravenøst (ca. 1/20).
Det er ingen akkumuleringsfenomener: konsentrasjonene forblir de samme, enten de oppdages 24 timer etter den første injeksjonen eller 24 timer etter den siste injeksjonen.
Halveringstiden er vanskelig å vurdere ved subkutan administrasjon og er estimert til å være ca. 24 timer. Biotilgjengeligheten av subkutan injiserbar erytropoietin er mye lavere enn det intravenøse legemidlet: ca. 20%.
05.3 Prekliniske sikkerhetsdata -
I noen prekliniske toksikologiske studier på hunder og rotter, men ikke hos aper, har erytropoietinbehandling vært assosiert med subklinisk benmargsfibrose (beinmargsfibrose er en kjent komplikasjon av kronisk nyresvikt hos mennesker og kan være relatert til sekundær hyperparatyreoidisme eller ukjente faktorer) . I en studie utført på hemodialysepasienter behandlet med erytropoietin i 3 år, var forekomsten av beinmargsfibrose ikke økt sammenlignet med en tilsvarende gruppe kontrollpasienter på dialyse, men ikke behandlet med erytropoietin.
Dyrestudier har vist at erytropoietin reduserer fostrets kroppsvekt, forsinker ossifikasjonsprosessen og øker fosterdødeligheten når den gis i ukentlige doser omtrent 20 ganger anbefalt for mennesker. Disse endringene tolkes som sekundære til den reduserte økningen i mors kroppsvekt.
Erytropoietin viste ingen aktivitet i mutagenisitetstester på cellekulturer av bakterier og pattedyr og in vivo i en mus mikronukleustest. Langsiktige kreftfremkallende studier har ikke blitt utført. Det er motstridende data i litteraturen om muligheten for at erytropoietin spiller en viktig rolle i spredningen av kreftceller. Disse dataene er basert på oppnådde resultater in vitro fra humane tumorvevsprøver; Imidlertid er omfanget i de kliniske omgivelsene uklart.
06.0 LEGEMIDDELOPPLYSNINGER -
06.1 Hjelpestoffer -
Dinatriumfosfatdihydrat
Natriummonobasisk fosfatdihydrat
Natriumklorid
Kalsiumkloriddihydrat
Polysorbat 20
Glycin
Leucine
Isoleucin
Threonine
Glutaminsyre
Fenylalanin
Vann for injiserbare løsninger
Natriumhydroksid (for å justere pH)
Saltsyre (for å justere pH)
06.2 Uforlikelighet "-
I mangel av inkompatibilitetsstudier, må dette legemidlet ikke blandes med andre produkter.
06.3 Gyldighetsperiode "-
30 måneder
06.4 Spesielle forholdsregler ved lagring -
Oppbevares i kjøleskap (2 ° C - 8 ° C). Ikke frys.
Oppbevar den ferdigfylte sprøyten i ytteremballasjen for å beskytte medisinen mot lys.
Under poliklinisk bruk kan pasienten fjerne produktet fra kjøleskapet og oppbevare det ved romtemperatur (ikke over 25 ° C) i en periode på maksimalt 3 dager.
06.5 Emballasje og innhold i emballasje -
0,3 ml oppløsning i type I glass ferdigfylt sprøyte med fast stålnål og PTFE-foret stempelstopper med eller uten nålebeskytter.
En pakke inneholder 1 eller 6 ferdigfylte sprøyter.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering -
Instruksjoner for håndtering av Retacrit:
1. Etter at du har fjernet en sprøyte fra blisteren, må du kontrollere at oppløsningen er klar, fargeløs og praktisk talt fri for synlige partikler.
2. Fjern nåldekselet og slipp luften fra nålen og sprøyten ved å holde sprøyten i oppreist posisjon og skyve stempelet forsiktig oppover.
3. Sprøyten er klar til bruk.
Retacrit skal ikke brukes hvis noe av det følgende skjer:
• blemmen er åpen eller på annen måte skadet;
• løsningen ikke er fargeløs eller inneholder synlige partikler i suspensjon;
• c "væske har lekket fra den ferdigfylte sprøyten eller kondens er synlig inne i blemmen som fortsatt er forseglet;
• medisinen ble ved et uhell frosset.
Dette legemidlet er kun beregnet for engangsbruk.
Ikke rist.
Ubrukte medisiner og avfall fra denne medisinen må kastes i henhold til lokale forskrifter.
07.0 INNEHAVER AV "MARKEDSFØRINGSTILLATELSEN" -
Hospira UK Limited
Horisont
Honey Lane
Hurley
Maidenhead
SL6 6RJ
Storbritannia
08.0 MARKEDSFØRINGSTILLATELSESNUMMER -
EU/1/07/431/001 ferdigfylt sprøyte
EU/1/07/431/002 ferdigfylt sprøyte
EU/1/07/431/026 ferdigfylt sprøyte med nålebeskyttelse
EU/1/07/431/027 ferdigfylt sprøyte med nålebeskyttelse
038381012
038381024
038381265
038381277
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN -
Dato for første godkjenning: 18. desember 2007
Dato for siste fornyelse: 15. november 2012
10.0 DATO FOR REVISJON AV TEKSTEN -
D.CCE september 2016
11.0 FOR RADIOMEDLEM, FULLSTØTTE DATA OM DEN INTERNE RADIASJONSDOSIMETRI -
12.0 FOR RADIOMEDLEM, YTTERLIGERE DETALJERTE INSTRUKSJONER OM EKSPORARISK FORBEREDELSE OG KVALITETSKONTROLL -