Aktive ingredienser: Dabigatran (dabigatran etexilat)
Pradaxa 110 mg harde kapsler
Pradaxa pakningsinnsatser er tilgjengelige for pakningsstørrelser:- Pradaxa 75 mg harde kapsler
- Pradaxa 110 mg harde kapsler
- Pradaxa 150 mg harde kapsler
Hvorfor brukes Pradaxa? Hva er den til?
Pradaxa er et legemiddel som inneholder virkestoffet dabigatranetexilat. Det blokkerer virkningen av et stoff i kroppen som er involvert i dannelsen av blodpropper.
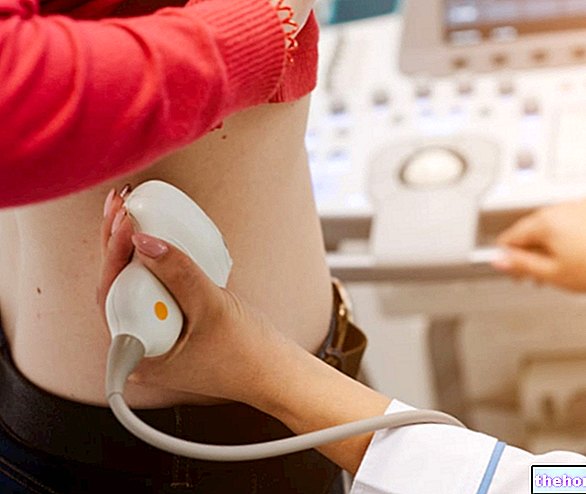
Pradaxa brukes til å forhindre blodpropp i venene etter kne- eller hofteutskiftningskirurgi hos voksne.
Pradaxa er et legemiddel som brukes for å redusere risikoen for blodårer i hjernen eller resten av kroppen blokkert av dannelse av blodpropper, hos voksne pasienter med endret hjerteslag (atrieflimmer) og med ytterligere risikofaktorer. Pradaxa er et legemiddel som gjør blodet tynnere, og reduserer risikoen for blodpropp.
Pradaxa er et legemiddel som brukes til å behandle blodpropper i venene i bena og lungene og for å forhindre at blodpropp kommer tilbake i venene i bena og lungene.
Kontraindikasjoner Når Pradaxa ikke skal brukes
Ikke ta Pradaxa
- dersom du er allergisk mot dabigatranetexilat eller noen av de andre innholdsstoffene i dette legemidlet (listet opp i avsnitt 6).
- hvis nyrefunksjonen din er alvorlig redusert
- hvis du har pågående blødninger.
- hvis du har skader på et organ som øker risikoen for alvorlig blødning.
- hvis du har en økt blødningstendens. Dette kan være medfødt, på grunn av ukjent årsak eller på grunn av andre medisiner.
- hvis du har alvorlig nedsatt leverfunksjon eller leversykdom som på en eller annen måte kan forårsake død.
- hvis du tar ketokonazol eller itrakonazol gjennom munnen, medisiner for behandling av soppinfeksjoner.
- hvis du tar ciklosporin, et legemiddel for å forhindre avstøtning etter organtransplantasjon.
- hvis du tar dronedarone, et legemiddel som brukes for å forhindre at problemet med uregelmessig hjerterytme kommer tilbake.
- hvis du tar medisiner for å forhindre blodpropp (f.eks. warfarin, rivaroxaban, apixaban eller heparin), bortsett fra når du bytter fra en antikoagulant behandling til en annen eller når et arterielt venekateter plasseres og tar heparin gjennom det for å holde det åpent.
- hvis du har blitt implantert med en kunstig hjerteventil.
Forholdsregler for bruk Hva du må vite før du bruker Pradaxa
Snakk med legen din før du tar Pradaxa. Du kan også trenge å se legen din under behandling med Pradaxa hvis du opplever symptomer eller hvis du må opereres. Fortell legen din dersom du har eller har lidd av en medisinsk tilstand eller sykdom, spesielt noen av dem som er inkludert i følgende liste:
- hvis du lider av leversykdom forbundet med unormale blodprøver, anbefales ikke bruk av Pradaxa.
- hvis du har økt risiko for blødning slik det kan være i følgende situasjoner:
- hvis du nylig har hatt blødninger.
- hvis du har hatt en biopsi (kirurgisk fjerning av vev) i forrige måned.
- hvis du har fått alvorlige skader (f.eks. beinbrudd, hodeskade eller skader som krevde kirurgi).
- hvis du lider av betennelse i spiserøret eller magen.
- hvis du har problemer med tilbakeløp av magesaft til spiserøret.
- hvis du har tatt medisiner som kan øke risikoen for blødninger, for eksempel aspirin (acetylsalisylsyre), klopidogrel, ticagrelor.
- hvis du tar antiinflammatoriske legemidler som diklofenak, ibuprofen, piroksikam.
- hvis du har hjerteinfeksjon (bakteriell endokarditt).
- hvis du vet at nyrefunksjonen din er svekket eller du lider av dehydrering (symptomer inkluderer tørst og vannlating i reduserte mengder mørk (konsentrert) urin).
- hvis du er over 75 år.
- hvis den veier 50 kg eller mindre.
- hvis du har hatt et hjerteinfarkt eller har blitt diagnostisert med tilstander som øker risikoen for å utvikle et hjerteinfarkt.
- hvis du gjennomgår en planlagt operasjon. Pradaxa må stoppes midlertidig på grunn av økt risiko for blødning under og kort tid etter operasjonen. Om mulig bør Pradaxa stoppes minst 24 timer før operasjonen. Hos pasienter med økt blødningsrisiko kan legen bestemme å stoppe behandlingen tidligere.
- hvis du gjennomgår en ikke -planlagt operasjon. Om mulig bør operasjonen utsettes til 12 timer etter den siste dosen Pradaxa. Hvis operasjonen ikke kan utsettes, kan det være økt risiko for blødning. Legen din vil vurdere risikoen for blødning og det haster med kirurgi.
- hvis du har et rør (kateter) satt inn i ryggen: et rør kan settes inn i ryggen, f.eks. for å administrere bedøvelsesmidler eller smertelindrende medisiner, under eller etter operasjonen. Hvis du får Pradaxa etter at du har fjernet et kateter, vil legen sjekke deg regelmessig.
- hvis du faller eller skader deg selv under behandlingen, spesielt hvis du får et slag i hodet, ring legen din med en gang. Legen din kan finne det nødvendig å se deg fordi du kan ha stor risiko for blødning.
Barn og ungdom
Pradaxa skal ikke brukes til barn og ungdom under 18 år.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Pradaxa
Fortell legen din eller apoteket dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler. F.eks .:
- Legemidler som reduserer blodpropp (f.eks. Warfarin, fenprocoumon, heparin, klopidogrel, prasugrel, ticagrelor, rivaroxaban)
- Antiinflammatoriske og smertelindrende medisiner (f.eks. Aspirin)
- Johannesurt, en urtemedisin for å behandle depresjon
- Antidepressiva medisiner kalt selektive serotoninopptakshemmere eller selektive serotonin-noradrenalinopptakshemmere
- Rifampicin eller klaritromycin, to antibiotika
- Legemidler til behandling av endret hjerteslag (f.eks. Amiodaron, dronedaron, kinidin, verapamil).
Forebygging av blodproppdannelse etter hofte- og kneutskiftning
Hvis du bruker medisiner som inneholder amiodaron, kinidin eller verapamil, bør du ta en redusert dose Pradaxa på 150 mg én gang daglig som 2 kapsler à 75 mg, da risikoen for blødning kan øke. Pradaxa og disse medisinene må tas sammen.
Hvis du tar medisiner som inneholder verapamil og nyrefunksjonen din er redusert med mer enn halvparten, bør du ta en redusert dose Pradaxa på 75 mg, da risikoen for blødning kan øke.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper, som har utviklet seg som et resultat av endret hjerteslag og Behandling av blodpropper i venene i bena og lungene, inkludert forebygging av blodpropp i venene i bena og lungene
Hvis du bruker verapamilholdige medisiner, bør du ta en redusert dose Pradaxa på 220 mg tatt som en kapsel på 110 mg to ganger daglig, da risikoen for blødning kan øke. Pradaxa og verapamilholdige medisiner bør tas sammen.
- Legemidler til behandling av soppinfeksjoner (f.eks. Ketokonazol, itrakonazol, posakonazol) med mindre det bare påføres huden
- Medisiner for å forhindre direkte episoder etter organtransplantasjon (f.eks. Takrolimus, cyklosporin)
- Virale medisiner for AIDS (f.eks. Ritonavir)
- Legemidler mot epilepsi (f.eks. Karbamazepin, fenytoin)
Advarsler Det er viktig å vite at:
Graviditet og amming
Effekten av Pradaxa på graviditet og foster er ikke kjent. Du bør ikke ta Pradaxa hvis du er gravid, med mindre legen din forteller deg at det er trygt å gjøre det. Hvis du er en kvinne i fertil alder, må du unngå å bli gravid mens du blir behandlet med Pradaxa.
Du bør ikke amme mens du blir behandlet med Pradaxa.
Kjøring og bruk av maskiner
Pradaxa har ingen kjente effekter på evnen til å kjøre bil eller bruke maskiner.
Pradaxa inneholder solnedgangsgult (E110)
Denne medisinen inneholder et fargestoff som kalles sunset yellow (E110) som kan forårsake allergiske reaksjoner
Dose, metode og administrasjonstidspunkt Hvordan bruke Pradaxa: Dosering
Ta alltid dette legemidlet nøyaktig slik legen din har fortalt deg. Rådfør deg med lege hvis du er i tvil.
Ta Pradaxa som anbefalt for følgende forhold:
Forebygging av blodproppdannelse etter kirurgi i kne eller hofte
Den anbefalte dosen er 220 mg én gang daglig (tatt som 2 kapsler à 110 mg).
Hvis nyrefunksjonen din er redusert med mer enn halvparten, eller hvis du er 75 år eller eldre, er anbefalt dose 150 mg én gang daglig (tatt som 2 kapsler à 75 mg).
Hvis du tar medisiner som inneholder amiodaron, kinidin eller verapamil, er anbefalt dose 150 mg en gang daglig (tatt som 2 kapsler à 75 mg).
Hvis du tar medisiner som inneholder verapamil og nyrefunksjonen din er redusert med mer enn halvparten, bør du ta en redusert dose Pradaxa på 75 mg, da risikoen for blødning kan øke.
Etter kneutskiftning
Du bør starte behandlingen med Pradaxa innen 1-4 timer etter at du har fullført operasjonen, ta en enkelt kapsel. Deretter to kapsler, en gang om dagen, i totalt 10 dager.
Etter hofteutskiftning
Du må starte behandlingen med Pradaxa innen 1-4 timer etter at du har fullført operasjonen, ta en enkelt kapsel. Deretter to kapsler, en gang om dagen, i totalt 28-35 dager.
For begge operasjonene bør behandlingen ikke startes ved blødning på operasjonsstedet.Hvis behandlingen ikke kan startes før dagen etter operasjonen, bør administrasjonen starte med en dose på 2 kapsler en gang daglig.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper som har utviklet seg som et resultat av endret hjerterytme og behandling av blodpropper i venene i bena og lungene, inkludert forhindring av dannelse av blodpropper i venene i bena og lungene
Den anbefalte dosen er 300 mg tatt som en 150 mg kapsel to ganger daglig.
Hvis du er 80 år eller eldre, er den anbefalte dosen Pradaxa 220 mg tatt som en 110 mg kapsel to ganger daglig.
Hvis du bruker verapamilholdige medisiner, bør du ta en redusert dose Pradaxa på 220 mg som en kapsel på 110 mg to ganger daglig, da risikoen for blødning kan øke.
Hvis du potensielt har økt risiko for blødning, kan legen din bestemme å foreskrive en 220 mg dose Pradaxa tatt som en 110 mg kapsel to ganger daglig.
Pradaxa kan tas med eller uten mat. Kapslen skal svelges hel med et glass vann for å sikre at magesekken frigjøres. Ikke brekk, tygg eller fjern granulatet fra kapslen, da dette kan øke risikoen for blødning.
Følg instruksjonene nedenfor når du bruker Pradaxa i blisterpakning
- Fjern kapslene fra blisterpakningen ved å løfte aluminiumsfolien på baksiden.
- ikke skyv kapslene gjennom blisterpakningen.
- aluminiumsfolien fra blisterpakningen skal bare løftes når en kapsel skal fjernes.
Følg instruksjonene nedenfor når du bruker Pradaxa pakket på flaske
- flasken åpnes ved å trykke og vri lokket.
Endring i antikoagulant behandling
- Bytte fra Pradaxa -behandling til behandling med antikoagulantia gitt ved injeksjon:
Forebygging av blodproppdannelse etter kirurgi i kne eller hofte
Ikke start behandlingen med injiserbare antikoagulantia (f.eks. Heparin) før 24 timer har gått siden siste administrering av Pradaxa.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper som har utviklet seg som et resultat av endret hjerterytme og behandling av blodpropper i venene i bena og lungene, inkludert forhindring av dannelse av blodpropper i venene i bena og lungene
Ikke start behandlingen med injiserbare antikoagulantia (f.eks. Heparin) før 12 timer har gått siden siste administrering av Pradaxa.
- Bytte fra behandling med antikoagulantia gitt ved injeksjon til behandling med Pradaxa:
Begynn å ta Pradaxa 0–2 timer før neste injeksjon.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper som har utviklet seg som et resultat av endret hjerteslag og behandling av blodpropper i venene i bena og lungene, inkludert forebygging av blod blodpropp i venene i bena og lungene
- Bytte fra Pradaxa-behandling til behandling med blodfortynnende medisiner som inneholder vitamin K-antagonister (f.eks. Fenprocoumon): legen din bør be deg om å ta blodprøver og fortelle deg når du skal starte behandling med vitamin K-antagonister.
- Bytte fra behandling med blodfortynnende medisiner som inneholder vitamin K-antagonister (f.eks. Fenprocoumon) til behandling med Pradaxa: Slutt å ta medisinen som inneholder vitamin K-antagonisten. Legen din bør be deg om å ta blodprøver og fortelle deg når du starter behandling med Pradaxa.
Overdosering Hva du skal gjøre hvis du har tatt for mye Pradaxa
Dersom du tar for mye av Pradaxa
Hvis du tar mer Pradaxa enn anbefalt, kan du ha økt risiko for blødning. Legen din kan ta en blodprøve for å vurdere risikoen for blødning.
Fortell legen din umiddelbart hvis du tar mer Pradaxa enn foreskrevet. Hvis det oppstår en blødningsepisode, kan det være nødvendig med kirurgi eller behandling med blodoverføringer.
Dersom du har glemt å ta Pradaxa
Forebygging av blodproppdannelse etter kirurgi i kne eller hofte
Fortsett med de resterende daglige dosene Pradaxa til vanlig tid neste dag. Ikke ta en dobbel dose for å gjøre opp for en glemt dose.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper som har utviklet seg som et resultat av endret hjerteslag og behandling av blodpropper i venene i bena og lungene, inkludert forebygging av blod blodpropp i venene i bena og lungene
Den glemte dosen kan fortsatt tas opptil 6 timer før neste dose. Hvis det er mindre enn 6 timer før neste dose, bør den glemte dosen hoppes over. Ikke ta en dobbel dose for å gjøre opp for en glemt dose.
Hvis du slutter å ta Pradaxa
Ta Pradaxa nøyaktig som foreskrevet. Ikke slutte å ta Pradaxa uten å sjekke med legen din først. Stopp av Pradaxa kan øke risikoen for å utvikle blodpropp hos pasienter som behandles etter hofte- eller kneutskiftning.
Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette legemidlet.
Bivirkninger Hva er bivirkningene av Pradaxa
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Pradaxa virker på blodproppssystemet, så de fleste bivirkninger er relatert til tegn som hematom eller blødning.
Store eller alvorlige blødningshendelser kan oppstå, dette er de mest alvorlige bivirkningene, som uansett beliggenhet kan være invalidiserende, livstruende eller til og med føre til døden. I noen tilfeller er det ikke sikkert at disse blødningene er synlige.
Hvis du opplever blødninger som ikke løser seg spontant, eller hvis du opplever symptomer på overdreven blødning (eksepsjonell svakhet, trøtt følelse, blek hud, svimmelhet, hodepine eller uforklarlig hevelse), kontakt lege umiddelbart.
Legen din kan beslutte å få deg sjekket nøye eller endre behandlingen.
Fortell legen din umiddelbart hvis du opplever en alvorlig allergisk reaksjon som forårsaker pustevansker eller svimmelhet.
Bivirkninger er listet opp nedenfor, gruppert etter hvor ofte de oppstår.
Vanlige (kan forekomme hos opptil 1 av 10 personer):
- Reduksjon i mengden hemoglobin i blodet (stoffet i røde blodlegemer)
- Unormale leverfunksjonstestresultater
Mindre vanlige (kan forekomme hos opptil 1 av 100 personer):
- Blødning som kan oppstå fra nese, mage eller tarm, penis / skjede eller urinveier (inkludert blod i urinen som gjør det rosa eller rødt), fra hemorroider, inn i endetarmen, under huden, i et ledd, fra et sår eller senere til det, etter operasjonen
- Dannelse av hematom eller hematom som oppstår etter en "operasjon
- Tilstedeværelse av blod i avføringen, påvist ved laboratorieundersøkelse
- Reduksjon i antall røde blodlegemer i blodet
- Reduksjon i andelen røde blodlegemer i blodet
- Allergisk reaksjon
- Han retched
- Diaré med dårlig formet eller flytende avføring
- Føler meg uvel
- Eksudasjon av en liten mengde væske fra snittet laget for kirurgiske formål
- Sårutslipp (ekssudasjon av væske fra operasjonssåret)
Sjeldne (kan forekomme hos opptil 1 av 1000 personer):
- Blør
- Blødning som kan oppstå i hjernen, fra et "kirurgisk snitt, injeksjonssted eller kateterinnføringssted i en vene
- Blodfarget utslipp fra kateterinnføringsstedet i en vene
- Ekspektorasjon av blod eller blodfarget sputum
- Reduksjon i antall blodplater i blodet
- Reduksjon i antall røde blodlegemer i blodet etter en "operasjon
- Alvorlig allergisk reaksjon som forårsaker pustevansker eller svimmelhet
- Alvorlig allergisk reaksjon som forårsaker hevelse i ansikt eller hals
- Merkbart hudutslett med mørkerøde, hovne, kløende klumper forårsaket av en allergisk reaksjon
- Plutselig endring av huden som endrer farge og utseende
- Kløe
- Magesår (inkludert sår i spiserøret)
- Betennelse i spiserøret og magen
- Tilbakestrømning av magesaft i spiserøret
- Smerter i magen eller magen
- Fordøyelsesbesvær
- Vansker med å svelge
- Væske fra et sår
- Væske som kommer fra et sår etter en operasjon
Ikke kjent (frekvens kan ikke estimeres ut fra tilgjengelige data):
- Pustevansker eller tungpustethet
Behandling av blodpropp i venene i bena og lungene, inkludert forhindring av gjenoppbygging av blodpropper i venene i bena og / eller lungene
Vanlige (kan forekomme hos opptil 1 av 10 personer):
- Blødning som kan oppstå fra nese, mage eller tarm, endetarm, penis / skjede eller urinveier (inkludert blod i urinen som gjør det rosa eller rødt) eller under huden
- Fordøyelsesbesvær
Mindre vanlige (kan forekomme hos opptil 1 av 100 personer):
- Blør
- Blødning som kan oppstå i en ledd fra et sår
- Blødning som kan oppstå fra hemorroider
- Reduksjon i antall røde blodlegemer i blodet
- Hematomdannelse
- Ekspektorasjon av blod eller blodfarget sputum
- Allergisk reaksjon
- Plutselig endring av huden som endrer farge og utseende
- Kløe
- Magesår
- Betennelse i spiserøret og magen
- Tilbakestrømning av magesaft i spiserøret
- Føler meg uvel
- Han retched
- Smerter i magen eller magen
- Diaré med dårlig formet eller flytende avføring
- Vansker med å svelge
- Unormale leverfunksjonstestresultater
- Økte leverenzymer
Sjeldne (kan forekomme hos opptil 1 av 1000 personer):
- Blødning som kan oppstå fra et "kirurgisk snitt eller injeksjonssted eller kateterinnføringssted i en vene eller fra hjernen
- Reduksjon i antall blodplater i blodet
- Alvorlig allergisk reaksjon som forårsaker pustevansker eller svimmelhet
- Alvorlig allergisk reaksjon som forårsaker hevelse i ansikt eller hals
- Merkbart hudutslett med mørkerøde, hovne, kløende klumper forårsaket av en allergisk reaksjon
- Vansker med å svelge
- Reduksjon i antall røde blodlegemer i blodet
Ikke kjent (frekvens kan ikke estimeres ut fra tilgjengelige data):
- Pustevansker eller tungpustethet
- Reduksjon i mengden hemoglobin i blodet (stoffet i røde blodlegemer)
- Reduksjon i antall røde blodlegemer i blodet
- Gulfarging av huden eller det hvite i øynene, forårsaket av lever- eller blodproblemer
Rapportering av bivirkninger
Snakk med legen din eller apoteket hvis du får bivirkninger. Dette inkluderer eventuelle bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også melde fra om bivirkninger direkte via det nasjonale meldingssystemet. Mer informasjon om sikkerheten til dette legemidlet.
Forebygging av blokkering av blodkar i hjernen eller resten av kroppen på grunn av dannelse av blodpropper som utvikler seg som følge av endret hjerteslag: I en klinisk studie var frekvensen av hjerteinfarkt høyere med Pradaxa enn med warfarin. Den totale forekomsten var lav.
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Ikke bruk dette legemidlet etter utløpsdatoen som er angitt på esken, blisteren eller flasken etter Utløpsdatoen. Utløpsdatoen refererer til den siste dagen i den måneden.
Blister: Oppbevares i originalpakningen for å beskytte mot fuktighet.
Flaske: Etter åpning bør medisinen brukes innen 4 måneder. Hold flasken tett lukket. Oppbevares i originalpakningen for å beskytte mot fuktighet.
Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Sammensetning og farmasøytisk form
Hva Pradaxa inneholder
- Virkestoffet er dabigatran, som administreres i form av dabigatranetexilat som dabigatranetexilatmesylat, i en dose på 110 mg.
- Andre innholdsstoffer er vinsyre, arabisk tyggegummi, hypromellose, dimetikon 350, talkum og hydroksypropylcellulose.
- Kapselskallet inneholder karrageenan, kaliumklorid, titandioksid, indigokarmin, solnedgangsgult (E110), hypromellose og renset vann.
- Svart trykkfarge inneholder skjellakk, N-butylalkohol, isopropylalkohol, industriell denaturert etanol, svart jernoksid, renset vann og propylenglykol.
Beskrivelse av hvordan Pradaxa ser ut og innholdet i pakningen
Pradaxa er en hard kapsel.
Pradaxa 110 mg harde kapsler har en ugjennomsiktig lyseblå hette og ugjennomsiktig kremkropp. Boehringer Ingelheim -logoen er trykt på hetten og koden "R110" på kapselen.
Pradaxa 110 mg harde kapsler er tilgjengelig i pakninger som inneholder 10x1, 30x1, 60x1 harde kapsler, i en flerpakning som inneholder 3 pakninger med 60x1 harde kapsler (180 harde kapsler) eller i en flerpakning som inneholder 2 pakninger med 50x1 harde kapsler (100 harde kapsler) i blister aluminium delelig med enhetsdose.
Pradaxa 110 mg harde kapsler er også tilgjengelig i pakninger som inneholder 60 x 1 harde kapsler i hvite perforerte enhetsdoser aluminiumsblister.
Pradaxa 110 mg harde kapsler er også tilgjengelig i flasker av polypropylen (plast) som inneholder 60 harde kapsler.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
PRADAXA 75 MG HARDE KAPSULER
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver harde kapsel inneholder 75 mg dabigatranetexilat (som mesylat).
Hjelpestoffer med kjente effekter:
Hver harde kapsel inneholder 2 mcg solnedgangsgult (E110).
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Hard kapsel.
Kapsler med ugjennomsiktig lyseblå hette og størrelse 2 ugjennomsiktig kremkropp fylt med gulaktige pellets. Boehringer Ingelheim -logoen er trykt på hodet, "R75" på kroppen.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Primær forebygging av tromboemboliske episoder hos voksne pasienter som gjennomgår valgfri total hofte- eller kneutskiftningskirurgi.
04.2 Dosering og administrasjonsmåte
Dosering
Primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi
Pasienter som gjennomgår valgfri kneutskiftningskirurgi
Den anbefalte dosen Pradaxa er 220 mg en gang daglig, tatt som 2 kapsler à 110 mg. Behandlingen bør starte oralt innen 1-4 timer etter endt operasjon med en 110 mg kapsel og fortsette fra neste dag med 2 kapsler en gang daglig i totalt 10 dager.
Pasienter som gjennomgår valgfri hofteerstatningskirurgi
Den anbefalte dosen Pradaxa er 220 mg en gang daglig, tatt som 2 kapsler à 110 mg. Behandlingen bør starte oralt innen 1-4 timer etter endt operasjon med en 110 mg kapsel og fortsette fra neste dag med 2 kapsler en gang daglig i totalt 28-35 dager.
For de følgende gruppene er den anbefalte daglige dosen Pradaxa 150 mg en gang daglig, tatt som 2 kapsler à 75 mg.
Behandlingen bør starte oralt innen 1-4 timer etter endt operasjon med en 75 mg kapsel og fortsette fra neste dag med 2 kapsler en gang daglig i totalt 10 dager (kneutskiftningskirurgi) eller 28 dager. -35 dager (hofteutskiftning kirurgi):
• Pasienter med moderat nedsatt nyrefunksjon (kreatininclearance, CrCL 30-50 ml / min [se Nedsatt nyrefunksjon (primær forebygging av venøs tromboembolisme-episoder ved ortopedisk kirurgi)]
• Pasienter som samtidig får verapamil, amiodaron, kinidin [se Samtidig bruk av Pradaxa med svake til moderate P-glykoprotein (P-gp) hemmere, for eksempel amiodaron, kinidin eller verapamil (primær forebygging av venøs tromboembolisme ved ortopedisk kirurgi)]
• Pasienter i alderen 75 år og eldre [se Eldre pasienter (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)]
For begge intervensjonene, hvis hemostase ikke er normal, bør starten på behandlingen utsettes. Hvis behandlingen ikke startes på operasjonsdagen, bør den startes med 2 kapsler en gang daglig.
Vurdering av nyrefunksjon (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi):
Hos alle pasienter:
• Nyrefunksjonen bør vurderes ved å beregne kreatininclearance (CrCL) før start av Pradaxa -behandling for å utelukke pasienter med alvorlig nedsatt nyrefunksjon (dvs. CrCL
• Nyrefunksjonen bør også evalueres når det er mistanke om nedsatt nyrefunksjon under behandlingen (f.eks. Hypovolemi, dehydrering og ved samtidig bruk av visse legemidler).
Metoden som ble brukt til å estimere nyrefunksjonen (CrCL i ml / min) under den kliniske utviklingen av Pradaxa var den til Cockgroft-Gault. Formelen er som følger:
• For kreatinin uttrykt i mcmol / l:
• For kreatinin uttrykt i mg / dl:
Denne metoden anbefales for å evaluere pasienters CrCL før og under behandling med Pradaxa.
Spesielle populasjoner
Nedsatt nyrefunksjon (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Behandling med Pradaxa hos pasienter med alvorlig nedsatt nyrefunksjon (CrCLr
Klinisk erfaring hos pasienter med moderat nedsatt nyrefunksjon (CrCL 30-50 ml / min) er begrenset. Disse pasientene bør behandles med forsiktighet. Den anbefalte dosen er 150 mg tatt en gang daglig som 2 75 mg kapsler (se pkt. 4.4 og 5.1).
Samtidig bruk av Pradaxa med svake til moderate P-glykoprotein (P-gp) hemmere, for eksempel amiodaron, kinidin eller verapamil (primær forebygging av venøs tromboembolisme ved ortopedisk kirurgi)
Pradaxa -dosen bør reduseres til 150 mg, tatt en gang daglig som to 75 mg kapsler, hos pasienter som får dabigatranetexilat og amiodaron, kinidin eller verapamil samtidig (se pkt. 4.4 og 4.5). I dette tilfellet må Pradaxa og disse medisinene tas sammen.
Hos pasienter med moderat nedsatt nyrefunksjon som samtidig behandles med dabigatranetexilat og verapamil, bør en dosereduksjon av Pradaxa til 75 mg per dag vurderes (se pkt. 4.4 og 4.5).
Eldre (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Klinisk erfaring er begrenset hos eldre pasienter (> 75 år). Disse pasientene bør behandles med forsiktighet. Den anbefalte dosen er 150 mg én gang daglig som to 75 mg kapsler (se pkt. 4.4 og 5.1).
Siden nedsatt nyrefunksjon kan være hyppig hos eldre (alder> 75 år), bør nyrefunksjonen vurderes ved å beregne CrCL før behandling med Pradaxa startes for å utelukke pasienter med alvorlig nedsatt nyrefunksjon (dvs.
Nedsatt leverfunksjon (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Pasienter med leverenzymer forhøyet over det dobbelte av den øvre grensen for normal (ULN) ble ekskludert fra kliniske studier som evaluerte forebygging av VTE etter valgfri total hofte- eller kneutskiftningskirurgi .. Det er ingen erfaring med behandling av denne subpopulasjonen av pasienter, og derfor bruk av Pradaxa anbefales ikke i denne populasjonen (se pkt. 4.4 og 5.2). Det er kontraindisert ved nedsatt leverfunksjon eller leversykdom som kan ha noen innvirkning på overlevelse (se pkt. 4.3).
Vekt (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Klinisk erfaring med anbefalt dose hos pasienter som veier 110 kg er svært begrenset Basert på kliniske og kinetiske data er ingen dosejustering nødvendig (se pkt. 5.2), men tett klinisk overvåking anbefales (se avsnitt 4.4).
Kjønn (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Basert på tilgjengelige kliniske og kinetiske data, er ingen dosejustering nødvendig (se pkt.5.2).
Bytte (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Fra behandling med Pradaxa til et parenteralt antikoagulant
Det anbefales å vente 24 timer etter siste dose før du bytter fra Pradaxa til et parenteralt antikoagulant (se pkt. 4.5).
Fra parenterale antikoagulantia til Pradaxa
Hold tilbake parenteral antikoagulant og start dabigatranetexilat 0-2 timer før planlagt neste dose av den opprinnelige behandlingen eller ved seponering ved kontinuerlig behandling (f.eks. Intravenøs, ikke-fraksjonert heparin (ENF)) (se pkt. 4.5).
Pediatrisk populasjon (primær forebygging av venøs tromboembolisme -episoder ved ortopedisk kirurgi)
Det er ingen relevant bruk av Pradaxa i den pediatriske populasjonen i indikasjonen: primær forebygging av venøs tromboembolisme -episoder hos pasienter som gjennomgår elektiv total hofteutskiftningskirurgi eller valgfri total kneutskiftningskirurgi.
Glemt dose (primær forebygging av venøse tromboembolisme -episoder ved ortopedisk kirurgi)
Det anbefales at de resterende daglige dosene av dabigatranetexilat fortsetter på samme tid neste dag.
Ikke doble doser for å gjøre opp for en glemt dose.
Administrasjonsmåte (primær forebygging av venøse tromboembolisme -episoder ved ortopedisk kirurgi)
Pradaxa kan tas med eller uten mat. Pradaxa bør svelges hele med et glass vann for å lette magesekken.
Pasienter bør instrueres om ikke å åpne kapslene, da dette kan føre til økt risiko for blødning (se pkt. 5.2 og 6.6).
04.3 Kontraindikasjoner
• Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene listet opp i pkt. 6.1
• Pasienter med alvorlig nedsatt nyrefunksjon (CrCL
• Klinisk signifikant aktiv blødning
• Skader eller tilstander, hvis de anses som en betydelig risikofaktor for større blødninger. De kan omfatte nåværende eller nylig gastrointestinalt sår, høy risiko for blødende neoplasmer, nylig hjerne- eller ryggmargsskade, nylig hjerne-, spinal- eller oftalmisk kirurgi, nylig intrakranial blødning, kjente eller mistenkte esophageal varices, arteriovenøse misdannelser, vaskulære aneurysmer eller større intraspinal eller intracerebral vaskulær abnormiteter
• Samtidig behandling med andre antikoagulantia, for eksempel ikke -fraksjonert heparin (ENF), lavmolekylær heparin (enoxaparin, dalteparin etc.), heparinderivater (fondaparinux etc.), orale antikoagulantia (warfarin, rivaroxaban, apixaban etc.) laget med unntak av spesifikke spesifikasjoner omstendigheter ved endring av antikoagulant terapi (se pkt. 4.2) eller når ENF administreres i doser som er nødvendige for å opprettholde et sentralt venøst eller arterielt kateterpatent (se pkt. 4.5)
• Nedsatt leverfunksjon eller leversykdom som kan ha noen innvirkning på overlevelse
• Samtidig behandling med systemisk ketokonazol, cyklosporin, itrakonazol og dronedaron (se pkt. 4.5)
• Hjerteventilproteser som krever antikoagulasjonsbehandling (se pkt. 5.1).
04.4 Spesielle advarsler og passende forholdsregler for bruk
Nedsatt leverfunksjon
Pasienter med forhøyede leverenzymer over det dobbelte av normalgrensen ble ekskludert fra kontrollerte kliniske studier som evaluerte forebygging av VTE etter valgfri total hofte- eller kneutskiftningskirurgi Det er ingen behandlingserfaring i denne subpopulasjonen av pasienter, og derfor er bruk av Pradaxa ikke anbefalt i denne befolkningen.
Blødningsrisiko
Dabigatran etexilat bør brukes med forsiktighet under forhold med økt risiko for blødning og i situasjoner som involverer samtidig bruk med stoffer som endrer hemostase ved å hemme blodplateaggregering. / eller hematokrit eller blodtrykk bør be om et søk etter blødningsstedet.
Faktorer som nedsatt nyrefunksjon (30-50 ml / min CrCL), alder ≥ 75 år, lave kroppsvekt plasmanivåer av dabigatran (se pkt.4.2, 4.5 og 5.2).
Samtidig bruk av ticagrelor øker eksponeringen for dabigatran og kan føre til farmakodynamiske interaksjoner, noe som kan føre til økt blødningsrisiko (se pkt. 4.5).
Bruk av acetylsalisylsyre (ASA), klopidogrel eller ikke-steroide antiinflammatoriske legemidler (NSAIDs), samt tilstedeværelse av spiserør, gastritt eller gastroøsofageal refluks øker risikoen for gastrointestinal blødning. Administrering av PPI kan anses å forhindre gastrointestinal blødning.
Risikoen for blødning kan øke hos pasienter som samtidig behandles med selektive serotoninopptakshemmere (SSRI) eller med selektive serotonin- og noradrenalinopptakshemmere (SNRI) (se pkt. 4.5).
Nær klinisk observasjon (på jakt etter tegn på blødning eller anemi) anbefales under behandling, spesielt hvis risikofaktorene kombineres (se pkt.5.1).
Tabell 1 oppsummerer faktorene som kan øke risikoen for blødning. Se også kontraindikasjonene i avsnitt 4.3.
Tabell 1: Faktorer som kan øke risikoen for blødning
Tilstedeværelse av lesjoner, tilstander, prosedyrer og / eller behandling med legemidler (for eksempel NSAIDs, blodplatehemmende midler, SSRI og SNRI, se avsnitt 4.5), som øker risikoen for større blødninger betydelig, krever en grundig "nytte-risiko-vurdering. Pradaxa må gis bare hvis fordelen oppveier risikoen for blødning.
Pradaxa krever normalt ikke rutinemessig overvåking av koagulasjonsparametere. Vurdering av dabigatranrelatert antikoagulant effekt kan imidlertid være nyttig for å unngå overdreven høy eksponering for dabigatran i nærvær av ytterligere risikofaktorer. INR -testen er ikke pålitelig hos pasienter behandlet med Pradaxa, og det er rapportert falsk positiv INR -forhøyelse. Derfor bør ikke INR -testen utføres Fortynnet plasmatrombintid (dTT), ecarin -tid (ECT), aktivert delvis tromboplastintid (aPTT) kan gi nyttig informasjon, men tester er ikke standardiserte og resultatene bør tolkes med forsiktighet (se pkt.5.1).
Tabell 2 viser avbrudd ved koagulasjonstester ved en tid som kan være forbundet med økt risiko for blødning (se pkt.5.1).
Tabell 2: Terskelgrenseverdier ved koagulasjonstestene som kan være forbundet med økt risiko for blødning
Pasienter som utvikler akutt nyresvikt bør slutte å ta Pradaxa (se pkt. 4.3).
Dataene for vektpasienter
Når alvorlig blødning oppstår, bør behandlingen stoppes og kilden til blødningen undersøkes (se pkt. 4.9).
Legemidler som kan øke risikoen for blødning bør ikke administreres samtidig eller bør administreres med forsiktighet med Pradaxa (se pkt. 4.5).
Bruk av fibrinolytiske legemidler til behandling av akutt iskemisk slag
Bruk av fibrinolytiske legemidler til behandling av akutt iskemisk hjerneslag kan vurderes hvis pasienten har dTT, ECT eller aPTT under den øvre grensen for det normale, i henhold til det lokale referanseområdet.
Interaksjoner med P-gp-induktorer
Ved samtidig administrering av P-gp-induktorer (som rifampicin, johannesurt (Hypericum perforatum), karbamazepin eller fenytoin) kan det forventes en reduksjon i plasmakonsentrasjonen av dabigatran og bør derfor unngås (se pkt. 4.5 og 5.2).
Kirurgi og intervensjoner
Pasienter på dabigatran etexilat som gjennomgår kirurgi eller invasive inngrep har økt risiko for blødning. Derfor kan kirurgiske inngrep kreve midlertidig suspensjon av behandlingen.
Forsiktighet og overvåking av antikoagulantaktivitet anbefales når behandlingen midlertidig avbrytes på grunn av kirurgi. Clearance av dabigatran hos pasienter med nyreinsuffisiens kan ta lengre tid (se pkt. 5.2). Dette bør evalueres før hver prosedyre. I slike tilfeller koagulasjonstest (se pkt. 4.4 og 5.1) kan bidra til å avgjøre om hemostase fortsatt er svekket.
Preoperativ fase
Tabell 3 oppsummerer tilbaketrekningsreglene før invasive eller kirurgiske inngrep.
Tabell 3: Uttaksregler før invasive eller kirurgiske inngrep
Hvis det er behov for hasteaksjon, bør dabigatranetexilat suspenderes midlertidig. Operasjonen / intervensjonen bør om mulig utsettes minst til 12 timer etter siste dose. Hvis operasjonen ikke kan utsettes, kan det være økt risiko for blødning Denne blødningsrisikoen må veies opp mot det haster med kirurgi.
Spinalbedøvelse / epiduralanestesi / lumbalpunksjon
Prosedyrer som spinalbedøvelse krever normale hemostatiske funksjoner.
Risikoen for spinal eller epidural hematom kan øke ved traumatisk eller gjentatt punktering og ved langvarig bruk av epidurale katetre Etter fjerning av et kateter bør det gå minst 2 timer før den første dabigatran etexilatet administreres. Disse pasientene krever hyppig observasjon av nevrologiske tegn og symptomer på spinal eller epidural hematom.
Postoperativ fase
Administrering av dabigatranetexilat bør gjenopptas så snart som mulig etter den invasive prosedyren eller operasjonen, forutsatt at det er fastslått at den kliniske situasjonen gir mulighet for tilstrekkelig hemostase.
Pasienter med høy blødningsrisiko eller pasienter med risiko for overeksponering, spesielt pasienter med moderat nedsatt nyrefunksjon (CrCL 30-50 ml / min), bør behandles med forsiktighet (se pkt. 4.4 og 5.1).
Pasienter med høy risiko for dødelighet på grunn av kirurgi og med iboende risikofaktorer for tromboemboliske hendelser
Det er begrensede data om effekt og sikkerhet for dabigatran hos disse pasientene, og bør derfor behandles med forsiktighet.
Hoftebruddskirurgi
Det er ingen data om bruk av Pradaxa hos pasienter som gjennomgår hoftebruddskirurgi. Behandling anbefales derfor ikke.
Fargestoffer
Pradaxa harde kapsler inneholder solnedgangsgult fargestoff (E110) som kan forårsake allergiske reaksjoner.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Antikoagulantia og blodplater
Det er ingen eller begrenset erfaring med følgende behandlinger som kan øke risikoen for blødning ved samtidig bruk med Pradaxa: antikoagulantia som ufraksjonert heparin (ENF), lavmolekylær heparin (LMWH) og heparinderivater (fondaparinux, desirudin), trombolytisk medisin produkter og vitamin K -antagonister, rivaroksaban eller andre orale antikoagulantia (se pkt. 4.3) og blodplatehemmende midler som GPIIb / IIIa -reseptorantagonister, tiklopidin, prasugrel, ticagrelor, dextran og sulfinpyrazon (se pkt. 4.4).
ENF kan administreres i doser som er nødvendige for å beholde et sentralt venøst eller arterielt kateterpatent (se avsnitt 4.3).
Klopidogrel: I en fase I -studie med friske, unge mannlige frivillige, resulterte samtidig administrering av dabigatranetexilat og klopidogrel ikke i ytterligere forlengelse av kapillærblødningstiden sammenlignet med klopidogrel alene. Videre forble "AUC ?, Ss og Cmax, ss og koagulasjonstiltak for effekten av dabigatran eller inhibering av blodplateaggregering som et mål på effekten av klopidogrel" i det vesentlige uendret ved sammenligning av kombinert behandling og de respektive mono-behandlingene: Med en ladningsdose på 300 mg eller 600 mg klopidogrel, dabigatran AUC, ss og Cmax, ble ss økt med omtrent 30-40% (se pkt. 4.4).
ASA: Effekten av samtidig administrering av dabigatranetexilat og ASA på risiko for blødning ble studert hos pasienter med atrieflimmer i en fase II-studie der randomisert samtidig administrering av ASA ble brukt. Basert på en analyse av ASA. Logistisk regresjon, Samtidig administrering av ASA og dabigatranetexilat 150 mg to ganger daglig kan øke risikoen for alle typer blødninger fra henholdsvis 12% til 18% og 24% med 81 mg og 325 mg ASA (se pkt. 4.4).
NSAIDs: NSAIDs administrert som kortvirkende smertestillende midler i den perioperative perioden har vist seg ikke å være forbundet med økt blødningsrisiko kombinert med dabigatranetexilat. Kronisk bruk av NSAID økte risikoen for blødning med omtrent 50%. Med begge dabigatranetexilater og warfarin. På grunn av blødningsrisiko, spesielt med NSAIDs med eliminasjonshalveringstid> 12 timer, anbefales derfor nøye observasjon av tegn på blødning (se pkt. 4.4).
LMWH: Samtidig bruk av LMWH som enoksaparin og dabigatran eteksilat er ikke blitt spesifikt evaluert. Etter bytte fra en 3-dagers behandling med enoksaparin 40 mg administrert en gang daglig etter sc-ruten, 24 timer etter administrering av LMWH. dose av enoksaparin, eksponeringen for dabigatran var litt lavere enn etter administrering av dabigatran etexilat alene (enkelt dose på 220 mg). Større anti-FXa / FIIa-aktivitet ble observert etter administrering av dabigatranetexilat forutgående med forbehandling med enoksaparin versus behandling med dabigatran etexilate alene. Dette antas å skyldes en drivende effekt av enoksaparinbehandling og anses ikke som klinisk relevant. Resultatene av andre dabigatranrelaterte antikoagulantaktivitetstester ble ikke signifikant modifisert ved forbehandling med enoksaparin.
Interaksjoner relatert til den metabolske profilen til dabigatranetexilat og dabigatran
Dabigatranetexilat og dabigatran metaboliseres ikke av cytokrom P450 -systemet og har ingen effekt. in vitro på humane cytokrom P450 -enzymer. Interaksjoner med beslektede legemidler og dabigatran er derfor ikke forventet.
Transportørinteraksjoner
Inhibitorer av P-gp
Dabigatran etexilat er et substrat for efflux-transportøren P-gp. Samtidig administrering med P-gp-hemmere (som amiodaron, verapamil, kinidin, ketokonazol, dronedaron, klaritromycin og ticagrelor) vil sannsynligvis resultere i økte plasmakonsentrasjoner av dabigatran.
Med mindre annet er spesifikt foreskrevet, er det nødvendig med tett klinisk overvåking (ser etter tegn på blødning eller anemi) når dabigatran administreres samtidig med sterke P-gp-hemmere. En koagulasjonstest hjelper til med å identifisere pasienter med økt risiko for blødning på grunn av "økt eksponering for dabigatran (se pkt. 4.2, 4.4 og 5.1).
Følgende potente P-gp-hemmere er kontraindisert: systemisk administrerte ketokonazol, cyklosporin, itrakonazol og dronedaron (se pkt. 4.3) Samtidig behandling med takrolimus anbefales ikke. P-gp-hemmere fra svake moderate medisiner (f.eks. Amiodaron, posakonazol, kinidin, verapamil og ticagrelor) bør brukes med forsiktighet (se pkt.4.2 og 4.4).
Ketokonazol: Ketokonazol etter en enkelt oral dose på 400 mg økte totalt AUC0-∞ og Cmax for dabigatran med henholdsvis 138% og 135% og henholdsvis 153% og 149% etter flere orale doser på 400. mg ketokonazol en gang daglig. Tid til topp, terminal halveringstid og gjennomsnittlig oppholdstid ble ikke endret av ketokonazol (se pkt. 4.4) Samtidig bruk med systemisk ketokonazol er kontraindisert (se pkt. 4.3).
Dronedarone: Når dabigatranetexilat og dronedaron ble gitt samtidig, økte de totale verdiene av dabigatran AUC0-∞ og Cmax henholdsvis omtrent 2,4 ganger og 2,3 ganger (+ 136% og 125%), etter flere doser på 400. mg dronedaron bud og henholdsvis omtrent 2,1 ganger og 1,9 ganger (+ 114% og 87%), etter en enkelt dose på 400 mg Den terminale halveringstiden og renal clearance av dabigatran ble ikke påvirket av dronedaron. doser av dronedaron ble administrert 2 timer etter dabigatranetexilat, økningen i dabigatran AUC0-∞ var henholdsvis 1,3 ganger og 1,6 ganger. Samtidig behandling med dronedaron er kontraindisert.
Amiodaron: Da Pradaxa ble administrert samtidig med en enkelt oral dose på 600 mg amiodaron, var mengden og absorpsjonshastigheten for amiodaron og dets aktive metabolitt DEA i hovedsak uendret. AUC og Cmax for dabigatran økte med henholdsvis ca. 60% og 50%. Interaksjonsmekanismen er ikke fullstendig belyst. Med tanke på den lange halveringstiden for amiodaron, kan den potensielle legemiddelinteraksjonen vedvare i flere uker etter seponering av amiodaron (se pkt. 4.2 og 4.4).
Hos pasienter som behandles for å forebygge VTE etter hofte- eller kneutskifting, bør Pradaxa -dosen reduseres til 150 mg én gang daglig som 2 x 75 mg kapsler ved samtidig behandling med dabigatranetexilat og amiodaron (se pkt.4.2). Nær klinisk overvåking anbefales når dabigatranetexilat kombineres med amiodaron, spesielt når det oppstår blødning og med ekstra forsiktighet for pasienter med mild til moderat nedsatt nyrefunksjon.
Kinidin: Kinidin ble administrert i doser på 200 mg hver 2. time opp til en total dose på 1000 mg. Dabigatran etexilat ble administrert to ganger daglig i 3 påfølgende dager, på den tredje dagen med eller uten kinidin. Dabigatran AUC, ss og Cmax, ss ble i gjennomsnitt økt med henholdsvis 53% og 56% ved samtidig administrering av kinidin (se pkt. 4.2 og 4.4).
Hos pasienter som behandles for å forebygge VTE etter hofte- eller kneutskiftning, bør Pradaxa -dosen reduseres til 150 mg én gang daglig som 2 x 75 mg kapsler hvis den behandles samtidig med dabigatranetexilat og kinidin (se pkt. 4.2). Tett klinisk overvåking anbefales når dabigatranetexilat kombineres med kinidin, spesielt når det oppstår blødning og med ekstra forsiktighet for pasienter med mild til moderat nedsatt nyrefunksjon.
Verapamil: Når dabigatranetexilat (150 mg) ble gitt samtidig med oral verapamil, økte Cmax og AUC for dabigatran, men størrelsen på denne endringen varierte med administreringstidspunktet og verapamilformuleringen (se pkt. 4.2 og 4.4).
Den maksimale økningen i dabigatran-eksponering ble observert med den første dosen av en verapamilformulering med umiddelbar frigjøring, administrert en time før du tok dabigatranetexilat (økning i Cmax med omtrent 180% og i AUC med omtrent 150%). Effekten ble gradvis redusert ved administrering av en depotformulering (økning i Cmax med omtrent 90% og AUC med omtrent 70%) eller ved administrering av flere doser verapamil (økning i Cmax med omtrent 60% og økning i AUC på ca. 50%).
Derfor er det nødvendig med nøye klinisk overvåking (leting etter tegn på blødning eller anemi) når dabigatran administreres samtidig med verapamil. Hos pasienter med normal nyrefunksjon etter hofte- eller kneutskiftningskirurgi behandlet med dabigatranetexilat og verapamil samtidig, bør dosen Pradaxa reduseres til 150 mg tatt som 2 x 75 mg kapsler en gang daglig. Hos pasienter med moderat nedsatt nyrefunksjon, behandlet samtidig med dabigatranetexilat og verapamil, bør en dosereduksjon av Pradaxa til 75 mg daglig vurderes (se pkt. 4.2 og 4.4). Nær klinisk overvåking anbefales når dabigatranetexilat kombineres med verapamil, spesielt når blødning oppstår og med ekstra forsiktighet ved pasienter med mild til moderat nedsatt nyrefunksjon.
Det ble ikke observert noen signifikant interaksjon da verapamil ble administrert 2 timer etter inntak av dabigatranetexilat (ca. 10% økning i Cmax og ca. 20% økning i AUC). Dette forklares med fullstendig absorpsjon av dabigatran etter 2 timer (se pkt. 4.4).
Klaritromycin: Når klaritromycin (500 mg to ganger daglig) ble gitt i kombinasjon med dabigatranetexilat hos friske frivillige, ble en økning i AUC på omtrent 19% og Cmax på omtrent 15% observert uten effekt på den kliniske sikkerheten, men hos pasienter som fikk dabigatran, kan en klinisk signifikant interaksjon ikke utelukkes når den kombineres med klaritromycin. Derfor bør det overvåkes nøye når dabigatranetexilat kombineres med klaritromycin og spesielt ved blødning, spesielt hos pasienter med mild til moderat nedsatt nyrefunksjon.
Ticagrelor: Når en enkelt dose på 75 mg dabigatranetexilat ble administrert samtidig med en startdose på 180 mg ticagrelor, økte dabigatran AUC og Cmax henholdsvis 1,73 og 1,95 ganger (+73 % og 95 %). Etter flere doser på 90 mg ticagrelor to ganger øker eksponeringen for dabigatran 1,56 og 1,46 ganger (+ 56% og 46%) for henholdsvis AUC og Cmax.
Samtidig administrering av en startdose på 180 mg ticagrelor og 110 mg dabigatranetexilat (ved steady state) økte AUC ?, Ss og Cmax, ss av dabigatran med henholdsvis 1,49 ganger og 1,65 ganger ( + 49% og 65) %), sammenlignet med administrering av dabigatranetexilat alene. Når en innledende dose på 180 mg ticagrelor ble administrert 2 timer etter administrering av dabigatranetexilat 110 mg (steady state), ble økningen i dabigatran AUC ?, Ss og Cmax, ss redusert til henholdsvis 1,27 ganger og 1,23 ganger (+ 27% og 23%), sammenlignet med administrering av dabigatranetexilat alene. Denne forskjøvede administrasjonen er den som anbefales for å starte ticagrelor med en startdose.
Samtidig administrering av 90 mg ticagrelor BID (vedlikeholdsdose) med 110 mg dabigatranetexilat økte den justerte AUCa, Ss og Cmax, ss av dabigatran med henholdsvis 1,26 ganger og 1,29 ganger sammenlignet med administrering av dabigatran etexilat alene.
Følgende potente P-gp-hemmere har ikke blitt studert klinisk, men basert på dataene i vitro en effekt som ligner på ketokonazol forventes:
Itrakonazol og cyklosporin, som er kontraindisert (se pkt. 4.3).
In vitro har takrolimus vist seg å ha en lignende hemmende effekt på P-gp som den som ble observert for itrakonazol og cyklosporin. Dabigatran etexilat er ikke klinisk studert i kombinasjon med takrolimus. Imidlertid tyder de begrensede kliniske dataene som er tilgjengelige med et annet P-gp-substrat (everolimus) på at inhiberingen av P-gp med takrolimus er svakere enn den som er observert med potente P-gp-hemmere. Basert på disse dataene anbefales ikke behandling samtidig med takrolimus .
Posakonazol hemmer også delvis P-gp, men har ikke blitt studert klinisk. Samtidig administrering av Pradaxa og posakonazol bør gjøres med forsiktighet.
Induktorer av P-gp
Samtidig administrering av en P-gp-induktor (som rifampicin, johannesurt (Hypericum perforatum), karbamazepin eller fenytoin) kan redusere dabigatran-konsentrasjonen og bør unngås (se pkt. 4.4 og 5.2).
Rifampicin: Pre-administrering av induktoren rifampicin i en dose på 600 mg én gang daglig i 7 dager reduserte den totale dabigatran-toppen og total eksponering med henholdsvis 65,5% og 67%. Induseringseffekten ble redusert, noe som resulterte i dabigatran -eksponering nær referanseverdien innen den syvende dagen etter avsluttet behandling med rifampicin. Ingen økning i biotilgjengeligheten ble observert etter ytterligere 7 dager.
Andre legemidler som påvirker P-gp
Proteasehemmere som ritonavir og dets kombinasjoner med andre proteasehemmere påvirker P-gp (både som hemmere og som indusere). Siden de ikke er undersøkt, anbefales de ikke for samtidig behandling med Pradaxa.
Substrat av P-gp
Digoksin: I en studie som involverte 24 friske pasienter, da Pradaxa ble administrert samtidig med digoksin, ble det verken observert endringer i digoksin eller signifikante kliniske endringer i eksponering for dabigatran.
Samtidig bruk av selektive serotonin gjenopptakshemmere (SSRI) eller med selektive serotonin og noradrenalin gjenopptakshemmere (SNRI)
SSRI og SNRI økte risikoen for blødning i alle behandlingsgrupper i RE-LY-studien.
mage -pH
Pantoprazol: Da Pradaxa ble gitt i kombinasjon med pantoprazol, ble det observert omtrent 30% reduksjon i området under plasmakonsentrasjonstidskurven for dabigatran. Pantoprazol og andre protonpumpehemmere (PPI) ble observert administrert med Pradaxa i kliniske studier og Samtidig behandling med PPI syntes ikke å redusere effekten av Pradaxa.
Ranitidine: Administrering av ranitidin med Pradaxa har ingen klinisk relevant effekt på absorpsjonen av dabigatran.
04.6 Graviditet og amming
Kvinner i fertil alder / prevensjon for menn og kvinner
Kvinner i fertil alder bør unngå å bli gravide mens de blir behandlet med dabigatranetexilat.
Svangerskap
Det er en begrenset mengde data tilgjengelig fra bruk av dabigatranetexilat hos gravide kvinner.
Dyrestudier har vist reproduksjonstoksisitet (se pkt. 5.3). Den potensielle risikoen for mennesker er ukjent.
Pradaxa skal ikke brukes under graviditet med mindre det er helt nødvendig.
Foringstid
Det er ingen kliniske data om effekten av dabigatran på ammende spedbarn.
Amming bør avbrytes under behandling med Pradaxa.
Fruktbarhet
Ingen data er tilgjengelige hos mennesker.
I dyreforsøk ble det observert en effekt på kvinnelig fruktbarhet i form av redusert implantasjon og økt tap før implantasjon ved en dose på 70 mg / kg (plasmaeksponering 5 ganger den hos pasienter). Ingen andre effekter på kvinnelig fruktbarhet ble observert. Det ble ikke funnet noen innflytelse på mannlig fruktbarhet. Ved maternelt toksiske doser (plasmaeksponering 5 til 10 ganger høyere enn hos pasienter) ble det observert redusert føtal kroppsvekt og embryoføtal levedyktighet med økte fosterendringer hos rotter og kaniner. I studier før og etter fødselen ble det observert økt fosterdødelighet ved doser som var toksiske for mødrene (en dose som tilsvarer 4 ganger høyere plasmaeksponering enn hos pasienter).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Pradaxa har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner.
04.8 Bivirkninger
Oppsummering av sikkerhetsprofilen
Totalt 10.795 pasienter ble behandlet i 6 aktivt kontrollerte VTE -forebyggingsstudier med minst en styrke av studielegemidlet. Av disse 6 684 pasientene ble behandlet med 150 mg eller 220 mg Pradaxa per dag.
De hyppigst rapporterte bivirkningene er blødning som oppstod hos totalt omtrent 14% av pasientene; hyppigheten av større blødninger (inkludert sårblødning) er mindre enn 2%.
Selv om det sjelden forekommer i kliniske studier, kan store eller alvorlige blødningshendelser oppstå som, uavhengig av beliggenhet, kan være invalidiserende, livstruende eller til og med død.
Sammendragstabell over bivirkninger
Tabell 4 viser bivirkninger sortert etter systemorganklasse (SOC) og frekvens ved bruk av følgende konvensjon: svært vanlig (≥ 1/10); vanlig (≥ 1/100,
Tabell 4: Bivirkninger
Blør
Tabell 5 rapporterer antall (%) pasienter som opplever uønskede blødningsreaksjoner i løpet av den VTE -forebyggende behandlingsperioden i de to sentrale kliniske studiene, i henhold til dose.
Tabell 5: Antall (%) pasienter som opplever bivirkninger
Definisjonene av bivirkninger av større blødninger i RE-NOVATE- og RE-MODEL-studiene var som følger:
• dødelig blødning
• klinisk manifest blødning assosiert med et fall i hemoglobin ≥ 20 g / l (tilsvarende 1,24 mmol / l) begge over forventet
• klinisk manifest blødning som er over forventet og krever transfusjon av ≥ 2 enheter erytrocytter eller fullblod som er over forventet
• symptomatisk retroperitoneal, intrakranial, intraokulær eller intraspinal blødning
• blødning som krevde seponering av behandlingen
• blødning som har krevd en ny operasjon.
Objektiv testing var nødvendig for retroperitoneal blødning (ultralydsskanning eller computertomografi (CT)) og intraspinal blødning (CT eller magnetisk resonansavbildning).
Rapportering av mistenkte bivirkninger
Rapportering av mistenkte bivirkninger som oppstår etter godkjenning av legemidlet er viktig, da det muliggjør kontinuerlig overvåking av nytte / risiko -balansen for legemidlet. Helsepersonell blir bedt om å rapportere alle mistenkte bivirkninger via det nasjonale rapporteringssystemet. "Adresse https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
Doser av dabigatranetexilat høyere enn anbefalt utsetter pasienten for økt risiko for blødning.
Hvis det er mistanke om overdosering, kan koagulasjonstester hjelpe til med å bestemme risikoen for blødning (se pkt. 4.4 og 5.1). Kvantitativ kalibrert dTT -test eller gjentatte dTT -målinger tillater forutsigelse av når visse nivåer av dabigatran vil nås (se pkt. 5.1) selv om andre tiltak er iverksatt f.eks. dialyse.
Overdreven antikoagulantaktivitet kan kreve seponering av Pradaxa -behandlingen. Det er ingen spesifikk motgift for dabigatran. Ved blødningskomplikasjoner bør behandlingen avbrytes og blødningsårsaken undersøkes Siden dabigatran hovedsakelig utskilles av nyrene, bør tilstrekkelig diurese opprettholdes. Passende støttende behandling som kirurgisk hemostase og gjenoppretting av blodvolum bør utføres etter legens skjønn.
Konsentrater av det aktiverte protrombinkomplekset (f.eks. FEIBA) eller rekombinant faktor VIIa eller konsentrater av koagulasjonsfaktorer II, IX og X kan vurderes. Det er noen eksperimentelle bevis som støtter disse stoffenes rolle i å motvirke den antikoagulerende effekten av dabigatran, men data om deres nytte i kliniske omgivelser og også om mulig risiko for rebound tromboemboli er svært begrenset. Koagulasjonstester kan bli upålitelige. av stoffene som står i kontrast til antikoagulerende effekt. Forsiktighet bør utvises ved tolkning av resultatene av disse testene.Administrering av blodplatekonsentrater bør også vurderes hvis det oppstår trombocytopeni eller langtidsvirkende blodplater. Alle symptomatiske behandlinger bør administreres i henhold til legens vurdering.
Avhengig av lokal tilgjengelighet, ved større blødninger, bør det vurderes om det er hensiktsmessig å konsultere en koagulasjonsekspert.
Siden proteinbinding er lav, kan dabigatran dialyseres; den kliniske erfaringen som viser bruken av denne tilnærmingen i kliniske studier er begrenset (se pkt. 5.2).
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: antitrombotika, direkte trombinhemmere.
ATC -kode: B01AE07.
Virkningsmekanismen
Dabigatran eteksilat er et lite molekylært prodrug som ikke utøver farmakologisk aktivitet. Etter oral administrering absorberes dabigatranetexilat raskt og omdannes til dabigatran ved esterasekatalysert hydrolyse i plasma og lever. Dabigatran er en potent direkte, konkurransedyktig, reversibel trombinhemmer og er det viktigste aktive stoffet som finnes i plasma.
Siden trombin (serinprotease) tillater omdannelse av fibrinogen til fibrin i koagulasjonskaskaden, forhindrer dets inhibering trombedannelse. Dabigatran hemmer fritt trombin, fibrinbundet trombin og trombinindusert blodplateaggregering.
Farmakodynamiske effekter
Studier utført på dyr in-vivo Og ex vivo demonstrert antitrombotisk effekt og antikoagulerende aktivitet av dabigatran etter intravenøs administrering og av dabigatran etexilat etter oral administrering i forskjellige dyremodeller av trombose.
Det er en klar sammenheng mellom plasmakonsentrasjonen av dabigatran og størrelsen på antikoagulerende effekt, basert på data fra fase II -studier. Dabigatran forlenger trombintiden (TT), ECT og aPTT.
Den trombintid (dTT) kalibrerte analysen for dabigatran på fortynnet plasma gir et estimat av plasmakonsentrasjonen av dabigatran som kan sammenlignes med de forventede plasmakonsentrasjonene av dabigatran.
ECT kan gi et direkte mål på aktiviteten til direkte trombinhemmere.
APTT -testen er mye brukt og gir en omtrentlig indikasjon på intensiteten av den antikoagulerende effekten oppnådd med dabigatran, men aPTT -testen er preget av begrenset følsomhet og er ikke indikert for den nøyaktige kvantifiseringen av antikoagulerende effekt, spesielt ved høye plasmakonsentrasjoner. . av dabigatran. Forhøyede aPTT -verdier bør tolkes med forsiktighet.
Generelt kan det argumenteres for at disse antikoagulantaktivitetsmålingene gjenspeiler dabigatran -nivåer og kan gi veiledning for vurdering av blødningsrisiko, det vil si å overskride 90 -prosentilgrensen for dabigatranivåer ved lavtid eller målt aPTT. Ved lavtid anses å være assosiert med økt risiko for blødning.
Ved steady state (etter 3 dager) var det geometriske gjennomsnittet av plasmakonsentrasjonen av dabigatran ved topptid målt ca. 2 timer etter administrering av 220 mg dabigatranetexilat 70,8 ng / ml, med et område på 35, 2-162 ng / ml ( 25. -75. Persentil).
Det geometriske gjennomsnittet av dabigatran-konsentrasjon ved lavtid, målt ved slutten av doseringsperioden (dvs. 24 timer etter en 220 mg dose dabigatran), gjennomsnittlig 22,0 ng / ml, med et område på 13, 0-35,7 ng / ml ( 25.-75. persentil).
Hos pasienter behandlet for forebygging av VTE etter hofte- eller kneutskifting med 220 mg dabigatranetexilat en gang daglig,
• den 90. persentilen av plasmakonsentrasjoner av dabigatran, målt ved lavtid (20-28 timer etter forrige dose), var 67 ng / ml (se pkt. 4.4 og 4.9),
• den 90. persentilen av aPTT ved lavtid (20-28 timer etter forrige dose) var 51 sekunder, eller 1,3 ganger den øvre grensen for det normale.
ECT ble ikke målt hos pasienter behandlet for forebygging av VTE etter hofte- eller kneutskifting med 220 mg dabigatranetexilat en gang daglig.
Klinisk effekt og sikkerhet
Etnisk opprinnelse
Ingen relevante inter-etniske forskjeller ble observert mellom kaukasiske, afroamerikanske, latinamerikanske, japanske eller kinesiske pasienter.
Kliniske studier ved profylakse av venøs tromboembolisme (VTE) etter større leddskifteoperasjoner
I 2 store, randomiserte, parallellgruppe, dobbeltblindede, dosebekreftende studier ble pasienter planlagt for større ortopedisk kirurgi (en for kneutskiftningskirurgi og en for hofteutskiftningskirurgi) behandlet med Pradaxa 75 mg eller 110 mg innen 1- 4 timer etter operasjonen og derfor med 150 eller 220 mg daglig, hemostase ble evaluert normalt eller med 40 mg enoksaparin dagen før operasjonen og derfor daglig.
I RE-MODEL-studien (kneutskiftning) var behandlingstiden 6-10 dager og i RE-NOVATE-studien (hofteutskiftning) var den 28-35 dager. Totalt 2.076 (hofteutskiftning) ble behandlet. Kne) og 3494 (hofteutskiftning) pasienter.
Kombinasjonen av alle episoder av VTE (som inkluderte PE, proksimal og distal DVT, både symptomatisk og asymptomatisk påvist med rutinemessig venografi) og dødelighet av alle årsaker var de primære endepunktene for begge studiene.
Kombinasjonen av alle de store episodene av VTE (som inkluderte PE, både symptomatisk og asymptomatisk proksimal DVT påvist med rutinemessig venografi) og VTE-relatert dødelighet var et sekundært endepunkt som ble ansett å ha større klinisk relevans.
Resultatene fra begge studiene viste at den antitrombotiske effekten av Pradaxa 220 mg og 150 mg var statistisk ikke dårligere enn enoksaparin for total VTE og dødelighet av alle årsaker. Den estimerte forekomsten av større episoder av VTE er VTE-relatert dødelighet for Dosen på 150 mg var litt verre enn for enoksaparin (tabell 6.) Det ble sett bedre resultater med dosen på 220 mg, der den estimerte forekomsten av større VTE -episoder var litt bedre enn for enoksaparin (tabell 6).
Kliniske studier ble utført på en pasientpopulasjon med en gjennomsnittsalder på> 65 år.
Det ble ikke funnet forskjeller i effekt og sikkerhet mellom menn og kvinner i kliniske fase 3 -studier.
Av pasientpopulasjonen som deltok i RE-MODEL og RE-NOVATE-studiene (5539 behandlede pasienter) led 51% av samtidig hypertensjon, 9% av samtidig diabetes, 9% av koronararteriesykdom og 20% hadde en historie med venøs insuffisiens . Ingen av disse tilstandene har vist seg å forstyrre effekten av dabigatran på forebygging av VTE eller blødningsfrekvensen.
Data for hoved-VTE- og VTE-relatert dødelighet-endepunkt var homogene med hensyn til det primære effekt-endepunktet og er vist i tabell 6.
Sluttpunktsdata for total VTE og alle dødsårsaker er vist i tabell 7.
Data for endepunktene for blødning som anses å være store, er oppført i tabell 8 nedenfor.
Tabell 6: Analyse av større VTE- og VTE-relatert dødelighet i behandlingsperioden i RE-MODELL og RE-NOVATE ortopediske kirurgiske studier
Tabell 7: Analyse av total VTE og dødelighet av alle årsaker i behandlingsperioden for RE-NOVATE og RE-MODEL ortopediske kirurgi-studier
Tabell 8: Store blødningsepisoder (ESM) etter behandling i individuelle RE-MODELL- og RE-NOVATE-studier
Pediatrisk populasjon
Det europeiske legemiddelkontoret (European Medicines Agency) har frafalt forpliktelsen til å levere resultatene av studier med Pradaxa i alle undergrupper av den pediatriske populasjonen for forebygging av tromboemboliske episoder i den autoriserte indikasjonen (se pkt. 4.2 for informasjon om pediatrisk bruk).
Kliniske studier for forebygging av tromboemboli hos pasienter med hjerteventilproteser
En fase II -studie evaluerte dabigatranetexilat og warfarin hos totalt 252 pasienter som gjennomgikk delvis nylig mekanisk ventiloperasjon (dvs. registrert under sykehusinnleggelse) og delvis mekanisk hjerteventilkirurgi. I mer enn tre måneder. Flere tromboemboliske hendelser (hovedsakelig hjerneslag og symptomatisk / asymptomatisk ventiltrombose) og flere blødningshendelser ble observert med dabigatranetexilat enn med warfarin. Hos umiddelbare postoperative pasienter manifesterte større blødninger seg hovedsakelig som hemoragisk perikardial utstrømning, spesielt hos pasienter som startet dabigatranetexilat kort tid (dvs. på dag 3) etter hjerteklaffprotesekirurgi (se avsnitt 4.3).
05.2 Farmakokinetiske egenskaper
Etter oral administrering blir dabigatranetexilat raskt og fullstendig omdannet til dabigatran, som er den aktive formen i plasma. Spaltning av prodrug-dabigatranetexilatet ved esterasekatalysert hydrolyse til virkestoffet dabigatran er den dominerende metabolske reaksjonen. Den absolutte biotilgjengeligheten av dabigatran etter oral administrering av Pradaxa er omtrent 6,5%.
Etter oral administrering av Pradaxa til friske frivillige, er den farmakokinetiske profilen til dabigatran i plasma preget av en rask økning i plasmakonsentrasjoner med Cmax nådd 0,5 - 2,0 timer etter dosering.
Absorpsjon
En studie som evaluerte den postoperative absorpsjonen av dabigatranetexilat, 1-3 timer etter operasjonen, viste en relativt langsom absorpsjon sammenlignet med den som ble sett hos friske frivillige, og demonstrerte en plasmakonsentrasjonstidsprofil uten høye plasmakonsentrasjoner. Høyeste plasmakonsentrasjon oppnås 6 timer etter administrering i en postoperativ periode på grunn av faktorer som anestesi, tarmparese og kirurgiske effekter, uavhengig av den orale formuleringen av legemidlet. I en videre studie ble det vist at langsom og forsinket absorpsjon vanligvis bare skjer på operasjonsdagen.I dagene etter er absorpsjonen av dabigatran rask med maksimal plasmakonsentrasjon oppnådd 2 timer etter legemiddeladministrasjon.
Mat endrer ikke biotilgjengeligheten til dabigatranetexilat, men forsinker tiden for å nå maksimal plasmakonsentrasjon med 2 timer.
Når pelletene tas uten (hydroksypropylmetylcellulose) HPMC -kapsel, kan den orale biotilgjengeligheten øke med 75% sammenlignet med referanseformuleringen med kapsel. Derfor må integriteten til HPMC -kapsler alltid bevares under klinisk bruk for å unngå en utilsiktet økning i biotilgjengeligheten av dabigatranetexilat. Pasienter bør derfor rådes til ikke å åpne kapslene og ikke ta innholdet alene (f.eks. Drysset på mat eller hellet i en drink) (se pkt.4.2).
Fordeling
Lav konsentrasjon uavhengig binding (34-35%) av dabigatran til humane plasmaproteiner ble observert. Distribusjonsvolumet for dabigatran på 60-70 l overstiger volumet av totale kroppsvæsker som indikerer moderat vevsfordeling av dabigatran.
Cmax og areal under plasmakonsentrasjon-tid-kurven var doseproporsjonal Plasmakonsentrasjoner av dabigatran viste en bi-eksponensiell nedgang med en gjennomsnittlig terminal halveringstid på 11 timer hos friske, eldre personer. Etter flere doser ble det observert en "terminal halveringstid på ca. 12-14 timer". Halveringstiden var uavhengig av dose. Halveringstiden forlenges hvis nyrefunksjonen er svekket som vist i tabell 9.
Biotransformasjon
Metabolisme og utskillelse av dabigatran ble studert etter administrering av en enkelt intravenøs dose radioaktivt dabigatran til friske mannlige individer. Etter en intravenøs dose ble dabigatran-avledet radioaktivitet hovedsakelig eliminert i urinen (85%). Fekal utskillelse ble estimert til å være 6% av den administrerte dosen. Total radioaktivitetsgjenoppretting varierte fra 88 til 94% av den administrerte dosen innen 168 timer etter administrering.
Dabigatran er underlagt konjugering med dannelsen av farmakologisk aktive acylglucuronider. Det er fire posisjonelle isomerer 1-O, 2-O, 3-O, 4-O av acylglucuronides som hver er estimert til å være mindre enn 10% av den totale dabigatran i plasma. Spor av andre metabolitter kan bare påvises ved svært sensitive analysemetoder. Dabigatran elimineres hovedsakelig uendret i urinen med en hastighet på omtrent 100 ml / min som tilsvarer glomerulær filtreringshastighet.
Spesielle populasjoner
Nyresvikt
I fase I-studier er eksponering (AUC) for dabigatran etter oral administrering av Pradaxa omtrent 2,7 ganger høyere hos frivillige med moderat nedsatt nyrefunksjon (CrCL mellom 30 og 50 ml / min) enn hos personer uten nedsatt nyrefunksjon.
Hos et lite antall frivillige med alvorlig nyreinsuffisiens (CrCL 10 - 30 ml / min) var eksponeringen for dabigatran (AUC) omtrent 6 ganger høyere og halveringstiden omtrent 2 ganger lengre enn den som ble observert i en populasjon uten nyreinsuffisiens. (Se avsnitt 4.2, 4.3 og 4.4).
Tabell 9: Halveringstid for totalt dabigatran hos friske personer og personer med nedsatt nyrefunksjon.
Clearance av dabigatran ved hemodialyse ble undersøkt hos 7 pasienter med kronisk nyresvikt i siste fase (ESRD) uten atrieflimmer. Dialyse ble utført ved en dialysatstrømningshastighet på 700 ml / min, i en varighet på fire timer, og med en blodstrømningshastighet på både 200 ml / min og 350-390 ml / min. Dette resulterte i en fjerning av henholdsvis 50% til 60% av dabigatran -konsentrasjonene. Mengden stoff som fjernes ved dialyse er proporsjonal med blodstrømmen opp til 300 ml / min. Antikoagulantaktiviteten til dabigatran ble redusert med synkende plasmakonsentrasjoner, og det farmakokinetiske / farmakodynamiske forholdet ble ikke endret ved prosedyren.
Eldre pasienter
Spesifikke fase I farmakokinetiske studier utført hos eldre personer viste en økning i AUC på 40 til 60% og mer enn 25% i C sammenlignet med unge personer.
Effekten av alder på eksponering av dabigatran ble bekreftet i RE-LY-studien med en høyere nedbunnskonsentrasjon på omtrent 31% hos personer ≥ 75 år og med en lavere lavkonsentrasjon på omtrent 22% hos personer i alder
Nedsatt leverfunksjon
Det ble ikke funnet noen endring av dabigatran -eksponering hos 12 personer med moderat nedsatt leverfunksjon (Child Pugh B) sammenlignet med 12 kontrollpersoner (se pkt. 4.2 og 4.4).
Kroppsvekt
Dabigatran -konsentrasjonene på lavtidstid var omtrent 20% lavere hos pasienter med kroppsvekt> 100 kg sammenlignet med pasienter med kroppsvekt mellom 50 og 100 kg. De fleste pasientene (80,8%) hadde kroppsvekt ≥ 50 kg og
Type
Aktiv substanseksponering i primære VTE -forebyggingsstudier var omtrent 40% til 50% høyere hos kvinnelige pasienter, og ingen dosejustering anbefales.
etnisk bakgrunn
Ingen relevante inter-etniske forskjeller ble observert mellom kaukasiere, afroamerikanere, latinamerikanere, japanere eller kinesere angående farmakokinetikken og farmakodynamikken til dabigatran.
Farmakokinetiske interaksjoner
Pro-drug dabigatran etexilat er et substrat for efflux-transportøren P-gp, men ikke dabigatran. Av denne grunn, samtidig bruk med hemmere av P-gp-transportøren (amiodaron, verapamil, klaritromycin, kinidin, dronedaron, ticagrelor og ketokonazol) og med induktorer (rifampicin) (se pkt. 4.2, 4.4 og 4.5).
Interaksjonsstudiene in vitro viste ingen inhibering eller induksjon av de viktigste cytokrom P450 isoenzymer. Dette ble bekreftet av in vivo-studier utført på friske frivillige, der det ikke ble vist interaksjon mellom denne behandlingen og følgende virkestoffer: atorvastatin (CYP3A4), digoksin (interaksjon med transportøren P-gp) og diklofenak (CYP2C9).
05.3 Prekliniske sikkerhetsdata
Data fra ikke-kliniske studier viser ingen spesiell fare for mennesker basert på konvensjonelle studier av sikkerhetsfarmakologi, toksisitet ved gjentatt dosering og gentoksisitet.
Effekter observert i toksisitetsstudier ved gjentatt dosering skyldtes den forsterkede farmakodynamiske effekten av dabigatran.
En effekt på kvinnelig fruktbarhet i form av redusert implantasjon og økt tap før implantasjon ble observert ved doser på 70 mg / kg (5 ganger plasmaeksponeringsnivået hos pasienter). Ved maternelt toksiske doser (5 til 10 ganger plasmaeksponeringsnivået hos pasienter) ble det observert en nedgang i føtal kroppsvekt og levedyktighet med en økning i fosterendringer hos rotter og kaniner. I en pre- og postnatal studie ble det observert en økning i fosterdødelighet ved maternelt toksiske doser (dose tilsvarende et plasmaeksponeringsnivå 4 ganger høyere enn det som ble observert hos pasienter).
I livslang toksisitetsstudier hos rotter og mus var det ingen tegn på et tumorigenisk potensial for dabigatran opp til en maksimal dose på 200 mg / kg.
Dabigatran, det aktive molekylet til dabigatranetexilatmesylat, er vedvarende i miljøet.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Kapselinnhold
• Vinsyre
• Arabisk tyggegummi
• Hypromellose
• Dimetikon 350
• Talkum
• Hydroksypropylcellulose
Kapsel
• Carrageenan
• Kaliumklorid
• Titandioksid
• Indigo karmin (E132)
• Gul solnedgang (E110)
• Hypromellose
Svart blekk for utskrift
• Shellac
• Svart jernoksid (E172)
• Kaliumhydroksyd
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
Blister og flaske: 3 år.
Når flasken er åpnet, bør legemidlet brukes innen 4 måneder.
06.4 Spesielle forholdsregler for lagring
Blister
Oppbevares i originalpakningen for å beskytte mot fuktighet.
Flaske
Oppbevares i originalpakningen for å beskytte mot fuktighet. Hold flasken tett lukket.
06.5 Emballasje og innhold i pakningen
Pakninger som inneholder 10 x 1, 30 x 1 eller 60 x 1 harde kapsler i perforerte endose blisterpakninger. I tillegg pakninger som inneholder 6 hvite aluminiumsblisterbånd, delbare med enhetsdose (60 x 1). Blisteren består av et øvre lag av aluminium belagt med polyvinylklorid-polyvinylacetat-kopolymerer (PVCAC-akrylater) i kontakt med produktet og et nedre lag av aluminium belagt med polyvinylklorid (PVC) i kontakt med produktet.
Polypropylenflaske med skruehett som inneholder 60 harde kapsler.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Når du bruker Pradaxa pakket i blisterpakninger, bør du følge følgende instruksjoner:
• Den harde kapsel må fjernes fra blisterpakningen ved å løfte aluminiumsfolien på baksiden.
• Den harde kapslen må ikke skyves gjennom blisterpakningen.
• Aluminiumsfolien på blisterpakningen bør bare løftes når en hard kapsel er nødvendig.
Når du bruker kapslene i flasker, bør du følge følgende instruksjoner:
• Flasken åpnes ved å trykke og vri lokket.
Ubrukte medisiner og avfall fra denne medisinen må kastes i henhold til lokale forskrifter.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
Boehringer Ingelheim International GmbH
Binger Str.173
D-55216 Ingelheim am Rhein
Tyskland
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
EU/1/08/442/001
038451011
EU/1/08/442/002
038451023
EU/1/08/442/003
038451035
EU/1/08/442/004
038451047
EU/1/08/442/017
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Dato for første godkjenning: 18. mars 2008
Dato for siste fornyelse: 17. januar 2013
10.0 DATO FOR REVISJON AV TEKSTEN
18. desember 2014