Aktive ingredienser: Tolterodina
Tolterodine 2 mg harde kapsler
Tolterodine 4 mg harde depotkapsler
Hvorfor brukes Tolterodina - Generisk legemiddel? Hva er den til?
Virkestoffet i Tolterodine er tolterodin. Tolterodin tilhører en klasse med legemidler som kalles antimuskarinika.
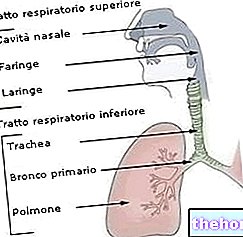
Tolterodin brukes til å behandle symptomene på overaktiv blæresyndrom. Hvis du har en overaktiv blære, vil det skje med deg
- ikke være i stand til å kontrollere utslippet av urin
- måtte skynde meg på do uten forvarsel og / eller gå på do ofte.
Kontraindikasjoner Når Tolterodina ikke skal brukes - Generisk legemiddel
Ta ikke Tolterodine hvis:
- du er allergisk (overfølsom) overfor tolterodin eller noen av de andre innholdsstoffene i Tolterodine (se avsnitt 6 for en liste over hjelpestoffer)
- klarer ikke å urinere (urinretensjon)
- har ukontrollert akutt vinkelglaukom (høyt trykk i øyet med synstap som ikke behandles riktig)
- lider av myasthenia gravis (overdreven muskelsvakhet)
- lider av alvorlig ulcerøs kolitt (sårdannelse og betennelse i tykktarmen)
- lider av alvorlig giftig megakolon (akutt utvidelse av tykktarmen).
Forholdsregler for bruk Det du trenger å vite før du bruker Tolterodina - Generisk legemiddel
Vær spesielt forsiktig med Tolterodina DOC:
- hvis du har problemer med å tisse og / eller har redusert urinstrøm
- hvis du har en gastrointestinal sykdom som påvirker passering og / eller fordøyelse av mat
- hvis du har nyreproblemer (nyresvikt).
- hvis du har leverproblemer
- hvis du har en nevrologisk sykdom som påvirker blodtrykk, tarm eller seksuell funksjon (noen nevropati i det autonome nervesystemet)
- hvis du har en "hiatus brokk" (en "brokk i et abdominal organ)
- hvis du noen ganger har redusert tarmmobilitet eller lider av alvorlig forstoppelse (redusert gastrointestinal mobilitet)
- hvis du har et hjerteproblem som:
- unormal hjertesporing (EKG)
- langsom puls (bradykardi)
- relevante eksisterende hjertelidelser som: kardiomyopati (svak hjertemuskulatur), myokardiskemi (redusert blodstrøm til hjertet), arytmi (uregelmessig hjerterytme) og hjertesvikt
- hvis du har unormalt lave kaliumnivåer (hypokalemi), kalsium (hypokalsemi) eller magnesium (hypomagnesemi) i blodet.
Inneholder omtrent 67,2 mg laktose (33,6 mg glukose og 33,6 mg galaktose) per dose. Dette må tas i betraktning hos pasienter med diabetes mellitus.
Dette legemidlet inneholder 0,00404 mmol (eller 0,092988 mg) natrium per dose. Dette bør tas i betraktning hos pasienter på et kontrollert natriumdiett.
Rådfør deg med lege eller apotek før du bruker Tolterodine hvis du tror at noe av dette gjelder deg.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Tolterodine - Generisk legemiddel
Fortell legen din dersom du bruker eller nylig har brukt andre legemidler, også reseptfrie.
Tolterodin, virkestoffet i Tolterodine, kan samhandle med andre medisiner.
Bruk av tolterodin anbefales ikke med:
- noen antibiotika (inneholder f.eks. erytromycin, klaritromycin)
- medisiner som brukes til å behandle soppinfeksjoner (som inneholder f.eks. ketokonazol, itrakonazol)
- medisiner som brukes til å behandle hiv.
Tolterodin bør brukes med forsiktighet sammen med:
- legemidler som påvirker matovergangen (som inneholder f.eks. metoklopramid og cisaprid)
- medisiner for behandling av uregelmessig hjerterytme (inneholdende f.eks. amiodaron, sotalol, kinidin, prokainamid, andre medisiner med virkningsmekanisme som ligner Tolterodins (antimuskarinske egenskaper) eller medisiner med motsatt virkningsmekanisme for Tolterodine (kolinerge egenskaper) Redusert gastrisk mobilitet forårsaket antimuskarinika kan påvirke absorpsjonen av andre legemidler. Spør legen din hvis du er usikker.
Å ta Tolterodine sammen med mat og drikke
Tolterodin kan tas før, under og etter et måltid.
Advarsler Det er viktig å vite at:
Graviditet og amming
Svangerskap
Du bør ikke bruke Tolterodine når du er gravid. Fortell legen din umiddelbart hvis du er gravid, tror du er gravid eller planlegger å bli gravid.
Foringstid
Det er ikke kjent om tolterodin, virkestoffet i Tolterodine, skilles ut i morsmelk. Amming mens du bruker Tolterodine anbefales ikke.
Rådfør deg med lege eller apotek før du tar medisiner.
Kjøring og bruk av maskiner
Tolterodin kan få deg til å føle deg svimmel, sliten eller forstyrret syn. Hvis dette skjer med deg, må du ikke kjøre kjøretøy eller bruke maskiner.
Viktig informasjon om noen av innholdsstoffene i Tolterodine
Dette legemidlet inneholder laktose. Hvis legen din har fortalt deg at du ikke tåler noen sukkerarter, må du kontakte legen din før du tar dette legemidlet.
Dosering og bruksmåte Hvordan bruke Tolterodina - Generisk legemiddel: Dosering
Dosering:
Ta alltid Tolterodine Accord nøyaktig slik legen din har fortalt deg. Rådfør deg med lege eller apotek hvis du er usikker.
De harde depottabletter er kun til oral bruk og skal svelges hele.
Ikke tygge kapslene.
Voksne:
Den vanlige dosen er en kapsel på 4 mg depottabletter, hard per dag.
Pasienter med lever- eller nyreproblemer:
Hos pasienter med lever- eller nyreproblemer kan legen redusere dosen til 2 mg Tolterodine daglig.
Barn:
Tolterodin er ikke anbefalt for barn.
Dersom du har glemt å ta Tolterodine
Hvis du glemmer å ta en dose til vanlig tid, ta den så snart du husker det, med mindre det er nesten tid for neste dose. I dette tilfellet hopper du over den glemte dosen og følger den normale behandlingsplanen.
Ikke ta en dobbel dose som erstatning for en glemt tablett.
Dersom du slutter å ta Tolterodine
Legen din vil fortelle deg hvor lenge behandlingen med Tolterodine skal vare. Ikke avslutt behandlingen før du ikke merker en umiddelbar effekt. Blæren din trenger litt tid for å tilpasse seg. Avslutt løpet av depottabletter som legen din har foreskrevet. Fortell legen din om du ikke merker noen effekt innen den tid.
Fordelen med behandlingen bør vurderes på nytt etter 2 til 3 måneder. Rådfør deg alltid med legen din hvis du tenker på å stoppe behandlingen.
Spør lege eller apotek dersom du har ytterligere spørsmål om bruk av Tolterodine.
Overdosering Hva du skal gjøre hvis du har tatt for mye Tolterodine - Generisk legemiddel
Hvis du eller noen andre tar for mange depottabletter, må du kontakte lege eller apotek umiddelbart. Symptomer på overdosering inkluderer hallusinasjoner, spenning, en raskere enn normal puls, utvidede pupiller og manglende evne til å tisse og puste normalt.
Bivirkninger Hva er bivirkningene av Tolterodine - Generic drug
Som alle andre legemidler kan Tolterodine forårsake bivirkninger, men ikke alle får det.
Se legen din eller nærmeste akuttmottak på sykehuset umiddelbart hvis du opplever noen av symptomene på angioødem, for eksempel:
- hevelse i ansikt, tunge eller svelg
- problemer med å svelge
- elveblest og pustevansker.
Du bør også kontakte legen din hvis du opplever symptomer på en overfølsomhetsreaksjon (for eksempel kløe, utslett, elveblest, pustevansker). Dette er ikke vanlig (forekommer hos færre enn 1 av 100 pasienter).
Se legen din eller nærmeste akuttmottak på sykehuset umiddelbart hvis du opplever noen av følgende symptomer:
- brystsmerter, pustevansker eller tretthet (selv i hvile), pustevansker om natten, hevelse i beina.
Dette kan være symptomer på hjertesvikt. Dette er ikke vanlig (forekommer hos færre enn 1 av 100 pasienter).
Følgende bivirkninger har blitt observert under tolterodinbehandling, med frekvensene angitt.
Svært vanlige bivirkninger (forekommer hos mer enn 1 av 10 pasienter) er:
- Tørr i munnen
Vanlige bivirkninger (forekommer hos færre enn 1 av 10 pasienter) er:
- Bihulebetennelse
- Svimmelhet
- Døsighet
- Hodepine
- Tørre øyne
- Tåkesyn
- Fordøyelsesbesvær (dyspepsi)
- Forstoppelse
- Magesmerter
- For mye luft eller gass i mage og tarm
- Smerte eller problemer med vannlating
- Diaré
- Væskeretensjon som forårsaker hevelse (for eksempel i anklene)
- Tretthet
Mindre vanlige bivirkninger (forekommer hos færre enn 1 av 100 pasienter) er:
- Allergiske reaksjoner
- Hjertefeil
- Nervøsitet
- Uregelmessig hjerterytme
- Hjertebank
- Brystsmerter
- Manglende evne til å tømme blæren
- Prikking i hender og føtter
- Svimmelhet
- Minnehemming
Andre rapporterte reaksjoner inkluderer alvorlige allergiske reaksjoner, forvirring, hallusinasjoner, rask puls, rødme i huden, halsbrann, oppkast, angioødem, tørr hud og desorientering. Det har også vært rapporter om forverring av demenssymptomer hos pasienter som behandles for demens.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Hold Tolterodine utilgjengelig for barn.
Bruk ikke Tolterodine etter utløpsdatoen som er angitt på etiketten / esken. Utløpsdatoen refererer til den siste dagen i måneden.
Må ikke oppbevares over 25 ° C.
HDPE -flaske: holdbarheten etter første åpning er 200 dager.
Legemidler skal ikke kastes i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Annen informasjon
Hva TOLTERODINE DOC
Virkestoffet i Tolterodine 2 mg harde depotkapsler er 2 mg tolterodintartrat, tilsvarende 1,37 mg tolterodin.
Virkestoffet i Tolterodine 4 mg harde depotkapsler er 4 mg tolterodintartrat, tilsvarende 2,74 mg tolterodin.
Andre innholdsstoffer er: laktosemonohydrat, mikrokrystallinsk cellulose, poly (vinylacetat), povidon, silika, natriumlaurylsulfat, natriumdokusat, magnesiumstearat, hydroksypropylmetylcellulose.
Kapselens sammensetning: indigo karminrød (E132), kinolingul (bare i 2 mg) (E104), titandioksid (E171), gelatin.
Tablettbelegg inne: etylcellulose, trietylcitrat, metakrylsyre - etylakrylatkopolymer, 1,2 -propylenglykol.
Hvordan Tolterodine ser ut og innholdet i pakningen
Tolterodin er harde kapsler med forlenget frigjøring for enkelt daglig dose.
Tolterodine 2 mg harde kapsler med forlenget frigjøring er ugjennomsiktig grønn-ugjennomsiktig grønn.
Tolterodine 4 mg harde kapsler med forlenget frigjøring er ugjennomsiktig blå - ugjennomsiktig blå.
Tolterodine 2 mg harde depotkapsler er tilgjengelige i følgende pakningsstørrelser:
- 14, 28, 30, 50, 84, 100 depotkapsler i harde blisterpakninger
- 30, 100 og 200 harde depotkapsler i HDPE-flaske.
Tolterodine 4 mg harde depotkapsler er tilgjengelige i følgende pakningsstørrelser:
- 7, 14, 28, 49, 84, 98 harde depotkapsler i blisterpakninger
- 30, 100 og 200 harde depotkapsler i HDPE-flaske
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
TOLTERODINA DOC 2 - 4 MG
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver depotkapsel, hard, inneholder: tolterodintartrat 2 mg tilsvarende 1,37 mg tolterodin.
Hver depotkapsel, hard, inneholder: tolterodintartrat 4 mg tilsvarende 2,74 mg tolterodin.
Hver 2 mg depotkapsel, hard, inneholder 32.704 - 34.496 mg laktosemonohydrat.
Hver 4 mg depotkapsel, hard, inneholder 65,408 - 68,992 mg laktosemonohydrat.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Kapsler med langvarig frigivelse.
TOLTERODINE DOC 2 mg: ugjennomsiktig grønn til ugjennomsiktig grønn hard gelatinkapsel, størrelse 1, inneholdende 2 hvite, runde, bikonvekse, belagte tabletter.
Tolterodine 4 mg: ugjennomsiktig blå til ugjennomsiktig blå hard gelatinkapsel, størrelse 1, inneholdende 4 hvite, runde, bikonvekse, belagte tabletter.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Tolterodin er indisert for symptomatisk behandling av tranginkontinens og / eller økt urinfrekvens og hastverk hos pasienter med overaktiv blæresyndrom.
04.2 Dosering og administrasjonsmåte
Voksne (inkludert eldre pasienter) :
Den anbefalte dosen er 4 mg én gang daglig, bortsett fra hos pasienter med nedsatt leverfunksjon eller alvorlig nedsatt nyrefunksjon (GFR ≤ 30 ml / min) for hvem den anbefalte dosen er 2 mg én gang daglig (se pkt. 4.4 og 5.2). Ved plagsomme bivirkninger kan dosen reduseres fra 4 mg til 2 mg en gang daglig.
De harde depotkapslene kan tas med eller uten mat og skal svelges hele.
Behandlingseffekten bør revurderes etter 2-3 måneder (se pkt.5.1).
Pediatriske pasienter :
Tolterodins effekt hos barn er ikke påvist (se pkt. 5.1). Tolterodin anbefales derfor ikke til barn.
04.3 Kontraindikasjoner
Tolterodin er kontraindisert hos pasienter med:
- Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene
- Urinretensjon
- Ukontrollert smalvinklet glaukom
- Myasthenia gravis
- Alvorlig ulcerøs kolitt
- Giftig megakolon.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Tolterodin bør brukes med forsiktighet hos pasienter med:
- Betydelig obstruksjon av blærehalsen med risiko for urinretensjon
- Obstruktiv gastrointestinal lidelse, f.eks. pylorisk stenose
- Nedsatt nyrefunksjon (se pkt. 4.2 og 5.2)
- Leversykdom (se pkt. 4.2 og 5.2)
- Nevropati som påvirker det autonome nervesystemet
- Hiatal brokk
- Risiko for redusert gastrointestinal motilitet.
Administrasjon av flere daglige doser på 4 mg (terapeutisk) og 8 mg (supraterapeutisk) tolterodin med umiddelbar frigjøring har blitt observert for å forlenge QTc-intervallet (se pkt. 5.1) .Den kliniske relevansen av disse dataene er uklar, og det avhenger av risikoen faktorer og disposisjonen til den enkelte pasient.
Tolterodin bør brukes med forsiktighet hos pasienter med risikofaktorer for QT -forlengelse, inkludert:
- Forlengelse av medfødt eller ervervet og dokumentert QT
- Elektrolyttforstyrrelser som hypokalemi, hypomagnesemi og hypokalsemi
- Bradykardi
- Tidligere alvorlig koronar hjertesykdom (kardiomyopati, myokardiskemi, arytmi, kongestiv hjertesvikt)
- Samtidig administrering av legemidler som forlenger QT -intervallet inkludert klasse 1A (f.eks kinidin, prokainamid) og klasse III (f.eks. Amiodaron, sotalol) antiarytmika.
Dette gjelder spesielt når du tar en kraftig CYP3A4 -hemmer (se pkt.5.1). Samtidig behandling med potente CYP3A4 -hemmere bør unngås (se pkt. 4.5 Interaksjoner).
Som med alle andre behandlinger for urinveis symptomer eller tranginkontinens, bør mulige organiske årsaker til hastverk og hyppighet vurderes før behandling.
Dette produktet inneholder omtrent 67,2 mg laktose (33,6 mg glukose og 33,6 mg galaktose) per dose. Dette må tas i betraktning hos pasienter med diabetes mellitus. Pasienter med sjeldne arvelige problemer med galaktoseintoleranse, Lapp-laktasemangel eller glukose-galaktosemalabsorpsjon bør ikke ta denne medisinen.
Dette legemidlet inneholder 0,00404 mmol (eller 0,092988 mg) natrium per dose. Dette bør tas i betraktning av pasienter som har et lavt natriuminnhold.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Hos pasienter med dårlig CYP2D6 -metabolisme anbefales ikke samtidig systemisk behandling med potente CYP3A4 -hemmere som makrolidantibiotika (erytromycin og klaritromycin), soppdrepende midler (ketokonazol og itrakonazol) og proteasehemmere på grunn av økte serumkonsentrasjoner. Tolterodin, med (følgelig) risiko overdosering (se pkt. 4.4).
Samtidig behandling med andre legemidler som har antimuskarine egenskaper kan resultere i mer uttalte terapeutiske effekter og bivirkninger. Omvendt kan den terapeutiske effekten av tolterodin reduseres etter samtidig behandling med kolinerge muskarine reseptoragonister. Reduksjonen i gastrisk motilitet forårsaket av antimuskarinika kan påvirke absorpsjonen av andre legemidler.
Effekten av prokinetiske legemidler som metoklopramid og cisaprid kan reduseres av tolterodin.
Samtidig behandling med fluoksetin (en kraftig CYP2D6-hemmer) resulterer ikke i en klinisk signifikant interaksjon siden tolterodin og dets CYP2D6-avhengige metabolitt, 5-hydroksymetyltolterodin, er likeverdige.
Legemiddelinteraksjonsstudier har ikke vist noen interaksjoner med warfarin eller kombinasjon av orale prevensjonsmidler (etinyløstradiol / levonorgestrel).
En klinisk studie indikerte at tolterodin ikke er en metabolsk hemmer av CYP2D6, 2C19, 2C9, 3A4 eller 1A2. Derfor forventes det ingen økning i plasmanivåer av legemidler som metaboliseres via disse isoenzymer når det administreres i kombinasjon med tolterodin.
04.6 Graviditet og amming
Svangerskap
Det er ingen tilstrekkelige data om bruk av tolterodin hos gravide kvinner.
Dyrestudier har vist reproduksjonstoksisitet (se pkt. 5.3) Den potensielle risikoen for mennesker er ukjent.
Tolterodin anbefales derfor ikke under graviditet.
Foringstid
Det er ingen data om utskillelse av tolterodin i morsmelk. Bruk av tolterodin bør unngås under amming.
Fruktbarhet
Ingen data fra fertilitetsstudier er tilgjengelige.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Siden denne medisinen kan forårsake forstyrrelser i innkvarteringen og påvirke reaksjonstiden, kan evnen til å kjøre bil og bruke maskiner påvirkes negativt.
04.8 Bivirkninger
På grunn av dets farmakologiske egenskaper kan tolterodin forårsake milde til moderate antimuskarine effekter, som tørr munn, dyspepsi og tørre øyne.
Bivirkninger er oppført nedenfor etter systemorganklasse og etter frekvens. Frekvenser er definert som: svært vanlige (≥1 / 10), vanlige (≥1 / 100a
Tabellen nedenfor viser dataene hentet fra kliniske studier utført med tolterodin og de fra legemiddelovervåking. Den vanligste rapporterte bivirkningen var munntørrhet, som forekom hos 23,4% av pasientene som ble behandlet med depottolterodin og hos 7,7% av pasientene som ble behandlet med placebo.
Forverrede symptomer på demens (f.eks. Forvirring, desorientering, hallusinasjoner) har blitt rapportert etter at tolterodinbehandling ble startet hos pasienter som tok kolinesterasehemmere for behandling av demens.
Pediatrisk populasjon
I to randomiserte, dobbeltblindede, placebokontrollerte fase III pediatriske studier med 710 pediatriske pasienter i 12 uker, var andelen pasienter med urinveisinfeksjon, diaré og unormal oppførsel høyere hos pasienter behandlet med tolterodin enn hos de som ble behandlet med placebo. (urinveisinfeksjon: tolterodin 6,8%, placebo 3,6%; diaré: tolterodin 3,3%, placebo 0,9%; unormal oppførsel: tolterodin 1,6%, placebo 0,4%(se avsnitt 5.1)
04.9 Overdosering
Den høyeste dosen tolterodintartrat administrert som en enkelt dose til friske frivillige i formuleringen med umiddelbar frigjøring var 12,8 mg. De mest alvorlige bivirkningene som ble observert var forstyrrelser i innkvarteringen og vannlating.
Ved overdose utføres mageskylling og administrert aktivt kull.
Behandle symptomene som følger:
- Alvorlige sentrale antikolinerge effekter (f.eks. Hallusinasjoner, alvorlig spenning): administrer fysostigmin.
- Kramper eller uttalt eksitasjon: administrer benzodiazepiner.
- Åndedrettssvikt: gi kunstig åndedrett.
- Takykardi: administrer? -Blockere.
- Urinretensjon: bruk av kateteret.
- Mydriasis: administrer pilokarpin øyedråper og / eller hold pasienten i mørket.
Det ble observert en økning i QT-intervallet med en enkelt daglig dose på 8 mg tolterodin med umiddelbar frigjøring (to ganger anbefalt daglig dose av formuleringen med umiddelbar frigjøring og tilsvarende tre ganger maksimal eksponering av formuleringen med depottabletter) administrert over. 4 dager. Ved overdosering av tolterodin bør standard støttende tiltak for behandling av QT -intervallforlengelse benyttes.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: genitourinary system og kjønnshormoner.
Farmakoterapeutisk undergruppe: urinantispasmodika.
ATC -kode: G04B D07.
Tolterodin er en spesifikk konkurrerende muskarinreseptorantagonist som demonstrerer selektivitet for urinblæren over spyttkjertlene in vivo. En av metabolittene til tolterodin (5-hydroksymetylderivat) viser en lignende farmakologisk profil som den for hovedforbindelsen. Hos omfattende metaboliserere bidrar denne metabolitten vesentlig til den terapeutiske effekten av tolterodin (se pkt. 5.2).
Effekten av behandlingen kan forventes innen 4 uker.
I fase III -programmet var det primære endepunktet reduksjonen i antall inkontinensepisoder per uke, og de sekundære endepunktene var reduksjonen i antall micturitions per 24 timer og økningen i gjennomsnittlig volum av urin per micturition. Disse parameterne er vist i tabellen nedenfor.
Effekten av behandling med tolterodin 4 mg depottabletter, en gang daglig, etter 12 uker, sammenlignet med placebo. Absolutte og prosentvise endringer fra baseline. Behandlingsforskjell tolterodin vs. placebo: gjennomsnittlig endring estimert i henhold til metoden for minst kvadrater og 95% konfidensintervall.
* 97,5% konfidensintervall ifølge Bonferroni
Etter 12 ukers behandling rapporterte 23,8% (121/507) i tolterodin-gruppen med depottabletter og 15,7% (80/508) i placebogruppen at de subjektivt hadde lite eller ingen blæreproblemer.
Virkningene av tolterodin er evaluert hos pasienter under undersøkelse for den grunnleggende urodynamiske evalueringen, som etter resultatet av de urodynamiske testene ble plassert i de positive urodynamiske (motoriske haster) eller negative urodynamiske (sensoriske haster) gruppene. Innen hver gruppe ble pasientene randomisert til å motta både tolterodin og placebo. Studien ga ikke overbevisende bevis for at tolterodin har noen effekt over placebo hos pasienter med sensorisk hast.
De kliniske effektene av tolterodin på QT-intervallet i er basert på EKG fra over 600 behandlede pasienter, inkludert eldre pasienter og pasienter med eksisterende kardiovaskulær sykdom. Behandlet gruppe.
Tolterodins effekt på QT-forlengelse ble videre undersøkt hos 48 friske frivillige (mann og kvinne) i alderen 18-55 år. Fagene ble gitt 2 mg bud og 4 mg bud tolterodin i formuleringen med umiddelbar frigjøring. Resultatene (korrigert i henhold til Fridericias formel) ved maksimale tolterodinkonsentrasjoner (1 time) viste en gjennomsnittlig økning i QTc -intervallet på henholdsvis 5,0 og 11,8 msek for 2 mg tolterodindoser. bud og 4 mg bud og 19,3 msek for mofloxacin (400 mg) brukt som kontrollmedisin. En farmakokinetisk / farmakodynamisk modell viste at QTc-intervallet er økt hos dårlige metaboliserere (CYP2D6-frie) behandlet med tolterodin 2 mg bud sammenlignbar med den som ble observert hos raske metaboliserere behandlet med 4 mg bud. Ved begge doser tolterodin overskred ingen personer, uavhengig av metabolsk profil, 500 msek av den absolutte QTcF -verdien eller viste endringer fra baseline på 60 msek. Disse endringene regnes som spesielt betydelige terskelverdier. Dosen på 4 mg bud tilsvarer en maksimal eksponering (Cmax) lik tre ganger den som ble oppnådd med den høyeste terapeutiske dosen av tolterodinkapslene med deponering.
Pediatrisk populasjon
Det er ikke påvist effekt i den pediatriske populasjonen. To 12-ukers randomiserte, dobbeltblindede, placebokontrollerte fase III pediatriske studier med tolterodinkapsler med forlenget frigjøring ble utført. 710 pediatriske pasienter (486 behandlede) ble undersøkt. Med tolterodin og 224 behandlet med placebo) i alderen 5 til 10 år med økt urinfrekvens og urinhastighet.
I begge studiene ble det ikke observert noen signifikant endring fra baseline mellom de to gruppene i det totale antallet inkontinensepisoder / uke (se pkt. 4.8).
05.2 Farmakokinetiske egenskaper
Farmakokinetiske egenskaper som er spesifikke for denne formuleringen: Tolterodine kapsler med depottabletter resulterer i langsommere absorpsjon av tolterodin enn tabletter med umiddelbar frigjøring. Som et resultat observeres maksimal serumkonsentrasjon 4 (2-6) timer etter administrering av kapslene. Den tilsynelatende halveringstiden for tolterodin administrert som kapsler er ca. 6 timer hos omfattende metaboliserere og ca. 10 timer hos dårlige metaboliserere (CYP2D6-mangel).
Etter administrering av kapslene oppnås steady state -konsentrasjoner innen 4 dager.
Det er ingen effekt av mat på biotilgjengeligheten av kapslene.
Absorpsjon: Etter oral administrering, gjennomgår tolterodin metabolisme i første pass i leveren katalysert av CYP2D6, noe som fører til dannelsen av 5-hydroksymetylmetabolitten, en viktig farmakologisk ekvipotent metabolitt.
Den absolutte biotilgjengeligheten til tolterodin er 17% hos omfattende metaboliserere og 65% hos dårlige metaboliserere (CYP2D6 -mangel).
Fordeling: Tolterodin og 5-hydroksymetylmetabolitten bindes hovedsakelig til orosomukosid.
De ubundne fraksjonene er henholdsvis 3,7% og 36%. Distribusjonsvolumet for tolterodin er 113 liter.
Eliminering: Tolterodin metaboliseres i stor grad av leveren etter oral administrering.
Den primære metabolske banen er mediert av det polymorfe enzymet CYP2D6 og fører til dannelsen av 5-hydroksymetylmetabolitten.Videre metabolisme fører til dannelsen av 5-karboksylsyren og N-dealkylerte 5-karboksylsyremetabolitter, som utgjør 51% henholdsvis. og 29% av metabolittene som finnes i urinen. En andel (ca. 7%) av befolkningen er mangelfull i CYP2D6-aktiviteten. Metabolismeprofilen som er identifisert for disse pasientene (med dårlig metabolsk kapasitet) er dealkylering via CYP3A4-enzymer til dealkylert N-tolterodin, som ikke forårsaker kliniske effekter.
Resten av befolkningen består av raske metaboliserere. Hos omfattende metaboliserere er serum systemisk clearance av tolterodin omtrent 30 l / time.Hos pasienter med dårlig metabolsk kapasitet, redusert clearance resulterer i signifikant økte serumkonsentrasjoner av tolterodin (omtrent 7 ganger) og ubestemmelige konsentrasjoner av 5-hydroksymetylmetabolitten.
5-hydroksymetylmetabolitten er farmakologisk aktiv og ekvipotent med hensyn til tolterodin.
På grunn av forskjeller i proteinbindingsegenskapene til tolterodin og 5-hydroksymetylmetabolitten, er eksponeringen (AUC) av fritt tolterodin hos pasienter med dårlig metabolsk kapasitet lik den for kombinert fri tolterodin og 5-hydroksymetylmetabolitt hos pasienter med CYP2D6-aktivitet når den gis i samme dose Sikkerhet, toleranse og klinisk respons er like uavhengig av fenotype.
Utskillelse av radioaktivitet etter administrering av [14C] -tolterodin er omtrent 77% i urinen og 17% i avføringen. Mindre enn 1% av dosen utskilles uendret og omtrent 4% som 5-hydroksymetylmetabolitten Den karboksylerte metabolitten og den tilsvarende dealkylerte metabolitten står for henholdsvis omtrent 51% og 29% av uringjenoppretting.
I det terapeutiske doseringsområdet er farmakokinetikken lineær.
Spesielle pasientgrupper
Nedsatt leverfunksjon: Hos personer med levercirrhose finnes omtrent 2 ganger høyere eksponering av gratis tolterodin og dets 5-hydroksymetylmetabolitt (se pkt. 4.2 og 4.4).
Nedsatt nyrefunksjon: Gjennomsnittlig eksponering av fritt tolterodin og dets metabolitt 5-hydroksymetyl dobles hos pasienter med alvorlig nedsatt nyrefunksjon [inulinclearance (GFR) ≤ 30 ml / min].
Hos disse pasientene ble plasmanivåene til de andre metabolittene markant økt (opptil 12 ganger).
Den kliniske relevansen av den økte eksponeringen av disse metabolittene er ukjent.
Ingen data er tilgjengelig i tilfeller av lett til moderat nedsatt nyrefunksjon (se pkt.4.2 og 4.4).
Pediatrisk populasjon
Eksponeringen av virkestoffet per dose / mg er lik hos voksne og ungdom.Gjennomsnittlig eksponering av virkestoffet per dose / mg er omtrent to ganger høyere hos barn i alderen 5 til 10 år enn hos voksne (se pkt.4.2 og 5.1)
05.3 Prekliniske sikkerhetsdata
Klinisk signifikante effekter ble ikke observert i toksisitet, mutagenisitet, kreftfremkallende og sikkerhetsfarmakologiske studier, bortsett fra de som er relatert til farmakologiske effekter av stoffet.
Reproduksjonstoksisitetsstudier ble utført på mus og kaniner.
Hos mus var det ingen effekter av tolterodin på fruktbarhet eller reproduktiv funksjon.
Tolterodin resulterte i embryonal dødelighet og fostermisdannelser etter plasmaeksponering (Cmax eller AUC) 20 eller 7 ganger høyere enn de som ble sett hos behandlede menn.
Ingen effekter på misdannelser ble observert hos kaniner, men studiene ble utført ved plasmaeksponeringsverdier (Cmax eller AUC) som var 20 eller 3 ganger høyere enn forventet hos mennesker.
Tolterodin, så vel som dets aktive metabolitter hos mennesker, forlenger handlingspotensialets varighet (90% av repolarisering) i purkinje-fibre hos hunder (14-75 ganger terapeutiske nivåer) og blokkerer strømmen av K + i hERG-kanaler (klonet menneskelig eter- a-go-go-relatert gen) (0,5-26,1 ganger terapeutiske nivåer).
I studier utført på hunder etter administrering av tolterodin og dets aktive humane metabolitter (doser 3,1 til 61,0 ganger høyere enn terapeutiske nivåer), ble forlengelse av QT -intervallet observert.
Den kliniske relevansen av denne effekten er ukjent.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Laktosemonohydrat
Mikrokrystallinsk cellulose
Poly (vinylacetat)
Povidon
Silika
Natriumlaurylsulfat
Sodium docusate
Magnesiumstearat (E470b)
Hydroksypropylmetylcellulose
Sammensetning av kapselen:
- Indigo rød (E132)
- Kinolin gul (bare i 2 mg) (E104)
- Titandioksid (E171)
- Gelé
Belegget består av:
- Etylcellulose
- Trietylcitrat
- Metakrylsyre - etylakrylatkopolymer
- 1,2-propylenglykol
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
2 år.
HDPE -flaske: holdbarheten etter åpning er 200 dager.
06.4 Spesielle forholdsregler for lagring
Må ikke oppbevares over 25 ° C.
06.5 Emballasje og innhold i pakningen
Kartong med passende antall PVC / PE / PVDC aluminiumsblister og en pakningsvedlegg.
Pakningsstørrelser for 2,0 mg kapsler:
blisterpakninger med 14, 28, 30, 50, 84, 100 depottabletter
Pakningsstørrelser for 4,0 mg kapsler:
blisterpakninger med 7, 14, 28, 49, 84, 98 depottabletter
Kartong med en ugjennomsiktig hvit HDPE -flaske som inneholder passende antall kapsler, med skruehett og pakningsvedlegg.
Pakninger med 30, 100, 200 kapsler.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Ingen spesielle instruksjoner. Ubrukte medisiner og avfall fra denne medisinen må kastes i henhold til lokale forskrifter.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
DOC Generici S.r.l. - Via Turati 40 - 20121 Milano - Italia.
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
AIC 040824017 / M - 2 mg harde kapsler med forlenget frigjøring - 14 kapsler i PVC / PE / PVDC -AL blister
AIC 040824029 / M - 2 mg harde kapsler med forlenget frigjøring - 28 kapsler i PVC / PE / PVDC -AL blister
AIC 040824031 / M - 2 mg harde kapsler med forlenget frigjøring - 84 kapsler i PVC / PE / PVDC -AL blister
AIC 040824043 / M - 2 mg harde kapsler med forlenget frigjøring - 30 kapsler i HDPE -flaske
AIC 040824056 / M - 2 mg harde kapsler med forlenget frigjøring - 100 kapsler i HDPE -flaske
AIC 040824068 / M - 2 mg harde kapsler med forlenget frigjøring - 200 kapsler i HDPE -flaske
AIC 040824070 / M - 4 mg harde kapsler med forlenget frigjøring - 7 kapsler i PVC / PE / PVDC -AL blister
AIC 040824082 / M - 4 mg harde kapsler med forlenget frigjøring - 14 kapsler i PVC / PE / PVDC -AL blister
AIC 040824094 / M - 4 mg harde kapsler med forlenget frigjøring - 28 kapsler i PVC / PE / PVDC -AL blister
AIC 040824106 / M - 4 mg harde kapsler med forlenget frigjøring - 49 kapsler i PVC / PE / PVDC -AL blister
AIC 040824118 / M - 4 mg harde kapsler med forlenget frigjøring - 84 kapsler i PVC / PE / PVDC -AL blister
AIC 040824120 / M - 4 mg harde kapsler med forlenget frigjøring - 98 kapsler i PVC / PE / PVDC -AL blister
AIC 040824132 / M - 4 mg harde kapsler med forlenget frigjøring - 30 kapsler i HDPE -flaske
AIC 040824144 / M - 4 mg harde kapsler med forlenget frigjøring - 100 kapsler i HDPE -flaske
AIC 040824157 / M - 4 mg harde kapsler med forlenget frigjøring - 200 kapsler i HDPE -flaske
AIC 040824169 / M - 2 mg harde kapsler med forlenget frigjøring - 30 kapsler i blister av PVC / PE / PVDC -AL
AIC 040824171 / M - 2 mg depotkapsler, harde - 50 kapsler i PVC / PE / PVDC -AL blister
AIC 040824183 / M - 2 mg harde kapsler med forlenget frigjøring - 100 kapsler i PVC / PE / PVDC -AL blister
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Mars 2013.
10.0 DATO FOR REVISJON AV TEKSTEN
Mars 2013.