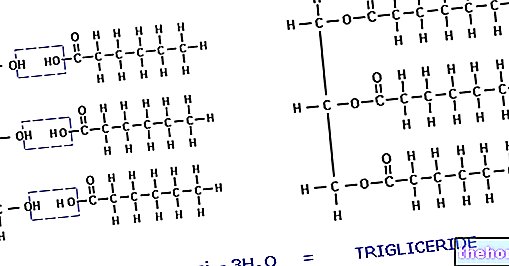
Aktive ingredienser: Pantoprazol
PANTOPAN 40 mg gastro-resistente tabletter
Pantopan pakningsinnsatser er tilgjengelige for pakningsstørrelser:- PANTOPAN 20 mg gastroresistente tabletter
- PANTOPAN 40 mg gastro-resistente tabletter
Indikasjoner Hvorfor brukes Pantopan? Hva er den til?
Pantopan er en 'selektiv protonpumpehemmer', som er et produkt som reduserer mengden syre som produseres i magen. Det brukes til behandling av syrerelaterte sykdommer i mage og tarm.
Pantopan brukes til å behandle:
Voksne og ungdom i alderen 12 år eller eldre:
- reflux esophagitis, en 'betennelse i spiserøret (røret som forbinder halsen med magen) ledsaget av tilbakeløp av syre fra magen.
Voksne:
- Infeksjon forårsaket av en bakterie som kalles Helicobacter pylori hos pasienter med duodenalsår og magesår, i kombinasjon med to antibiotika (utryddelsesbehandling). Målet er å eliminere bakterien og redusere sannsynligheten for at sårene kommer tilbake.
- Magesår og tolvfingertarm.
- Zollinger-Ellisons syndrom og andre sykdomstilstander som forårsaker overflødig magesyre.
Kontraindikasjoner Når Pantopan ikke skal brukes
Ikke ta Pantopan
- Hvis du er allergisk (overfølsom) overfor pantoprazol eller noen av de andre innholdsstoffene i Pantopan (se punkt 6).
- Hvis du er allergisk mot medisiner som inneholder andre protonpumpehemmere.
Forholdsregler for bruk Hva du trenger å vite før du bruker Pantopan
Vær spesielt forsiktig med Pantopan
- Hvis du har alvorlige leverproblemer. Fortell legen din dersom du noen gang har hatt leverproblemer. I så fall vil legen din trenge hyppigere kontroll av leverenzym, spesielt hvis du tar Pantopan for langtidsbehandling. deretter kan behandlingen avbrytes.
- Hvis du har lave kroppslager eller risikofaktorer for redusert vitamin B12-absorpsjon og er i langvarig behandling med pantoprazol. Som alle produkter som reduserer syresekresjon, kan pantoprazol redusere absorpsjonen av vitamin B12.
- Hvis du tar et legemiddel som inneholder atazanavir (for behandling av HIV -infeksjon) samtidig med pantoprazol, må du spørre legen din om spesifikke råd.
Fortell legen din umiddelbart hvis du merker noen av følgende symptomer:
- utilsiktet vekttap,
- tilbakevendende oppkast,
- problemer med å svelge,
- tilstedeværelse av blod i oppkastet,
- hvis du er blek og føler deg svak (anemi),
- tilstedeværelse av blod i avføringen,
- alvorlig eller vedvarende diaré, da en liten økning i smittsom diaré er observert med Pantopan.
Legen din kan bestemme at du må gjennomgå noen tester for å utelukke ondartet sykdom da pantoprazol kan lindre symptomene på kreft og kan forårsake forsinkelse i diagnosen. Hvis symptomene vedvarer til tross for behandling, vil ytterligere undersøkelser bli vurdert.
Hvis du tar Pantopan for langtidsbehandling, mer enn et år, kan det hende at legen din sjekker deg regelmessig. Når du oppsøker legen din, bør du rapportere nye eller eksepsjonelle symptomer og omstendigheter.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Pantopan
Pantopan kan påvirke effektiviteten til andre medisiner, så fortell legen din dersom du tar det
- medisiner som ketokonazol, itrakonazol og posakonazol (brukes mot soppinfeksjoner) eller erlotinib (indikert mot visse typer kreft) fordi Pantopan kan endre effektiviteten.
- Warfarin og fenprocoumon som påvirker fortykning eller tynning av blodet. Du kan trenge ytterligere kontroller.
- Atazanavir (brukes til å behandle HIV -infeksjon).
Fortell legen din eller apoteket dersom du bruker eller nylig har brukt andre legemidler, også reseptfrie.
Advarsler Det er viktig å vite at:
Graviditet og amming
Det er ikke tilstrekkelige data om bruk av pantoprazol under graviditet Det er påvist passering av det aktive stoffet i morsmelk.
Hvis du er gravid eller tror at du venter en baby eller ammer, bør du bare ta dette legemidlet hvis legen din mener at fordelen for deg oppveier den potensielle risikoen for det ufødte eller barnet.
Rådfør deg med lege eller apotek før du tar medisiner.
Kjøring og bruk av maskiner
Hvis du opplever svimmelhet eller synsforstyrrelser som bivirkninger, må du ikke kjøre bil eller bruke maskiner.
Dose, metode og administrasjonstidspunkt Hvordan du bruker Pantopan: Dosering
Ta alltid Pantopan nøyaktig slik legen din har fortalt deg. Hvis du er i tvil, bør du kontakte lege eller apotek.
Når og hvordan du skal ta Pantopan
Ta tablettene en time før et måltid uten å tygge eller knuse dem, men svelg dem hele med litt vann.
Med mindre legen din forteller deg noe annet, er den vanlige dosen:
Voksne:
For behandling av infeksjon forårsaket av en bakterie som kalles Helicobacter pylori hos pasienter med duodenalsår og magesår, i kombinasjon med to antibiotika (utryddelsesbehandling).
En tablett to ganger daglig pluss to antibiotika tabletter: amoksicillin, klaritromycin og metronidazol (eller tinidazol), som hver skal tas to ganger daglig med pantoprazol -tabletten. Ta den første pantoprazol -tabletten en "time før frokost og den andre pantoprazol -tabletten en" time før kveldsmaten. Følg legens instruksjoner og sørg for å lese pakningsvedlegget for disse antibiotika. Vanlig behandling er 1-2 uker.
For behandling av magesår og duodenalsår
Den vanlige dosen er en tablett per dag. Etter å ha konsultert legen din, kan dosen dobles. Legen din vil fortelle deg hvor lenge du skal ta medisinen. Behandlingsperioden for magesår er vanligvis mellom 4 og 8 uker. Behandlingsperioden for duodenalsår er vanligvis mellom 2 og 4 uker.
For langsiktig behandling av Zollinger-Ellison syndrom og andre tilstander som forårsaker overflødig magesyre.
Vanligvis er den anbefalte startdosen to tabletter om dagen.
Ta de to tablettene en time før et måltid. Legen din kan deretter justere dosen avhengig av mengden magesyre som produseres. Hvis det er foreskrevet mer enn to tabletter om dagen, ta tablettene to ganger daglig. Legen din foreskriver en daglig dose på mer enn fire tabletter om dagen, vil du bli fortalt nøyaktig når du skal slutte å ta medisinen.
Spesielle pasientgrupper
- Hvis du har nyreproblemer eller moderate eller alvorlige leverproblemer, bør du ikke ta Pantopan for å utrydde Helicobacter pylori.
- Hvis du har alvorlige leverproblemer, bør du ikke ta mer enn en pantoprazol 20 mg tablett per dag (pantoprazol 20 mg tabletter er tilgjengelig for dette).
- Barn under 12 år. Disse tablettene er ikke beregnet på bruk til barn under 12 år.
Overdosering Hva du skal gjøre hvis du har tatt for mye Pantopan
Dersom du tar for mye av Pantopan
Fortell legen din eller apoteket: det er ingen kjente symptomer på overdosering.
Dersom du har glemt å ta Pantopan
Ikke ta en dobbel dose som erstatning for en glemt tablett. Ta din neste normale dose til planlagt tidspunkt.
Dersom du slutter å ta Pantopan
Ikke slutt å ta disse tablettene uten å snakke med legen din eller apoteket først.
Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette produktet.
Bivirkninger Hva er bivirkningene av Pantopan
Som alle legemidler kan Pantopan forårsake bivirkninger, men ikke alle får det.
Hyppigheten av mulige bivirkninger listet nedenfor er definert i henhold til følgende konvensjon:
svært vanlig (rammer flere enn 1 av 10 brukere)
vanlig (rammer 1 til 10 brukere av 100)
uvanlig (rammer 1 til 10 brukere av 1000)
sjelden (rammer 1 til 10 brukere av 10.000)
svært sjelden (forekommer hos færre enn 1 av 10.000)
ikke kjent (frekvens kan ikke bestemmes ut fra tilgjengelige data).
Hvis du merker noen av følgende bivirkninger, må du slutte å bruke disse tablettene og fortelle legen din umiddelbart eller kontakte nærmeste legevakt:
Alvorlige allergiske reaksjoner (hyppighet sjelden): hevelse i tungen og / eller halsen, problemer med å svelge, elveblest, pustevansker, hevelse i ansiktet (Quinckes ødem / angioødem), alvorlig svimmelhet med svært rask puls og kraftig svette.
Alvorlige hudsykdommer (frekvens ikke kjent): blemmer og rask forverring av allmenntilstand, erosjon (inkludert lett blødning) i øyne, nese, munn / lepper eller kjønnsorganer (Stevens-Johnsons syndrom, Lyells syndrom, erythema multiforme) og lysfølsomhet .
Andre alvorlige effekter (frekvens ikke kjent): gulfarging av huden eller det hvite i øynene (alvorlig skade på leverceller, gulsott) eller feber, utslett, forstørrede nyrer med noen ganger smerter ved vannlating og smerter i korsryggen (alvorlig betennelse av nyrene).
Andre bivirkninger er:
- Mindre vanlige (påvirker 1 til 10 brukere per 1000) hodepine; svimmelhet diaré; ubehag, oppkast; oppblåsthet og flatulens (luft); forstoppelse; tørr i munnen; magesmerter og ubehag; hudutslett, eksantem, utslett; klø; føler seg svak, sliten eller generelt uvel; søvnforstyrrelser. Hvis du tar en protonpumpehemmer som pantoprazol, spesielt i mer enn ett år, kan du ha en litt økt risiko for hofte-, håndledds- eller ryggbrudd. Hvis du har osteoporose eller tar kortikosteroider (noe som kan øke risikoen av osteoporose) kontakt legen din.
- Sjelden (påvirker 1 til 10 av 10 000) endring eller tap av smak; synsforstyrrelser som tåkesyn; urticaria; articolar smerter; muskelsmerter; vektendringer; økning i kroppstemperatur; høy feber; hevelse i ekstremiteter (perifert ødem); allergiske reaksjoner; depresjon; brystforstørrelse hos menn.
- Veldig sjelden (påvirker færre enn 1 av 10.000) desorientering.
- Ikke kjent (frekvens kan ikke bestemmes ut fra tilgjengelige data) hallusinasjoner, forvirring (spesielt hos pasienter som tidligere har hatt disse symptomene); redusert konsentrasjon av natrium i blodet.
Hvis du tar pantoprazol i mer enn tre måneder, kan nivået av magnesium i blodet falle. Lave magnesiumnivåer kan manifestere seg med tretthet, ufrivillig rykninger i muskler, desorientering, kramper, svimmelhet og økt puls. Kontakt legen din umiddelbart hvis du har noen av disse symptomene. Lave nivåer av magnesium kan også føre til en reduksjon i kalium- eller kalsiumnivået i blodet. Legen din bør avgjøre om du vil kontrollere magnesiumnivået i blodet med jevne mellomrom.
Bivirkninger identifisert gjennom blodprøver:
- Mindre vanlige (påvirker 1 til 10 brukere av 1000) økte leverenzymer
- Sjeldne (rammer 1 til 10 brukere av 10 000) økt bilirubin; økt fett i blodet; drastisk nedgang i sirkulerende granulocytter, forbundet med høy feber.
- Svært sjelden (forekommer hos færre enn 1 av 10.000) reduksjon i antall blodplater som kan forårsake blødning eller blåmerker, mer enn normalt; reduksjon i antall hvite blodlegemer som kan føre til hyppigere infeksjoner; unormal reduksjon i antall røde og hvite blodlegemer, samt blodplater.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Oppbevares utilgjengelig for barn
Bruk ikke Pantopan etter utløpsdatoen som er angitt på esken og esken etter Utløpsdato.
Utløpsdatoen refererer til den siste dagen i måneden.
HDPE -flasker: ikke ta tablettene 120 dager etter at du har åpnet flasken
Dette legemidlet krever ingen spesielle oppbevaringsbetingelser.
Legemidler bør ikke kastes i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Sammensetning og farmasøytisk form
Hva Pantopan inneholder
- Den aktive ingrediensen er pantoprazol. En mage-resistent tablett inneholder 40 mg pantoprazol (som natriumsesquihydrat).
- Andre innholdsstoffer er: Kjerne: vannfritt natriumkarbonat, mannitol (E421), crospovidon, povidon K90, kalsiumstearat. Belegg: hypromellose, povidon K25, titandioksid (E171), gult jernoksid (E172), propylenglykol, metakrylsyre-etylakrylatkopolymer (1: 1), polysorbat 80, natriumlaurylsulfat, trietylcitrat. Trykkfarge: skjellakk, rødt jernoksid (E172), svart jernoksid (E172) og gult jernoksid (E172), konsentrert ammoniakkløsning.
Hvordan Pantopan ser ut og innholdet i pakningen
Gule, ovale, bikonvekse gastro-resistente tabletter merket "P40" på den ene siden.
Emballasje: flasker (høy tetthet polyetylen beholder med lav tetthet polyetylen lukking) og blister (ALU / ALU blister) uten eller med papp forsterkning (blister lommebok).
Pantopan er tilgjengelig i følgende pakninger:
Pakninger med 7, 10, 14, 15, 24, 28, 30, 48, 49, 56, 60, 84, 90, 98, 98 (2x49), 100, 112, 168 gastro-resistente tabletter.
Sykehuspakninger med 50, 90, 100, 140, 140 (10x14), 150 (10x15), 700 (5x140) gastro-resistente tabletter.
Ikke alle pakningsstørrelser markedsføres.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
PULMAXAN PULVER FOR INNÅNDING
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Pulmaxan 100 mcg / dosering, pulver for innånding
En Turbohaler dispenser inneholder: aktiv ingrediens: budesonid 20 mg
Pulmaxan 200 mcg / dosering, pulver for innånding
En Turbohaler dispenser inneholder: aktiv ingrediens: budesonid 20 mg
Pulmaxan 400 mcg / dosering, pulver for innånding
En Turbohaler dispenser inneholder: aktiv ingrediens: budesonid 20 mg
For fullstendig liste over hjelpestoffer, se 6.1.
03.0 LEGEMIDDELFORM
Pulver for innånding.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Pulmaxan er indisert ved behandling av bronkial astma.
04.2 Dosering og administrasjonsmåte
Dosen av Pulmaxan bør tilpasses den enkelte pasient i forhold til alvorlighetsgraden av astma og behandlingsfasen.
Voksne: i tilfeller av alvorlig astma i begynnelsen av inhalert kortikosteroidbehandling eller ved reduksjon eller seponering av oral kortikosteroidbehandling, er den anbefalte dosen 200 mcg 2-4 ganger daglig.
Vedlikeholdsdosen er individuell og bør være minimumsdosen som tillater fravær av symptomer: vanligvis er en innånding på 200 mcg per dag tilstrekkelig.
Barn fra 6 år og oppover: vanligvis 200 mcg per dag, i to doser. Om nødvendig kan dosen økes opp til 400 mcg per dag.
Ved forverring anbefales det å øke dosen Pulmaxan i henhold til resept.
Effekten begynner
Forbedring av astmakontroll etter administrering av inhalert Pulmaxan kan skje innen 24 timer etter behandlingstiden, selv om maksimal fordel oppnås etter 1-2 ukers behandling eller mer.
Instruksjoner for riktig bruk av Turbohaler -regulatoren:
Turbohaler drives av den inspirerende strømmen; dette betyr at når en pasient inhalerer gjennom munnstykket, kommer stoffet inn i luftveiene etter den inhalerte luften.
MERK: Det er viktig å instruere pasienten om å:
• les bruksanvisningen nøye i pakningsvedlegget.
• pust kraftig og dypt inn gjennom munnstykket for å sikre at den optimale dosen når lungene;
• pust aldri ut gjennom munnstykket;
• Skyll munnen med vann etter å ha pustet inn den foreskrevne dosen for å minimere risikoen for orofaryngeale candida -infeksjoner.
Pasienten kan ikke oppleve noen smak eller følelse av medisin mens han bruker Turbohaler på grunn av den lille mengden medisin som administreres.
Pasienter som ikke er behandlet med kortikosteroider
Den komplette terapeutiske effekten av Pulmaxan oppstår vanligvis innen 10 dager fra behandlingsstart, men hos pasienter der det er rikelig bronkial sekresjon, for eksempel å hindre inntrengning av den aktive ingrediensen i slimhinnen, anbefales det å assosiere kort tidsperiode (ca. 2 uker) en oral kortikosteroidbehandling. Det starter med full dosering og gradvis avtar til vedlikehold med Pulmaxan alene.
Forverring av astma etter bakterielle infeksjoner bør behandles med antibiotika ved å øke dosen av Pulmaxan.
Pasienter som trenger vedlikeholdsbehandling for sin astma, kan dra fordel av Pulmaxan Turbohaler -behandling ved anbefalte doser. For pasienter som ikke svarer tilstrekkelig på startdoser, kan høyere doser gi ytterligere astmakontroll.
Pasienter behandlet med inhalerte glukokortikosteroider
Kliniske studier utført på mennesker har vist en forbedring av effekten oppnådd med samme mengde budesonid som frigis av Turbohaler sammenlignet med aerosol under trykk. Derfor, når pasienter behandlet med Pulmaxan Nebuliser Suspension overføres til behandling med Pulmaxan Turbohaler og kontroll av astma er bra, er det mulig å redusere dosen til halve dosen administrert med aerosol under trykk. I tillegg, hos pasienter som er overført fra andre inhalerte glukokortikosteroider til Pulmaxan Turbohaler, kan en dosereduksjon vurderes etter først å ha gitt pasienten en lignende dose som den som ble brukt før overføringen.
Pasienter behandlet med orale kortikosteroider
Pulmaxan Turbohaler kan tillate erstatning eller betydelig dosereduksjon av orale glukokortikosteroider, slik at astmakontroll kan opprettholdes.
Spesiell oppmerksomhet bør rettes mot å overføre en pasient fra oral kortikosteroidbehandling til Pulmaxan -behandling, på grunn av langsom gjenoppretting av hypotalamiske funksjoner endret ved langvarig behandling med orale kortikosteroider. Ved overgang fra oral kortikosteroidbehandling til Pulmaxan skal pasienten være i en relativt stabil fase. En høy dose Pulmaxan administreres i kombinasjon med den tidligere brukte orale dosen i omtrent 10 dager.
Deretter bør den orale steroiddosen gradvis reduseres (for eksempel med 2,5 milligram Prednisolon eller tilsvarende hver måned) til lavest mulig nivå. I mange tilfeller er det mulig å erstatte det orale steroidet helt med Pulmaxan. For mer informasjon om kortikosteroiduttak, se pkt.4.4.
Ved bytte fra oral behandling til Pulmaxan i noen tilfeller kan det imidlertid være en reduksjon i den systemiske steroideffekten med symptomer som ledd og / eller muskelsmerter, tretthet og depresjon til tross for vedlikehold eller forbedring av lungefunksjonen. Pasienter bør oppmuntres til å fortsette behandlingen med Pulmaxan Turbohaler, men bør overvåkes for objektive tegn på binyreinsuffisiens.
Tiden som kreves for å gjenopprette den fysiologiske produksjonen av naturlige kortikosteroider kan være lang, og under visse forhold, for eksempel fysisk stress på grunn av alvorlige infeksjoner, traumer og kirurgi, kan det være nødvendig å kombinere Pulmaxan med oral kortikosteroidbehandling; selv i tilfeller av forverring, spesielt når det er forbundet med økt viskositet og dannelse av slimpropper, kan det være nødvendig med kortvarig komplementær behandling med orale steroider.
04.3 Kontraindikasjoner
Overfølsomhet overfor budesonid. Lungetuberkulose og andre bakterielle, virale og soppinfeksjoner som påvirker luftveiene.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Pulmaxan er en grunnleggende behandling for astmasykdom og bør derfor tas regelmessig i foreskrevne doser og så lenge legen din finner det hensiktsmessig.
Ved sår som påvirker fordøyelsessystemet, er det nødvendig med nøye overvåking av pasienten under hele behandlingsperioden.
Pulmaxan er ikke beregnet på rask forbedring av akutte episoder av astma, som krever en kortvirkende inhalert bronkodilatator.
Legen må nøye vurdere tilfeller av pasienter som ikke har fordeler av bruk av kortvirkende bronkodilatatorer eller som øker antall inhalasjoner sammenlignet med den vanlige. I disse tilfellene bør legen vurdere behovet for økt behandling med antiinflammatoriske legemidler, for eksempel ved å øke dosene inhalert budesonid eller ved å starte en kur med oral glukokortikosteroidbehandling.
Spesiell oppmerksomhet bør rettes mot overføring av pasienter fra oral steroidbehandling, da risikoen for binyrekompromis kan forbli i lang tid. Pasienter som har krevd akuttbehandling med høye doser kortikosteroider eller langvarig behandling med høye doser inhalerte kortikosteroider kan også være i fare. Slike pasienter kan vise tegn og symptomer på binyreinsuffisiens når de utsettes for alvorlig stress. I perioder med stress eller ved elektiv kirurgi bør ytterligere dekning med systemisk kortikosteroid vurderes.
Under undertrykkelsesfasen av systemisk glukokortikosteroidbehandling kan noen pasienter oppleve generell ubehag som muskel- og leddsmerter. Generell glukokortikosteroid insuffisiens bør mistenkes i de sjeldne tilfellene av symptomer som tretthet, hodepine, kvalme og oppkast. I disse tilfellene kan en midlertidig økning i dosen av orale glukokortikosteroider noen ganger være nødvendig.
Erstatning av systemisk steroidbehandling med inhalert terapi kan noen ganger manifestere allergier, for eksempel rhinitt og eksem, tidligere kontrollert av systemisk steroidbehandling. Disse allergiske manifestasjonene bør kontrolleres symptomatisk med antihistaminmedisiner og / eller aktuelle preparater.
Nedsatt leverfunksjon påvirker eliminering av glukokortikosteroider, noe som resulterer i redusert eliminasjonshastighet og høyere systemisk eksponering. Det er nødvendig å være klar over mulige systemiske bivirkninger, men de farmakokinetiske egenskapene til budesonid administrert intravenøst til cirrhotiske pasienter var lik de som ble funnet hos friske personer.Farmakokinetikken til budesonid etter oral administrering ble påvirket av nedsatt leverfunksjon. økt systemisk tilgjengelighet.Dette er imidlertid av begrenset klinisk betydning for Pulmaxan, ettersom dets muntlige bidrag til systemisk tilgjengelighet er relativt lite etter administrering av inhalasjon.
Samtidig bruk av ketokonazol, HIV -proteasehemmere eller andre potente CYP3A4 -hemmere bør unngås. Hvis dette ikke er mulig, bør tidsperioden mellom de to behandlingene være så lang som mulig (se også 4.5).
Spesiell forsiktighet er nødvendig for pasienter med aktiv eller hvilende lungetuberkulose og hos pasienter med sopp- eller virusinfeksjoner i luftveiene.
Oral candidiasis kan oppstå under behandling med inhalert kortikosteroid. Denne infeksjonen kan kreve behandling med passende soppdrepende behandling, og behandlingen må kanskje stoppes hos noen pasienter (se også 4.2).
Ved langtidsbehandling med høye doser Pulmaxan kan lokale og systemiske effekter oppstå. Systemiske effekter ved inhalert kortikosteroidbehandling forekommer sjeldnere enn ved oral kortikosteroidbehandling.
Systemiske effekter kan oppstå med inhalerte kortikosteroider, spesielt når det foreskrives i høye doser over lengre perioder. Disse effektene er mindre sannsynlige enn ved oral kortikosteroidbehandling.
Mulige systemiske effekter inkluderer Cushings syndrom, Cushingoid -aspekt, adrenal undertrykkelse, veksthemming hos barn og ungdom, redusert beinmineraltetthet, grå stær, glaukom og, mer sjelden, en rekke psykologiske eller atferdsmessige effekter, inkludert psykomotorisk hyperaktivitet, søvnforstyrrelser, angst, depresjon eller aggresjon (spesielt hos barn). Det er derfor viktig at dosen av det inhalerte kortikosteroidet er den lavest mulige dosen som opprettholder effektiv kontroll av astma. Derfor, på grunnlag av det ovennevnte, når astmakontrollen er oppnådd, bør dosen som skal brukes i vedlikeholdsbehandling være den minst effektive. Pulmaxan bør brukes med forsiktighet hos barn. Pulmaxan bør brukes med forsiktighet hos berørte pasienter. Fra sopp og virus infeksjoner (som meslinger og vannkopper) og hos personer med glaukom og grå stær.
Som med andre inhalerte behandlinger, kan paradoksal bronkospasme oppstå med en umiddelbar økning i piping etter administrering. I dette tilfellet bør inhalert budesonid seponeres umiddelbart, pasienten bør evalueres og alternativ behandling startes om nødvendig.
Innflytelse på vekst
Det anbefales at høyden på barn ved langvarig behandling med inhalerte kortikosteroider overvåkes periodisk. Hvis veksten bremses, bør behandlingen revurderes for å redusere dosen av inhalerte kortikosteroider. Fordelene med behandling med kortikosteroider. Og mulig risiko vekstundertrykkelse bør vurderes nøye, og det bør vurderes å henvise pasienten til en pediatrisk lungespesialist.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Hos pasienter på oral kortikosteroidbehandling bør overgangen til bruk av inhalert Pulmaxan alene skje gradvis.Etter stabilisering av pasienten kombineres Pulmaxan og dosen av det orale kortikosteroidet reduseres gradvis, mens pasientens generelle tilstand overvåkes. Med jevne mellomrom. Dette er nødvendig på grunn av langsom gjenoppretting av binyrefunksjonen svekket ved langvarig bruk av det orale kortikosteroid (se 4.2).
Det er ikke observert interaksjoner mellom budesonid og andre legemidler som brukes ved behandling av astma.
Metabolismen av budesonid medieres hovedsakelig av CYP3A4, cytokrom P450 isoenzym. Inhibitorer av dette enzymet, for eksempel ketokonazol og itrakonazol, kan derfor øke systemisk eksponering for budesonid flere ganger (se 4.4).
Siden det ikke er tilgjengelige data for å støtte en doseringsanbefaling, bør kombinasjonen av disse legemidlene unngås. Hvis dette ikke er mulig, bør det gå lengst mulig tid mellom de to behandlingene, og en reduksjon i dosen av budesonid kan vurderes.
Basert på en begrenset mengde data om denne interaksjonen for høye doser budesonid administrert inhalert, kan det oppstå betydelige økninger i plasmanivåer (i gjennomsnitt fire ganger) når itrakonazol, 200 mg én gang daglig, administreres samtidig med inhalert budesonid. (enkeltdose lik 1000 mcg).
Økte plasmakonsentrasjoner og forbedrede effekter av kortikosteroider ble observert hos kvinner som også ble behandlet med østrogen og prevensjonssteroider, mens det ikke ble observert noen effekt ved bruk av budesonid og samtidig inntak av lave doser orale prevensjonsmidler.
Siden binyrens funksjon kan være hemmet, kan en ACTH -stimuleringstest for å diagnostisere "hypofyseinsuffisiens gi falske (lave verdier) resultater."
Ved anbefalte doser har cimetidin en liten effekt på farmakokinetikken til oralt administrert budesonid som ikke er klinisk relevant.
04.6 Graviditet og amming
Resultatene kom fra store potensielle epidemiologiske studier og fra erfaring etter markedsføring på verdensbasis indikerer de ingen negative effekter på fosteret / nyfødtes helse ved bruk av inhalert budesonid under graviditet. Som med andre legemidler er det for administrering av budesonid under graviditet nødvendig å vurdere de forventede fordelene for moren med hensyn til risikoen for fosteret.
Budesonid utskilles i morsmelk. Imidlertid forventes det ingen effekt på det ammende barnet ved terapeutiske doser av Pulmaxan. Budesonid kan brukes under amming.
Vedlikeholdsterapi med inhalert budesonid (200 eller 400 mikrogram to ganger daglig) hos ammende astmatiske kvinner resulterer i ubetydelig systemisk eksponering for budesonid hos spedbarn som ammes.
I en farmakokinetisk studie var den estimerte daglige dosen for spedbarnet 0,3% av den daglige dosen som ble tatt av moren for både doseringsnivåer og gjennomsnittlig plasmakonsentrasjon hos spedbarnet ble estimert til å være 1/600 av konsentrasjonene observert i mors plasma, forutsatt fullstendig oral biotilgjengelighet for spedbarnet. Budesonidkonsentrasjoner funnet i plasma -prøver til spedbarn ble alltid funnet å være under kvantifiseringsgrensen.
Basert på data innhentet ved bruk av inhalert budesonid og på det faktum at budesonid viser en lineær farmakokinetisk profil innenfor det terapeutiske doseområdet etter nasal, inhalert, oral og rektal administrering ved terapeutiske doser av budesonid, er l "spedbarnseksponering antagelig lav.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Pulmaxan påvirker ikke evnen til å kjøre bil og bruke maskiner.
04.8 Bivirkninger
Kliniske studier, litteratur og markedsføringserfaring tyder på at følgende bivirkninger kan forekomme.
Følgende definisjoner refererer til forekomsten av uønskede effekter:
Frekvenser er definert som: svært vanlige (≥ 1/10), vanlige (≥1 / 100 til
* Vennligst se delen "Pediatrisk befolkning" nedenfor.
Sjelden, for ukjente mekanismer, kan medisiner administrert ved innånding forårsake bronkospasme.
Ved inhalasjon av glukokortikosteroider kan tegn og symptomer på systemiske glukokortikosteroideffekter sjelden forekomme, inkludert adrenal hypofunksjonalitet og redusert veksthastighet som sannsynligvis vil avhenge av dose, eksponeringstid, samtidig og tidligere steroidbehandling og sensitivitet.
Pasienter som nylig har fått diagnosen kronisk obstruktiv lungesykdom (KOL) som starter behandling med inhalerte kortikosteroider har økt risiko for å utvikle lungebetennelse. En vektet evaluering av 8 samlede kliniske studier utført på 4643 pasienter med KOL og behandlet med budesonid og 3643 pasienter randomisert til behandlinger uten inhalerte kortikosteroider fant imidlertid ingen økt risiko for å utvikle lungebetennelse. Resultatene av de første 7 av disse 8 kliniske studiene ble publisert i en metaanalyse.
Pediatrisk populasjon
Gitt risikoen for veksthemming hos den pediatriske pasientpopulasjonen, bør veksten overvåkes som beskrevet i pkt.4.4.
04.9 Overdosering
Akutt overdose med Pulmaxan, selv i høye doser, forventes ikke å forårsake kliniske problemer.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: annen anti-astma, inhalatorer, glukokortikoider.
ATC -kode: R03BA02
Budesonid er et glukokortikosteroid med høy lokal antiinflammatorisk aktivitet.
Aktuell antiinflammatorisk aktivitet
Den eksakte virkningsmekanismen for glukokortikosteroider ved behandling av astma er ikke fullt ut forstått. Antinflammatoriske aktiviteter som inhibering av frigjøring av inflammatoriske mediatorer og inhibering av den cytokinmedierte immunresponsen er trolig viktig. Budesonids egenstyrke, målt som affinitet for glukokortikoidreseptorer, er omtrent 15 ganger høyere enn prednisolon.
En klinisk studie utført på astmatiske pasienter, der inhalert budesonid ble sammenlignet med oral administrering, viste "statistisk signifikant bevis på effekt med inhalert, men ikke oral administrering, sammenlignet med placebo.
Derfor kan den terapeutiske effekten av konvensjonelle doser av budesonid, administrert ved innånding, i stor grad tilskrives lokal virkning i luftveiene.
I provokative studier utført på dyr og pasienter har budesonid vist seg å ha en anti-anafylaktisk og antiinflammatorisk effekt, representert ved reduksjon av graden av bronkial obstruksjon i umiddelbar og sen allergisk respons.
Reaktivitet i luftveiene
Hos hyperreaktive pasienter har budesonid vist seg å redusere luftveienes respons på direkte og indirekte stimuli.
Klinisk sikkerhet
Pediatrisk populasjon
Spaltelampeundersøkelser ble utført hos 157 barn (5-16 år), behandlet med en gjennomsnittlig daglig dose på 504 mg i 3-6 år. Resultatene ble sammenlignet med 111 aldersmatchede astmatiske barn.
Inhalert budesonid var ikke assosiert med økt forekomst av posterior subkapsulær grå stær.
Aktiviteten til hypothalamus-hypofyse-binyre-aksen
Studier med Pulmaxan hos friske frivillige har vist doserelaterte effekter på plasma og urinkortisol.
ACTH -testen har vist at behandling med Pulmaxan, ved anbefalte doser, gir vesentlig mindre effekt på binyrefunksjonen enn prednison 10 mg.
05.2 "Farmakokinetiske egenskaper
Absorpsjon
Etter oral inhalering via Pulmaxan Turbohaler oppstår plasmakonsentrasjoner av budesonid (4,0 nmol / l etter en dose på 800 mg) innen 30 minutter. Maksimal plasmakonsentrasjon og arealet under plasmakonsentrasjonstidsprofilkurven øker lineært med dosen, men er litt (20-30%) høyere etter gjentatte doser (3 ukers behandling) enn etter en enkelt dose.
Lungeavsetning hos friske personer ble estimert til å være 34% ± 10% av den leverte dosen (aritmetisk gjennomsnitt ± SD), mens 22% ble beholdt i munnstykket og resten (ca. 45% av den leverte dosen) ble inntatt.
Fordeling
Budesonid har et distribusjonsvolum på omtrent 3 L / kg. Plasmaproteinbinding er i gjennomsnitt 85-90%.
Biotransformasjon
First pass hepatisk budesonid metaboliseres raskt i en høy prosentandel (≥ 90%) til metabolitter preget av lav glukokortikosteroidaktivitet. Hovedmetabolittene er 6β-hydroksybudesonid og 16α-hydroksyprednisolon, hvis glukokortikosteroidaktivitet er mindre enn 1% sammenlignet med budesonids metabolisme av budesonid medieres hovedsakelig av isoenzymet CYP3A4, som tilhører cytokrom P450.
Eliminering
Metabolittene til budesonid utskilles som sådan eller i konjugert form, hovedsakelig via nyrene. Uendret budesonid finnes ikke i urinen. Budesonid har en høy systemisk clearance (ca. 1,2 l / min), og etter IV-administrering er terminal halveringstid i gjennomsnitt 2-3 timer.
Linjæritet
Ved klinisk relevante doser er de kinetiske parametrene til budesonid doseavhengige.
Pediatrisk populasjon
Budesonid har en systemisk clearance på omtrent 0,5 l / min hos 4-6 år gamle astmatiske barn. Barn har en klaring per kg kroppsvekt som er omtrent 50% større enn hos voksne. Den terminale halveringstiden for budesonid etter innånding er ca. 2,3 timer hos astmatiske barn, omtrent den samme som hos friske voksne.
Hos astmatiske barn som ble behandlet med Pulmaxan Turbohaler (800 mg enkeltdose), nådde plasmakonsentrasjonen Cmax (4,85 nmol / l) 13,8 minutter etter innånding, og reduserte deretter raskt; AUC var 10,3 nmol • t / L.
AUC -verdien er generelt sammenlignbar med den som ses hos voksne med samme dose, men C -verdien har en tendens til å være høyere hos barn.
Lungeavsetning hos barn (31% av den nominelle dosen) er lik den som ble målt hos friske voksne (34% av den nominelle dosen).
05.3 Prekliniske sikkerhetsdata
Resultatene av akutte, subakutte og kroniske toksisitetsstudier viser at de systemiske effektene av budesonid enten er mindre alvorlige eller ligner dem som ble observert etter administrering av andre glukokortikosteroider, for eksempel redusert vektøkning, atrofi av lymfoide og binyrevev.
Budesonid, evaluert med seks forskjellige tester, viste ingen mutagene eller klastogene effekter.
Økningen i forekomsten av cerebrale gliomer, funnet i en karsinogenitetsstudie utført hos hannrotter, ble ikke bekreftet i en påfølgende studie, der forekomsten av gliomer observert i gruppene behandlet med aktive legemidler (budesonid, prednisolon, triamcinolonacetat) var lik den som ble observert i kontrollgruppene. Karsinogenitetsstudier utført på hannrotter tillot å observere leverendringer (primære hepatocellulære neoplasmer) som ble bekreftet i en annen studie utført ved behandling av dyr med budesonid og referanseglukokortikosteroider. Disse manifestasjonene er sannsynligvis relatert til reseptoreffekter av glukokortikosteroider og representerer en effekt som er typisk for den terapeutiske klassen.
Den tilgjengelige kliniske erfaringen viser at det ikke er bevis for at budesonid eller andre glukokortikosteroider forårsaker hjernegliomer eller primære hepatocellulære neoplasmer hos mennesker.
Studier på dyr har vist teratogene effekter som varierer etter dyrearten.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Produktet inneholder ikke hjelpestoffer.
06.2 Uforlikelighet
Det oppstår ikke
06.3 Gyldighetsperiode
2 år
06.4 Spesielle forholdsregler for lagring
Må ikke oppbevares over 30 ° C. Oppbevares med lokket tett lukket.
06.5 Emballasje og innhold i pakningen
Turbohaler er en multidose -dispenser for pulver, drevet av den inspirerende strømmen. Dispenseren er laget av plastmateriale og kan inneholde 50, 100 eller 200 doser.
06.6 Bruksanvisning og håndtering
Se 4.2
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
AstraZeneca S.p.A.
Volta -palasset
Via F. Sforza
Basiglio (MI)
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
Pulmaxan 100 mcg / dosering, pulver for innånding - 1 dispenser på 200 doser - AIC 027621010
Pulmaxan 200 mcg / dosering, pulver for innånding - 1 dispenser på 100 doser - AIC 027621022
Pulmaxan 400 mcg / dosering, pulver for innånding - 1 dispenser på 50 doser - AIC 027621034.
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
AIC -dato: 04.10.1995
Fornyelsesdato: 30.12.2008
10.0 DATO FOR REVISJON AV TEKSTEN
AIFA Fastsettelse av mai 2012.