Hva er Temozolomide Hospira?
Temozolomide Hospira er et legemiddel som inneholder virkestoffet temozolomid. Den er tilgjengelig som kapsler (hvit og grønn: 5 mg; hvit og gul: 20 mg; hvit og rosa: 100 mg; hvit og blå: 140 mg; hvit og brun: 180 mg; hvit: 250 mg).
Temozolomide Hospira er et 'generisk legemiddel', noe som betyr at Temozolomide Hospira ligner et 'referansemedisin' som allerede er godkjent i EU (EU) kalt Temodal.
Hva brukes Temozolomide Hospira til?
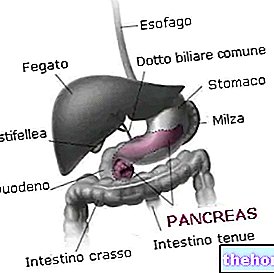
Temozolomide Hospira er et legemiddel mot kreft. Det er indisert for behandling av ondartede gliomer (hjernesvulster) i følgende pasientgrupper:
voksne nylig diagnostisert med glioblastoma multiforme (en spesielt aggressiv type hjernesvulst). Temozolomide Hospira brukes først med strålebehandling, deretter alene;
voksne og barn fra tre år med et ondartet gliom som glioblastoma multiforme eller anaplastisk astrocytom, når svulsten har dukket opp igjen eller blitt verre etter standardbehandling. Temozolomide Hospira brukes alene hos disse pasientene.
Medisinen kan bare fås på resept.
Hvordan brukes Temozolomide Hospira?
Behandling med Temozolomide Hospira bør forskrives av en lege med erfaring i behandling av hjernesvulster.
Doseringen av Temozolomide Hospira, gitt en gang daglig, avhenger av kroppsoverflaten (beregnet ut fra pasientens høyde og vekt) og varierer fra 75 til 200 mg per kvadratmeter en gang daglig. De avhenger av hvilken type kreft som behandles, om pasienten tidligere har blitt behandlet, om Temozolomide Hospira brukes alene eller sammen med andre behandlinger, og pasientens respons på behandlingen. Temozolomide Hospira bør administreres mellom måltidene.
Før de får Temozolomide Hospira, kan pasienter også trenge medisin som forhindrer oppkast. Temozolomide Hospira bør brukes med forsiktighet hos pasienter med alvorlige lever- eller nyreproblemer.
For fullstendig informasjon, se Sammendrag av produktkarakteristikker (også inkludert i EPAR).
Hvordan fungerer Temozolomide Hospira?
Virkestoffet i Temozolomide Hospira, temozolomid, tilhører en gruppe legemidler mot kreft som kalles alkyleringsmidler. I kroppen omdannes temozolomid til en annen forbindelse kalt MTIC. MTIC binder seg til cellene i DNA i reproduksjonsfasen, og blokkerer derved celledeling. Som et resultat kan kreftceller ikke reprodusere seg og svulstveksten bremses.
Hvordan har Temozolomide Hospira blitt studert?
Siden Temozolomide Hospira er et generisk legemiddel, har studiene vært begrenset til bevis som viser at medisinen er bioekvivalent med referansemedisinen Temodal. To medisiner er bioekvivalente når de produserer de samme nivåene av det aktive stoffet i kroppen.
Hva er fordelene og risikoene med Temozolomide Hospira?
Fordi Temozolomide Hospira er et generisk legemiddel og er bioekvivalent med referansemedisinen, antas fordelene og risikoen med medisinen å være de samme som referansemedisinen.
Hvorfor har Temozolomide Hospira blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) konkluderte med at Temozolomide Hospira har vist seg å ha sammenlignbar kvalitet og være bioekvivalent med Temodal basert på kravene i EU -lovgivningen. Derfor er CHMP av den oppfatning at fordelene, som i tilfellet med Temodal, oppveier de identifiserte risikoene. Komiteen anbefalte derfor å gi markedsføringstillatelse for Temozolomide Hospira.
Annen informasjon om Temozolomide Hospira
15. mars 2010 ga EU -kommisjonen Hospira UK Ltd en "markedsføringstillatelse" for Temozolomide Hospira, gyldig i hele EU.
Markedsføringstillatelsen er gyldig i fem år og kan fornyes etter denne perioden.
For hele versjonen av Temozolomide Hospira EPAR, klikk her.
For mer informasjon om Temozolomide Hospira -behandling, les pakningsvedlegget (inkludert i EPAR).
Den fullstendige EPAR -versjonen av referansemedisinen finnes også på Byråets nettsted.
Siste oppdatering av dette sammendraget: 03/2010.
Informasjonen om Temozolomide Hospira publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.