Redigert av Dr. Giovanni Chetta
Fra biokjemi til biomekanikk

Ekstra-cellulær matrise (MEC)
En beskrivelse, om enn det lille vi vet i dag, av ECM (ekstracellulær matrise) er avgjørende for å bedre forstå viktigheten av endringer i ryggraden og holdning for helse.
Hver celle, som alle flercellede levende organismer, må "føle" og samhandle med omgivelsene for å kunne utføre sine vitale funksjoner og overleve. I en flercellet organisme må cellene koordinere de forskjellige atferdene som i et fellesskap av mennesker.

ECM beskrives generelt som sammensatt av flere store klasser av biomolekyler:
- Strukturelle proteiner (kollagen og elastin)
- Spesialiserte proteiner (fibrillin, fibronektin, laminin etc.)
- Proteoglykaner (aggrecans, syndecans) og glusaminoglycans (hyaluronaner, kondroitinsulfater, heparansulfater, etc.)
Blant de strukturelle proteinene, dvs. kollagen danner den mest representerte familien av glykoproteiner i dyreriket. De er de mest tilstedeværende proteiner i ECM (men ikke det viktigste) og er de grunnleggende bestanddelene i riktig bindevev (brusk, bein, fascia, sener, ledbånd).
Kollagener blir for det meste syntetisert av fibroblaster, men epitelceller er også i stand til å syntetisere dem.
Kollagenfibrene samhandler kontinuerlig med en enorm mengde andre molekyler i ECM som utgjør et biologisk kontinuum som er grunnleggende for cellens liv.De tilhørende kollagenene i fibriller spiller en dominerende rolle i dannelsen og vedlikeholdet av strukturer som er i stand til å motstå spenningskrefter som er nesten uelastisk kollagen produseres og metaboliseres på nytt som en funksjon av den mekaniske belastningen og dens viskoelastiske egenskaper har stor innvirkning på menneskets holdning.
Kollagenfibre takket være deres PG / GAG -belegg (proteoglykaner / glukosaminoglykaner) besitter biosensor og bioledende egenskaper. Vi vet faktisk at enhver mekanisk kraft som er i stand til å generere en strukturell deformasjon, stresser de intermolekylære bindingene som gir en liten elektrisk strøm, det vil si den piezoelektriske strømmen (Athenstaedt, 1969). Derfor har det tredimensjonale og allestedsnærværende kollagennettverket også den særegne egenskapen ved å lede bioelektriske signaler i de tre dimensjonene i rommet, basert på det relative arrangementet mellom kollagenfibriller og celler, i afferent retning (fra ECM til cellene) eller vice versa efferent.
Alt dette representerer et sanntids MEC-celle kommunikasjonssystem og slike elektromagnetiske bio-signaler kan føre til viktige biokjemiske endringer, for eksempel i "bein osteoklaster kan ikke" fordøye "piezoelektrisk ladet bein (Oschman, 2000).
Til slutt bør det understrekes at cellen, ikke overraskende, produserer kontinuerlig og med store energiforbruk (ca. 70%) materiale som nødvendigvis må utvises gjennom eksklusiv lagring av protokollagen (biologisk forløper for kollagen) i spesifikke vesikler ( Albergati, 2004).
De aller fleste virveldyrvev krever samtidig tilstedeværelse av to vitale egenskaper: styrke og elastisitet. Et ekte nettverk av elastiske fibre, plassert inne i ECM for disse vevene, gjør det mulig å gå tilbake til de opprinnelige forholdene etter sterke trekk.De elastiske fibrene er i stand til å øke utvidelsen av et organ eller en del av det minst fem ganger. Lange, uelastiske kollagenfibre er spredt mellom de elastiske fibrene med den presise oppgaven å begrense en "overdreven deformasjon ved trekk i vevene." Elastin representerer hovedkomponenten i elastiske fibre og finnes i spesielt store mengder i blodkar med elastiske egenskaper ( utgjør mer enn 50% av den totale tørrvekten til aorta), i leddbåndene, i lungen og i huden. Glatte muskelceller og fibroblaster er de viktigste produsentene av forløperen, tropoelastin.
ECM inneholder et stort (og fremdeles ikke godt definert) antall spesialiserte ikke-kollagenproteiner som vanligvis har spesifikke bindingssteder for andre ECM-molekyler og celleoverflatereseptorer. På denne måten fungerer hver eneste komponent i disse proteinene som en "forsterker" av kontakter, både mellom lignende og forskjellige molekyler, og skaper et uendelig biokjemisk nettverk som er i stand til å generere, modulere, variere og forplante seg selv på avstand millioner og millioner av biokjemisk informasjon (og energi).
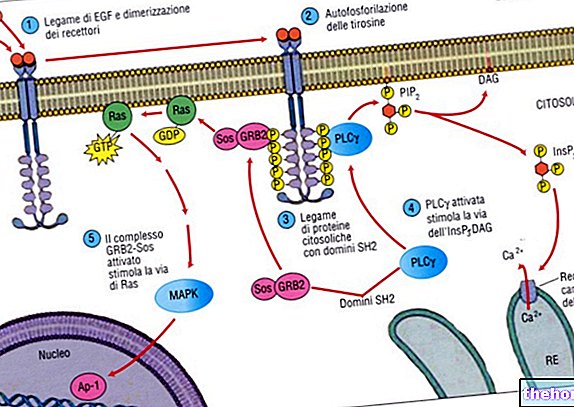
Et viktig "spesialisert protein i den ekstracellulære matrisen er fibronektin, glykoprotein med høy molekylvekt som finnes i alle virveldyr. Fibronektin ser ut til å kunne påvirke cellevekst, intercellulær vedheft og med ECM, cellemigrasjon på forskjellige måter (cellen kan bevege seg opptil 5 cm per dag - Albergati, 2004) etc. Den mest kjente isoformen, type III, binder seg til integriner . Sistnevnte er en familie av transmembrane proteiner som fungerer som mekanoreseptorer: de transduserer, selektivt og på en modulerbar måte, mekaniske trekk og press fra ECM inne i cellen og omvendt, og induserer en rekke reaksjoner i cytoplasma som involverer cytoskjelettet og andre proteiner som de regulerer celleadhesjon, vekst og migrasjon (Hynes, 2002).
Glukosaminoglykaner (GAGS) og proteoglykaner (PG) danner et sterkt hydratisert gelignende stoff definert i bindevevet, der de fibrillære proteiner er plassert og imbrisert. Denne formen for polysakkaridgel er på den ene siden i stand til å la ECM motstå betydelige trykkrefter og på den andre siden tillate en rask, konstant og selektiv diffusjon av næringsstoffer, metabolitter og hormoner mellom blod og vev.
Polysakkaridkjedene til glukosaminoglykaner er volumetrisk for stive til å brette seg inn i de kompakte kuleformede strukturene som er typiske for polypeptidkjeder, i tillegg er de sterkt hydrofile. Av disse grunnene (og sannsynligvis også for andre ukjente for oss) har GAG -ene en tendens til å anta ekstreme konformasjoner. opptar et stort volum i forhold til massen og danner dermed betydelige mengder gel selv ved lave konsentrasjoner Den høye mengden negative ladninger (GAG -ene representerer de mest tallrike anioniske cellene, som vanligvis sulfateres, produseres av dyreceller) tiltrekker seg mange kationer; blant disse spilles en dominerende rolle av Na + som gir hele den osmotiske kapasiteten og fanger en enorm mengde vann i ECM. På denne måten genereres hevelser (turgorer) som gjør at ECM kan motsette seg selv viktige trykkrefter (takket være dette, for eksempel kan brusk i hoften, under fysiologiske forhold, perfekt motstå et trykk på flere hundre atmosfærer).
Inne i bindevevet representerer GAGs mindre enn 10-12% av den globale vekten, men takket være deres egenskaper fyller de mange av de ekstracellulære mellomrom som danner porer av hydrert gel i forskjellige størrelser og tettheter av elektriske ladninger og fungerer dermed som selektive nøkkelpunkter eller "servere" der trafikken til molekyler og celler inne i MEC reguleres, basert på størrelse, vekt og elektrisk ladning.
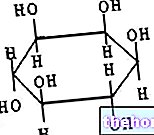
Hyaluronsyre (hyaluronan, hyaluronat) representerer kanskje den enkleste av GAG-ene. Eksperimentelle og molekylærbiologiske data bekrefter at den spiller en grunnleggende rolle på nivå av bein og ledd når det gjelder motstand mot betydelige trykk. Fylling av mellomrom i ECM under embryonal utvikling : det skaper tomme mellomrom mellom cellene de vil migrere inn i senere stadier (Albergati, 2004).
Ikke alle PG blir utskilt av ECM, noen er integrerte komponenter i plasmamembraner (Alberts, 2002).
Extra-Cellular Matrix kan derfor betraktes som et veldig komplekst nettverk der proteiner, PGS og GAG gir utallige funksjoner, inkludert strukturell støtte og regulering av hvert vev og organisk aktivitet. Global mobil homeostase bør betraktes som et kompleks av mekanismer som kan oppstå og utvikle seg inne i cellen eller utenfor ECM; i sistnevnte tilfelle kan cellen representere det mellomliggende eller siste målet. De ekstracellulære komponentene, i tillegg til å representere fysiske støttestrukturer for det cellulære stillaset, fungerer også som virkelige steder for initiering, utvikling og avslutning av vitale prosesser som angår både det endocellulære miljøet og organer og systemer. Vi står overfor et uendelig biokjemisk nettverk som er i stand til å generere, modulere, variere og spre seg, selv på avstand, millioner og millioner av informasjon.
Hver celle i kroppen samhandler konstant med ECM, både under de mekaniske og kjemiske og energiske aspektene, med "dramatiske" effekter på vevets statiske og dynamiske arkitektur. I følge P. A. Bacci representerer den interstitielle matrisen virkelig moren til vitale reaksjoner, stedet der først og fremst utvekslingen mellom materie og energi finner sted. Alle vev er forbundet og funksjonelt integrert med hverandre ikke i lukkede, men åpne systemer; kontinuerlige utvekslinger finner sted mellom dem, som kan skje både lokalt og systemisk, og utnytter biokjemiske, biofysiske og elektromagnetiske meldinger, det vil si ved bruk av de forskjellige energiformene.
Som F. G.I huset representerer cellen og den ekstracellulære matrisen bare to tilsynelatende separate verdener som nødvendigvis for hele levetiden må samhandle når som helst for å fungere på en korrekt og synergistisk måte. Dette krever en ekstraordinær serie signaler etterfulgt av en like utrolig rekke molekylærbiologiske aktiviteter.
Andre artikler om "Extra -Cellular Matrix - Structure and Functions"
- Behandling av skoliose
- Skoliose - årsaker og konsekvenser
- Skoliose diagnose
- Prognose for skoliose
- Bindevev og Bindefascia
- Tilkoblingsbånd - funksjoner og funksjoner
- Holdning og tensegrity
- Menneskets bevegelse og viktigheten av setestøtte
- Viktigheten av riktig seteleie og okklusal støtte
- Idiopatisk skoliose - myter å fjerne
- Klinisk tilfelle av skoliose og terapeutisk protokoll
- Behandlingsresultater Klinisk caseskoliose
- Skoliose som en naturlig holdning - Bibliografi