Aktive ingredienser: Irbesartan
Karvea 300 mg tabletter
Pakningsinnsatser fra Karvea er tilgjengelige for pakningsstørrelser:- Karvea 75 mg tabletter
- Karvea 150 mg tabletter
- Karvea 300 mg tabletter
Hvorfor brukes Karvea? Hva er den til?
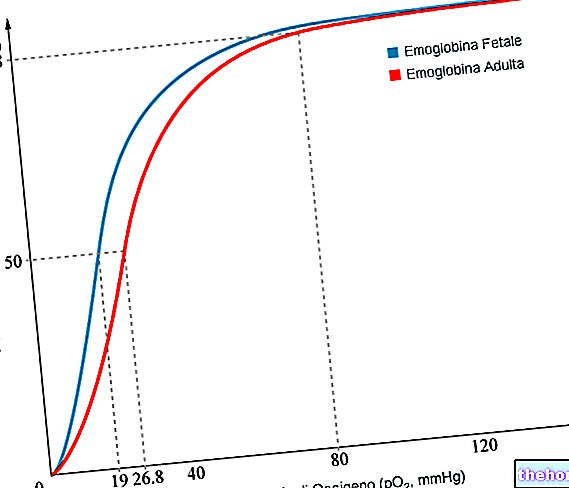
Karvea tilhører en gruppe medisiner kjent som angiotensin-II reseptorantagonister. Angiotensin-II er et stoff produsert av kroppen som binder seg til reseptorer i blodårene og får dem til å trekke seg sammen. Dette resulterer i en økning i blodtrykket. Karvea forhindrer angiotensin -II fra binding til disse reseptorene, slik at blodårene utvides og blodtrykket faller. Karvea bremser forfall av nyrefunksjon hos pasienter med høyt blodtrykk og diabetes type 2.
Karvea brukes til voksne pasienter
- for å behandle høyt blodtrykk (essensiell arteriell hypertensjon)
- for å beskytte nyrene hos hypertensive pasienter med høyt blodtrykk, type 2 diabetes og med tegn på nedsatt nyrefunksjon på laboratorietester.
Kontraindikasjoner Når Karvea ikke skal brukes
Bruk ikke Karvea:
- dersom du er allergisk mot irbesartan eller noen av de andre innholdsstoffene i dette legemidlet
- hvis du er mer enn 3 måneder gravid (det er også bedre å unngå Karvea tidlig i svangerskapet - se avsnittet om graviditet)
- hvis du har diabetes eller nedsatt nyrefunksjon, og du blir behandlet med en blodtrykkssenkende medisin som inneholder aliskiren
Forholdsregler for bruk Hva du må vite før du bruker Karvea
Snakk med legen din før du tar Karvea hvis du har noen av følgende tilstander:
- overdreven oppkast eller diaré
- hvis du lider av nyreproblemer
- hvis du lider av hjerteproblemer
- hvis du tar Karvea for diabetiske nyresykdommer. I dette tilfellet kan legen din bestille regelmessige blodprøver, spesielt for å måle kaliumnivået i serum ved dårlig nyrefunksjon.
- hvis du må opereres (opereres) eller ta bedøvelsesmidler
- hvis du tar noen av følgende medisiner som brukes til å behandle høyt blodtrykk:
- en "ACE-hemmer" (f.eks. enalapril, lisinopril, ramipril), spesielt hvis du har diabetesrelaterte nyreproblemer.
- aliskiren
Legen din kan kontrollere nyrefunksjonen, blodtrykket og mengden elektrolytter (for eksempel kalium) i blodet med jevne mellomrom.
Se også informasjon under overskriften "Ikke bruk Karvea"
Du bør fortelle legen din dersom du tror du er gravid (eller hvis det er en mulighet for å bli gravid). Karvea anbefales ikke tidlig i svangerskapet og må ikke tas hvis det er mer enn 3 måneder gravid, da det kan forårsake alvorlig skade på barnet ditt hvis det brukes på det stadiet (se avsnittet om graviditet).
Barn og ungdom
Dette legemidlet bør ikke brukes til barn og ungdom ettersom sikkerhet og effekt ennå ikke er fullstendig fastslått.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Karvea
Fortell legen din eller apoteket dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler.
Legen din må kanskje endre dosen din og / eller ta andre forholdsregler: Hvis du tar en ACE -hemmer eller aliskiren (se også informasjon under overskriftene: "Ikke ta Karvea" og "Advarsler og forsiktighetsregler")
Du kan trenge blodprøver hvis du bruker:
- kaliumtilskudd
- kaliumholdige bordsalterstatninger
- kaliumsparende medisiner (for eksempel noen diuretika)
- medisiner som inneholder litium Hvis visse smertestillende midler, kalt ikke-steroide antiinflammatoriske medisiner, tas, kan effekten av irbesartan reduseres.
Med Karvea sammen med mat og drikke
Karvea kan tas med eller uten mat.
Advarsler Det er viktig å vite at:
Graviditet og amming
Svangerskap
Du bør fortelle legen din dersom du tror du er gravid (eller hvis det er en mulighet for å bli gravid); legen din vil vanligvis råde deg til å slutte å ta Karvea før du blir gravid eller så snart du vet at du er gravid, og vil råde deg til å ta en annen medisin i stedet for Karvea. tidlig graviditet og må ikke tas hvis du er mer enn 3 måneder gravid, siden det kan være forårsake alvorlig skade på babyen din hvis den tas etter den tredje måneden av svangerskapet.
Foringstid
Fortell legen din dersom du ammer eller skal begynne å amme. Karvea anbefales ikke for kvinner som ammer, og legen din kan velge en annen behandling hvis du ønsker å amme, spesielt hvis barnet er nyfødt eller ble født for tidlig.
Kjøring og bruk av maskiner
Det er ikke utført studier på evnen til å kjøre bil og bruke maskiner.
Det er usannsynlig at Karvea påvirker din evne til å kjøre bil eller bruke maskiner. Noen ganger kan det imidlertid oppstå svimmelhet eller tretthet under behandling for høyt blodtrykk. Hvis dette skjer, snakk med legen din før du kjører bil eller bruker maskiner.
Karvea inneholder laktose.
Hvis legen din har fortalt deg at du ikke tåler noen sukkerarter (f.eks. Laktose), må du kontakte legen din før du tar dette legemidlet.
Dose, metode og administrasjonstidspunkt Hvordan bruke Karvea: Dosering
Ta alltid dette legemidlet nøyaktig slik legen din har fortalt deg. Rådfør deg med lege eller apotek hvis du er i tvil.
Administrasjonsmåte
Karvea er til oral bruk. Svelg tablettene med tilstrekkelig væske (f.eks. Et glass vann). Du kan ta Karvea med eller uten mat. Prøv å ta medisinen samtidig hver dag. Behandlingen bør fortsette så lenge legen din anser det nødvendig. Nødvendig .
- Pasienter med høyt blodtrykk
Vanlig dose er 150 mg en gang daglig. Dosen kan økes til 300 mg én gang daglig, avhengig av reduksjon i blodtrykksnivået.
- Pasienter med høyt blodtrykk og diabetes type 2 med nyresykdom
Hos pasienter med høyt blodtrykk og diabetes type 2 er den angitte vedlikeholdsdosen 300 mg én gang daglig for behandling av assosiert nyresykdom.
Legen kan bestemme seg for å bruke lavere doser, spesielt i starten av behandlingen, spesielt pasienter som hemodialyse, eller hos pasienter over 75 år.
Maksimal antihypertensiv effekt bør oppnås 4-6 uker etter oppstart av behandlingen.
Bruk hos barn og ungdom
Karvea skal ikke gis til barn under 18 år. Kontakt et lege umiddelbart hvis et barn svelger tabletter.
Overdosering Hva du skal gjøre hvis du har tatt for mye Karvea
Dersom du tar for mye av Karvea
Kontakt legen din umiddelbart hvis du ved et uhell tar for mange tabletter.
Dersom du har glemt å ta Karvea
Hvis du ved et uhell har glemt å ta en dose, fortsett behandlingen som normalt. Ikke ta en dobbel dose for å gjøre opp for en glemt dose.
Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette legemidlet.
Bivirkninger Hva er bivirkningene av Karvea
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Noen av disse effektene kan være alvorlige og kan kreve legehjelp.
Som med lignende medisiner er det rapportert om sjeldne tilfeller av allergiske hudreaksjoner (rødhet, elveblest) samt lokal hevelse i ansikt, lepper og / eller tunge hos pasienter som tar irbesartan. Hvis du får noen av disse symptomene eller hvis du har problemer med å puste, må du slutte å ta Karvea og kontakte legen din umiddelbart.
Hyppigheten av bivirkninger listet nedenfor er definert ved bruk av følgende konvensjon:
Svært vanlige: kan ramme mer enn 1 av 10 personer
Vanlige: kan ramme opptil 1 av 100 personer
Mindre vanlige: kan ramme opptil 1 av 100 mennesker
Bivirkninger rapportert i kliniske studier for pasienter behandlet med Karvea var:
- Svært vanlige (kan ramme flere enn 1 av 10 personer): Hvis du har høyt blodtrykk og diabetes type 2 med nyresykdom, kan blodprøver vise forhøyede kaliumnivåer.
- Vanlige (kan forekomme hos opptil 1 av 10 personer): svimmelhet, kvalme / oppkast, tretthet og blodprøver kan vise økte nivåer av et enzym som måler muskel- og hjertefunksjon (kreatinkinase). Hos pasienter med høyt blodtrykk og diabetes type 2 med nyresykdom er det også rapportert om svimmelhet når man står opp fra en liggende eller sittende stilling, lavt blodtrykk når man står opp fra en liggende eller sittende stilling, smerter i ledd eller muskler. nivåene av et protein i de røde blodcellene (hemoglobin).
- Mindre vanlige (kan forekomme hos opptil 1 av 100 personer): økt hjertefrekvens, rødme, hoste, diaré, fordøyelsesbesvær / halsbrann, seksuell dysfunksjon (problemer knyttet til seksuell ytelse), brystsmerter.
Noen bivirkninger har blitt rapportert siden markedsføring av Karvea. Bivirkninger med ukjent frekvens er: spinnende følelse, hodepine, smakforstyrrelser, ringing i ørene, muskelkramper, smerter i ledd og muskler, unormal leverfunksjon, økte nivåer av kalium i blodet, forstyrrelser i nyrefunksjonen og betennelse i små blodkar påvirker hovedsakelig huden (en tilstand som kalles leukocytoklastisk vaskulitt). Mindre vanlige tilfeller av gulsott (gulfarging av huden og / eller det hvite i øynene) er også rapportert.
Rapportering av bivirkninger
Rådfør deg med lege eller apotek dersom du får bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Du kan også rapportere bivirkninger direkte via det nasjonale rapporteringssystemet som er oppført i vedlegg V.
Ved å rapportere bivirkninger kan du hjelpe til med å gi mer informasjon om sikkerheten til dette legemidlet.
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Ikke bruk dette legemidlet etter utløpsdatoen som er angitt på esken og blisteren etter Utløpsdatoen refererer til siste dag i måneden.
Må ikke oppbevares over 30 ° C.
Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Hva Karvea inneholder
- Virkestoff er irbesartan. Hver Karvea 300 mg tablett inneholder 300 mg irbesartan.
- Andre innholdsstoffer er: mikrokrystallinsk cellulose, kryssbundet karmellosenatrium, laktosemonohydrat, magnesiumstearat, kolloidalt hydrert silika, pregelatinisert maisstivelse og poloksamer 188
Hvordan Karvea ser ut og innholdet i pakningen
Karvea 300 mg tabletter er hvite til off-white, bikonvekse, ovale med et hjerte preget på den ene siden og tallet 2773 preget på den andre siden.
Karvea 300 mg tabletter er tilgjengelig i pakninger med 14, 28, 56 eller 98 tabletter i blisterpakninger. Enkeldose blisterpakninger på 56 x 1 tablett er også tilgjengelig for sykehusbruk.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
KARVEA 300 MG TABLETTER
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver tablett inneholder 300 mg irbesartan.
Hjelpestoff: 61,50 mg laktosemonohydrat per tablett.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Tablett.
Hvit til off-white, bikonveks, oval i form med et hjerte gravert på den ene siden og tallet 2773 preget på den andre siden.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Karvea er indisert hos voksne for behandling av essensiell arteriell hypertensjon.
Det er også indisert for behandling av nyresykdom hos voksne hypertensive pasienter med type 2 diabetes mellitus som en del av en antihypertensiv legemiddelbehandling (se pkt.5.1).
04.2 Dosering og administrasjonsmåte
Dosering
Den vanlige anbefalte start- og vedlikeholdsdosen er 150 mg én gang daglig, uavhengig av samtidig matinntak. Karvea i en dose på 150 mg en gang daglig gir generelt bedre 24 -timers blodtrykkskontroll enn 75 mg. Imidlertid kan initiering av 75 mg behandling vurderes, spesielt hos hemodialysepasienter og pasienter. Eldre pasienter over 75 år.
Hos pasienter som ikke er tilstrekkelig kontrollert med 150 mg én gang daglig, kan dosen av Karvea økes til 300 mg, eller andre antihypertensive midler kan administreres samtidig. Spesielt har tilsetning av et vanndrivende middel som hydroklortiazid vist en additiv effekt med Karvea (se pkt. 4.5).
Hos hypertensive pasienter med type 2 diabetes bør behandling startes med irbesartan 150 mg én gang daglig og økes til 300 mg én gang daglig som anbefalt vedlikeholdsdose for behandling av nyresykdom. Demonstrasjonen av nyrefordelen med Karvea hos hypertensive pasienter med type 2 diabetes er basert på studier der irbesartan ble brukt som tillegg til andre antihypertensive legemidler etter behov for å oppnå målblodtrykk (se pkt.5.1).
Spesielle populasjoner
Nyresvikt
Hos personer med nedsatt nyrefunksjon er dosering ikke nødvendig. En lavere startdose (75 mg) bør vurderes hos pasienter som gjennomgår hemodialyse (se pkt. 4.4).
Leverinsuffisiens
Hos personer med mild eller moderat leverinsuffisiens er dosering ikke nødvendig. Det er ingen kliniske data fra pasienter med alvorlig leverinsuffisiens.
Eldre pasienter
Selv om det bør vurderes å starte behandling med 75 mg hos eldre over 75 år, er det vanligvis ikke nødvendig med dosejustering.
Pediatrisk populasjon
Sikkerhet og effekt av Karvea hos barn i alderen 0 til 18 år er ikke fastslått.Tilgjengelige data er beskrevet i pkt.4.8, 5.1 og 5.2, men det kan ikke gis anbefalinger om dosering.
Administrasjonsmåte
For oral bruk.
04.3 Kontraindikasjoner
Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene (se pkt. 6.1).
Andre og tredje trimester av svangerskapet (se pkt. 4.4 og 4.6).
04.4 Spesielle advarsler og passende forholdsregler for bruk
Volumreduksjon
Hos pasienter med volum og / eller natrium som er tømt på grunn av intens vanndrivende behandling, lavt natriumdiett, diaré eller oppkast, kan det oppstå episoder med symptomatisk hypotensjon, spesielt etter administrering av den første dosen. I slike tilfeller må den underliggende tilstanden korrigeres før du starter behandling med Karvea.
Renovaskulær hypertensjon
Det er en økt risiko for alvorlig hypotensjon og nyresvikt hos personer med bilateral nyrearteriestenose, eller nyrearteriestenose med bare en fungerende nyre, behandlet med legemidler som virker i renin-angiotensinaldosteronsystemet.
Selv om dette ikke er dokumentert i Karvea-terapi, bør en lignende effekt også forventes med angiotensin-II-reseptorantagonister.
Nyresvikt og nyretransplantasjon
Periodisk overvåking av kalium- og kreatininnivået i serum anbefales når Karvea brukes hos pasienter med nedsatt nyrefunksjon. Det er ingen kliniske data om administrering av Karvea til pasienter med nyretransplantasjon nylig.
Hypertensive pasienter med diabetes type 2 og nyresykdom
I en analyse utført i studien med pasienter med avansert nyresykdom, var ikke effekten av irbesartan på nyre- og kardiovaskulære hendelser ensartet i alle undergrupper. Spesielt var de mindre gunstige hos kvinner og ikke-hvite personer (se pkt.5.1).
Hyperkalemi
Som med andre legemidler som forstyrrer renin-angiotensin aldosteronsystemet, kan det oppstå hyperkalemi under behandling med Karvea, spesielt ved tilstedeværelse av nedsatt nyrefunksjon, åpen proteinuri på grunn av diabetisk nyresykdom og / eller hjertesvikt. Nøye overvåking av serumkalium anbefales hos risikopasienter (se pkt. 4.5).
Litium
Kombinasjonen av litium og Karvea anbefales ikke (se pkt. 4.5).
Aorta- og mitralventilstenose, obstruktiv hypertrofisk kardiomyopati
Som med andre vasodilatatorer kreves spesiell oppmerksomhet hos pasienter som lider av aorta- eller mitralstenose, eller obstruktiv hypertrofisk kardiomyopati.
Primær aldosteronisme
Pasienter med primær aldosteronisme reagerer vanligvis ikke på antihypertensive legemidler som virker gjennom hemming av renin-angiotensinsystemet, og derfor anbefales ikke bruk av Karvea.
Generell
Hos pasienter hvis vaskulære tone og nyrefunksjon hovedsakelig er avhengig av aktiviteten til renin-angiotensin-aldosteronsystemet (f.eks. Pasienter med alvorlig kongestiv hjertesvikt eller med underliggende nyresykdom, inkludert nyrearteriestenose), behandling med angiotensinkonverterende enzymhemmere eller angiotensin -II -reseptorantagonister som påvirker dette systemet har vært assosiert med utbruddet av akutt hypotensjon, azotaemi, oliguri eller sjelden akutt nyresvikt. Blodtrykksfall hos pasienter med iskemisk hjertesykdom eller iskemisk kardiovaskulær sykdom kan føre til hjerteinfarkt eller hjerneslag.
Som observert for angiotensinkonverterende enzymhemmere, er irbesartan og andre angiotensinantagonister tilsynelatende mindre effektive for å senke blodtrykket hos svarte pasienter enn hos ikke-svarte pasienter, muligens på grunn av høyere forekomst. Av lav-renin-tilstander i den svarte hypertensive populasjonen (se avsnitt 5.1).
Svangerskap
Angiotensin II reseptorantagonistbehandling (AIIRAs) bør ikke startes under graviditet.En alternativ antihypertensiv behandling med en etablert sikkerhetsprofil for bruk under graviditet bør brukes for pasienter som planlegger graviditet. Med mindre fortsatt AIIRA -behandling anses som avgjørende.
Når graviditet er diagnostisert, bør behandling med AIIRA stoppes umiddelbart, og om nødvendig bør alternativ behandling startes (se pkt. 4.3 og 4.6).
Laktose
Dette legemidlet inneholder laktose. Pasienter med sjeldne arvelige problemer med galaktoseintoleranse, Lapp -laktasemangel eller glukose / galaktosemalabsorpsjon bør ikke ta denne medisinen.
Pediatrisk populasjon
Irbesartan har blitt studert i den pediatriske populasjonen mellom 6 og 16 år, men nåværende data, i påvente av tilgjengeligheten av nye, er ikke tilstrekkelige for å støtte bruken av den også hos barn (se pkt. 4.8, 5.1 og 5.2).
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Diuretika og andre antihypertensive midler: Andre antihypertensive midler kan øke den hypotensive effekten av irbesartan; Karvea har imidlertid blitt trygt administrert i kombinasjon med andre antihypertensive legemidler, som betablokkere, langtidsvirkende kalsiumkanalblokkere og tiaziddiuretika. diuretika kan føre til en tilstand av hypovolemi og risiko for hypotensjon ved oppstart av behandling med Karvea (se pkt. 4.4).
Kaliumtilskudd og kaliumsparende diuretika: basert på erfaring med bruk av andre legemidler som er aktive på renin-angiotensinsystemet, samtidig bruk av kaliumsparende diuretika, kaliumtilskudd, kaliumholdige bordsalterstatninger eller andre legemidler som kan øke kalium (f.eks. heparin) kan føre til en økning i serumkalium og anbefales derfor ikke (se pkt. 4.4).
Litium: Reversible økninger i serum litiumkonsentrasjoner og toksisitet er rapportert under samtidig administrering av litium- og angiotensinkonverterende enzymhemmere.
Lignende effekter har så langt vært veldig sjelden dokumentert med irbesartan. Derfor anbefales ikke denne kombinasjonen (se pkt. 4.4). Hvis det er et reelt behov for kombinasjonen, anbefales nøye overvåking av litiumnivåer i serum.
Ikke-steroide antiinflammatoriske legemidler: Når angiotensin II-antagonister administreres samtidig med ikke-steroide antiinflammatoriske legemidler (dvs. selektive COX-2-hemmere, acetylsalisylsyre (> 3 g / dag) og ikke-selektive ikke-steroide anti- inflammatoriske legemidler), demping av den antihypertensive effekten.
Som med ACE-hemmere kan samtidig bruk av angiotensin II-antagonister og ikke-steroide antiinflammatoriske legemidler føre til økt risiko for forverring av nyrefunksjonen, inkludert mulig akutt nyresvikt, og til en økning i serumkalium, spesielt hos pasienter med pre -eksisterende beskjeden nyrefunksjon. Kombinasjonen bør administreres med forsiktighet, spesielt hos eldre. Pasienter bør være tilstrekkelig hydrert og nyrefunksjon må overveies etter oppstart av kombinasjonsbehandling og periodisk deretter.
Ytterligere informasjon om irbesartan -interaksjoner: I kliniske studier ble farmakokinetikken til irbesartan ikke påvirket av hydroklortiazid Irbesartan metaboliseres hovedsakelig av CYP2C9 og i mindre grad via glukuronidering. Ingen signifikante farmakokinetiske eller farmakodynamiske interaksjoner ble observert etter samtidig administrering av irbesartan og warfarin, et legemiddel metabolisert av CYP2C9. Effekten av CYP2C9 -induktorer, som rifampicin, på farmakokinetikken til irbesartan er ikke evaluert.
Farmakokinetikken til digoksin ble ikke endret ved samtidig administrering av irbesartan.
04.6 Graviditet og amming
Svangerskap
Bruk av angiotensin II -reseptorantagonister (AIIRA) anbefales ikke i første trimester av svangerskapet (se pkt. 4.4). Bruk av AIIRA er kontraindisert i andre og tredje trimester av svangerskapet (se pkt. 4.3 og 4.4).
Epidemiologiske bevis på risikoen for teratogenisitet etter eksponering for ACE -hemmere i første trimester av svangerskapet har ikke vært avgjørende; en liten økning i risiko kan imidlertid ikke utelukkes. Selv om ingen kontrollerte epidemiologiske data om risiko med angiotensin II -reseptorantagonister (AIIRA) er tilgjengelige, kan en lignende risiko også eksistere for denne legemiddelklassen.En alternativ antihypertensiv behandling bør brukes for pasienter som planlegger graviditet. Med en påvist sikkerhetsprofil for bruk under graviditet med mindre fortsatt behandling med AIIRA anses som avgjørende.
Når graviditet er diagnostisert, bør behandling med AIIRA stoppes umiddelbart, og om nødvendig bør alternativ behandling startes.
Eksponering for AIIRA i andre og tredje trimester er kjent for å indusere fostertoksisitet (nedsatt nyrefunksjon, oligohydramnios, retardasjon av hodeskallen) og neonatal toksisitet (nyresvikt, hypotensjon, hyperkalemi) hos kvinner (se pkt. 5.3).
Skulle eksponering for AIIRA ha oppstått fra andre trimester av svangerskapet, anbefales ultralydkontroll av nyrefunksjon og hodeskalle.
Nyfødte hvis mødre har tatt AIIRA bør overvåkes nøye for hypotensjon (se pkt. 4.3 og 4.4).
Foringstid
Siden det ikke er tilgjengelige data om bruk av Karvea under amming, anbefales ikke Karvea, og alternative behandlinger med en bevist sikkerhetsprofil for bruk under amming foretrekkes, spesielt når du ammer nyfødte og premature.
Det er ukjent om irbesartan eller dets metabolitter skilles ut i morsmelk.
Tilgjengelige farmakodynamiske / toksikologiske data fra rotter viste utskillelse av irbesartan eller dets metabolitter i melk (for mer informasjon, se pkt. 5.3).
Fruktbarhet
Irbesartan hadde ingen effekt på fruktbarheten til behandlede rotter og deres avkom opp til doseringsnivåer som induserte de første tegnene på foreldretoksisitet (se pkt. 5.3).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Det er ikke utført studier på effekter av irbesartan på evnen til å kjøre bil og bruke maskiner Basert på dets farmakodynamiske egenskaper påvirker irbesartan neppe disse evnene. Ved kjøring eller bruk av maskiner bør det bemerkes at svimmelhet eller tretthet kan oppstå under behandling.
04.8 Bivirkninger
I placebokontrollerte kliniske studier med hypertensive pasienter var den totale forekomsten av bivirkninger hos personer behandlet med irbesartan (56,2%) sammenlignbar med den som ble sett hos personer behandlet med placebo (56,5%). Behandling på grunn av kliniske eller laboratoriebivirkninger var mindre hyppig for irbesartanbehandlede pasienter (3,3%) enn for placebobehandlede pasienter (4,5%). Forekomsten av bivirkninger var ikke doseavhengig (anbefalt doseområde), kjønn, alder, rase eller behandlingsvarighet.
Hos diabetiske hypertensive pasienter med mikroalbuminuri og normal nyrefunksjon ble ortostatisk svimmelhet og hypotensjon rapportert hos 0,5% (dvs. uvanlig) av pasientene selv, men bedre enn placebo.
Tabellen nedenfor viser de farmakologiske bivirkningene som er rapportert i placebokontrollerte kliniske studier der 1965 hypertensive pasienter fikk irbesartan. Elementer merket med en stjerne (*) refererer til bivirkninger som ble rapportert ytterligere hos> 2% av diabetiske hypertensive pasienter med kronisk nyresvikt og åpen proteinuri og hovedsakelig for placebo.
Hyppigheten av bivirkninger rapportert nedenfor er definert ved bruk av følgende konvensjon: svært vanlig (≥ 1/10); vanlig (≥ 1/100 til
Bivirkninger som er rapportert videre fra markedsføring er også listet opp Disse bivirkningene er avledet fra spontane rapporter.
Forstyrrelser i immunsystemet
Ikke kjent: overfølsomhetsreaksjoner som angioødem, utslett, urtikaria.
Metabolisme og ernæringsforstyrrelser
Ikke kjent: hyperkalemi.
Nervesystemet lidelser
Vanlige: svimmelhet, ortostatisk svimmelhet (*).
Ikke kjent: svimmelhet, hodepine.
Øre- og labyrintforstyrrelser
Ikke kjent: tinnitus.
Hjertepatologier
Mindre vanlige: takykardi.
Vaskulære patologier
Vanlig: ortostatisk hypotensjon (*).
Mindre vanlige: rødhet.
Sykdommer i luftveiene, thorax og mediastinum
Mindre vanlige: hoste.
Gastrointestinale lidelser
Vanlige: kvalme / oppkast.
Mindre vanlige: diaré, smerter / svie.
Ikke kjent: dysgeusi.
Hepatobiliære lidelser
Mindre vanlige: gulsott.
Ikke kjent: hepatitt, nedsatt leverfunksjon.
Hud og subkutant vev
Ikke kjent: leukocytoklastisk vaskulitt.
Muskel -skjelett- og bindevevssykdommer
Vanlig: muskuloskeletale smerter.
Ikke kjent: artralgi, myalgi (i noen tilfeller assosiert med økte plasmakreatinkinase -nivåer), muskelkramper.
Nyrer og urinveier
Ikke kjent: nedsatt nyrefunksjon inkludert tilfeller av nyresvikt hos risikopasienter (se pkt. 4.4).
Sykdommer i reproduktive system og bryst
Mindre vanlige: seksuell dysfunksjon.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlig: tretthet.
Mindre vanlige: brystsmerter.
Diagnostiske tester
Svært vanlige: Hyperkalemi (*) forekom oftere hos diabetespasienter behandlet med irbesartan enn hos de som ble behandlet med placebo. Hos diabetiske hypertensive pasienter med mikroalbuminuri og normal nyrefunksjon forekom hyperkalemi (≥ 5,5 mEq / L) hos 29,4% av pasientene irbesartan 300 mg gruppe og 22% av pasientene i placebogruppen. Hos diabetiske hypertensive pasienter med kronisk nyresvikt og åpen proteinuri, forekom hyperkalemi (≥ 5,5 mEq / L) hos 46,3% av pasientene i irbesartan -gruppen og 26,3% av pasientene i placebogruppen.
Vanlig: Signifikant økning i plasmakreatinkinase (1,7%) ble observert hos personer behandlet med irbesartan. Ingen av disse økningene var assosiert med identifiserbare kliniske hendelser i muskuloskeletalen. En nedgang i hemoglobin * -verdiene, som ikke er klinisk signifikant, ble observert hos 1,7% av hypertensive pasienter med avansert diabetisk nyresykdom behandlet med irbesartan.
Pediatrisk populasjon
I en randomisert klinisk studie av 318 hypertensive barn og ungdom, mellom 6 og 16 år, forekom følgende bivirkninger i løpet av tre ukers dobbeltblind fase: hodepine (7,9%), hypotensjon (2, 2%), svimmelhet (1,9%), hoste (0,9%). I den åpne 26-ukers perioden i denne kliniske studien var de hyppigste rapporterte laboratorieavvikene: økning i kreatinin (6,5%) og forhøyede CK-verdier hos 2% av behandlede barn.
04.9 Overdosering
Studier utført hos voksne personer behandlet med doser opp til 900 mg / dag i 8 uker har ikke vist tegn på toksisitet. De mest sannsynlige manifestasjonene av overdose antas å være hypotensjon og takykardi; bradykardi kan også være assosiert med overdosering. Ingen spesifikk informasjon er tilgjengelig for behandling av Karvea -overdose. Pasienten bør overvåkes nøye og behandlingen bør være symptomatisk og støttende tiltak Foreslåtte tiltak inkluderer induksjon av utslipp og / eller mageskylling Aktivt kull kan brukes ved behandling av overdose Irbesartan fjernes ikke ved hemodialyse.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: Angiotensin-II antagonister, uten tilknytning.
ATC -kode: C09C A04.
Virkningsmekanismen
Irbesartan er en potent og selektiv angiotensin-II reseptor (type AT1) antagonist som er aktiv for oral administrering. Det antas å blokkere alle AT1-medierte effekter av angiotensin-II, uansett om opprinnelsen til syntesen av angiotensin- eller ikke. II. Selektiv antagonisme for angiotensin-II (AT1) reseptorer forårsaker en økning i plasma renin og angiotensin-II nivåer og en reduksjon i plasma aldosteronkonsentrasjon. Potassemi er ikke vesentlig endret av irbesartan alene. Anbefalte doser. Irbesartan hemmer ikke ACE (kininase-II), et enzym som genererer angiotensin-II og kataboliserer bradykinin for å produsere inaktive metabolitter. Irbesartan krever ikke metabolsk aktivering for å utføre farmakologisk aktivitet.
Klinisk effekt
Hypertensjon
Irbesartan reduserer blodtrykksverdiene med minimale endringer i hjertefrekvensen. Blodtrykksreduksjon er doseavhengig for dosering én gang daglig med en trend mot et platå ved doser over 300 mg. Doser på 150-300 mg en gang daglig viste seg å kunne redusere blodtrykksverdiene målt i liggende eller sittende stilling i hele den vurderte perioden (opptil 24 timer fra siste inntak av stoffet), med høyere gjennomsnittlig nedgang på 8-13 / 5-8 mmHg (henholdsvis systoliske og diastoliske verdier) sammenlignet med de som ble oppdaget med placebo.
Toppreduksjon av blodtrykket oppnås innen 3-6 timer etter administrering, og den blodtrykkssenkende effekten opprettholdes i minst 24 timer. Ved anbefalte doser, etter 24 timer, er reduksjonen i blodtrykket fortsatt ca. 60-70%. den tilsvarende maksimale toppen for systolisk og diastolisk reduksjon. En dose på 150 mg én gang daglig ga en lav og gjennomsnittlig 24 timers antihypertensiv respons ganske lik administrering av samme mengde legemiddel i 2 doser.
Den antihypertensive effekten av Karvea er tydelig innen 1-2 uker etter behandling, med maksimal effekt oppnådd innen 4-6 uker etter oppstart av behandlingen.Den antihypertensive effekten er konstant under langtidsbehandling. Etter brå seponering av legemidlet, går blodtrykket gradvis tilbake til baseline. Ingen "rebound" effekt på blodtrykket ble observert.
De blodtrykkssenkende effektene av irbesartan og tiaziddiuretika øker. Hos pasienter som ikke er tilstrekkelig kontrollert med irbesartan alene, gir tilsetning av en lav dose hydroklortiazid (12,5 mg) til irbesartan én gang daglig ytterligere reduksjon av blodtrykket opptil maksimalt 7 -10 / 3-6 mmHg sammenlignet med placebo (henholdsvis systoliske og diastoliske verdier).
Effekten av Karvea påvirkes ikke av alder eller kjønn. Som med andre legemidler som påvirker renin-angiotensinsystemet, har svart hypertensive pasienter en signifikant lavere respons på irbesartan monoterapi. Når irbesartan gis i kombinasjon med en lav dose hydroklortiazid (f.eks. 12,5 mg / dag), reflekterer den antihypertensive responsen hos svarte pasienter den hos hvite pasienter.
Det er ingen klinisk relevant effekt på serum urinsyre eller urinsyreutskillelse.
Pediatrisk populasjon
Blodtrykksreduksjon med etablerte titrerte doser irbesartan på 0,5 mg / kg (lav), 1,5 mg / kg (middels) og 4,5 mg / kg (høy) ble evaluert over en periode på tre uker på 318 barn og ungdom, mellom 6 og 16 år, hypertensiv eller utsatt (diabetiker, familiehistorie med hypertensjon).
På slutten av de tre ukene var gjennomsnittlig reduksjon fra baseline i den primære effektvariabelen for å sitte nedstrøms systolisk blodtrykk (SeSBP) på 11,7 mmHg (lav dose), 9,3 mmHg (middels dose), 13,2 mgHg (høy dose). Ingen signifikante forskjeller ble observert mellom disse dosene. Den justerte gjennomsnittlige endringen i sittende nedstrøms diastolisk blodtrykk (SeDBP) var som følger: 3,8 mmHg (lav dose), 3,2 mmHg (middels dose), 5,6 mmHg (høy dose). I den påfølgende 2 -ukers perioden, hvor pasientene ble randomisert til enten aktiv substans eller placebo, hadde pasienter behandlet med placebo en økning på 2,4 mmHg i SeSBP og 2,0 mmHg i SeDBP sammenlignet med endringer på + 0,1 og - 0,3 mmHg hos de som ble behandlet med alle doser irbesartan (se pkt. 4.2).
Hypertensjon og diabetes type 2 med nyresykdom
"Irbesartan Diabetic Nephropathy Trial (IDNT)" viser at irbesartan reduserer utviklingen av nyresykdom hos pasienter med kronisk nyresvikt og åpen proteinuri. IDNT var en kontrollert, dobbeltblind, morbiditets- og dødelighetsstudie som sammenlignet Karvea, amlodipin og placebo. Langtidseffektene (gjennomsnittlig 2,6 år) av Karvea på progresjon av nyresykdom og alle forårsaker dødelighet hos 1715 hypertensive pasienter med type 2 diabetes, proteinuri ≥ 900 mg / dag og serumkreatinin mellom 1 og 3 mg / dL. Pasientene ble gradvis oppgradert fra 75 mg til en vedlikeholdsdose på 300 mg Karvea, 2,5 mg til 10 mg amlodipin eller placebo, som tolereres. pasienter i alle grupper mottok mellom 2 og 4 antihypertensive legemidler (f.eks. diuretika, betablokkere, alfablokkere) for å oppnå et målblodtrykk ≤ 135/85 mmHg eller en 10 mmHg reduksjon i systolisk BP hvis blodtrykket var> 160 mmHg. % av pasientene i placebogruppen oppnådde dette blodtrykksmålet der tallet var henholdsvis 76% og 78% i irbesartangruppen og i den amlodipinen. Irbesartan reduserte betydelig den relative risikoen for forekomst av det kombinerte primære endepunktet, inkludert dobling av serumkreatinin, nyresykdom i sluttstadiet (ESRD) eller alle årsaker til dødelighet. Omtrent 33% av pasientene i irbesartan -gruppen oppnådde det sammensatte nyre primære endepunktet sammenlignet med 39% og 41% i placebo- og amlodipingruppene [20% relativ risikoreduksjon versus placebo (p = 0,024) og 23% relativ risikoreduksjon sammenlignet med amlodipin (p = 0,006)]. Når hver komponent i det primære endepunktet ble analysert individuelt, ble det ikke observert noen effekt på dødelighet av alle årsaker, mens det var en positiv trend i ESRD-reduksjon og en signifikant reduksjon i dobling av serumkreatinin.
Undergrupper ble analysert basert på kjønn, rase, alder, diabetesens varighet, blodtrykk ved baseline, serumkreatinin og albuminutskillelsesrate for å bekrefte effekt. Hos kvinner og svarte pasienter utgjorde de henholdsvis 32 % og 26 % av totalt studiepopulasjon, var det ingen nyrefunksjon, selv om konfidensintervaller ikke utelukket det. Når det gjelder det sekundære endepunktet for fatale og ikke-fatale kardiovaskulære hendelser, ble det ikke observert noen forskjell. mellom de tre gruppene i den totale befolkningen, men i irbesartangruppen , sammenlignet med placebogruppen, ble det observert en "økt forekomst av ikke-dødelig MI hos kvinner og en nedgang i forekomsten hos menn. Hos kvinner i irbesartangruppen, sammenlignet med amlodipin., økte forekomsten av ikke-dødelig MI og hjerneslag ble observert, mens sykehusinnleggelse på grunn av hjertesvikt ble redusert i befolkningen Total.
Imidlertid ble det ikke identifisert noen forklaring på disse funnene hos kvinner.
Studien "Irbesartans effekter på mikroalbuminuri hos hypertensive pasienter med type 2 diabetes mellitus (IRMA 2)" viser at irbesartan 300 mg reduserer progresjonen til åpen proteinuri hos pasienter med mikroalbuminuri. IRMA 2 var en sykdomsstudie, placebokontrollert, dobbeltblind, hos 590 pasienter med type 2 diabetes, mikroalbuminuri (30-300 mg / dag) og normal nyrefunksjon (serumkreatinin ≤ 1,5 mg / dl hos menn og 300 mg / dag og en økning i UAER på minst 30% fra baseline) . Standard blodtrykksmål var ≤ 135/85 mmHg. Ytterligere antihypertensive legemidler (unntatt ACE-hemmere, angiotensin-II reseptorantagonister og kalsiumdihydropyridinantagonister) ble tilsatt etter behov for å oppnå ønsket blodtrykk. Mens lignende blodtrykk var oppnådd i alle grupper, færre individer i irbesartan 300 mg -gruppen (5,2%) enn hos Placebo (14,9%) eller irbesartan 150 mg gruppe (9,7%) oppnådde det åpenbare proteinuri -endepunktet, og viste en 70%relativ risikoreduksjon sammenlignet med placebo (p = 0,0004) for høyere doser. I løpet av de tre første månedene av behandlingen ble det ikke observert noen parallell forbedring i glomerulær filtrasjonshastighet (GFR). Sakte progresjon til klinisk proteinuri var tydelig allerede på tre måneder og fortsatte over en toårsperiode.
Regresjon til normoalbuminuri (
05.2 Farmakokinetiske egenskaper
Etter oral administrering absorberes irbesartan godt: studier av absolutt biotilgjengelighet ga verdier på omtrent 60-80%. Samtidig matinntak påvirker ikke biotilgjengeligheten av irbesartan vesentlig. Proteinbinding er omtrent 96%, med en ubetydelig mengde binding til blodceller. Distribusjonsvolumet er 53-93 liter. Etter oral eller intravenøs administrering av 14C-merket irbesartan kan 80-85% av den påviste radioaktiviteten skyldes uendret irbesartan Irbesartan metaboliseres av leveren ved oksidasjon og glukuronokonjugasjon. Den mest representerte sirkulerende metabolitten (ca. 6%) er irbesartan glukuronid. . utdanning in vitro indikerer at irbesartan primært oksideres via cytokrom P450-isoenzym CYP2C9. CYP3A4 isoenzym har en ubetydelig effekt.
Irbesartan viser lineær og dose proporsjonal farmakokinetikk over doseområdet 10 til 600 mg. En mindre enn proporsjonal økning i oral absorpsjon ble observert ved doser over 600 mg (to ganger maksimal anbefalt dose); mekanismen for dette er ukjent. Høyeste plasmakonsentrasjon oppnås 1,5-2 timer etter oral administrering. Total kropps- og nyreclearance er henholdsvis 157-176 og 3-3,5 ml / min. Den endelige eliminasjonshalveringstiden for irbesartan er 11-15 timer. Steady-state plasmakonsentrasjoner oppnås innen 3 dager etter initiering av dosering en gang daglig Redusert akkumulering av irbesartan (plasma etter gjentatt dosering daglig. I en studie ble det observert noe høyere plasmakonsentrasjoner hos hypertensive pasienter., Var det ingen forskjell i halveringstid eller akkumulering av irbesartan. Ingen dosejustering er nødvendig hos pasienter Irbesartan AUC og Cmax-verdier var også noe høyere hos eldre pasienter (≥ 65 år) enn hos unge personer (18-40 år). terminal halveringstid ble ikke signifikant endret. Ingen dosejustering er nødvendig hos eldre pasienter.
Irbesartan og dets metabolitter elimineres både via galde og nyre. Etter oral eller intravenøs administrering av 14C-irbesartan gjenvinnes omtrent 20% av radioaktiviteten i urinen, og resten kan påvises i avføringen. Mindre enn 2% av dosen som tas tas ut i urinen som uforandret irbesartan.
Pediatrisk populasjon
Farmakokinetikken til irbesartan ble evaluert hos 23 hypertensive barn etter én og flere administrasjoner av daglige doser irbesartan (2 mg / kg) opptil en maksimal daglig dose på 150 mg i fire uker. Av de 23 barna ble 21 evaluert for sammenligning med voksen farmakokinetikk (tolv barn var over 12 år, ni var mellom 6 og 12 år). Resultatene viste at Cmax-, AUC- og clearance -nivåer var sammenlignbare med de som ble observert hos voksne pasienter administrert irbesartan 150 mg per dag. En begrenset akkumulering av irbesartan i plasma (18%) ble observert etter en daglig dose gjentatt én gang.
Nyresvikt
Hos personer med nedsatt nyrefunksjon eller hemodialyse endres de farmakokinetiske parametrene til irbesartan ikke signifikant. Irbesartan fjernes ikke under hemodialyseprosessen.
Leverinsuffisiens
Hos personer med mild til moderat levercirrhose er de farmakokinetiske parametrene til irbesartan ikke signifikant endret.
Det er ikke utført studier på pasienter med alvorlig nedsatt leverfunksjon.
05.3 Prekliniske sikkerhetsdata
Det er ingen tegn på unormalt målorgan eller systemisk toksisitet ved klinisk passende doser.
I prekliniske sikkerhetsstudier forårsaket høye doser irbesartan (≥ 250 mg / kg / dag hos rotter og ≥ 100 mg / kg / dag hos makaker) en reduksjon i parametere for røde blodlegemer (erytrocytter, hemoglobin, hematokrit). Ved svært høye doser (≥ 500 mg / kg / dag) ble degenerative endringer i nyrene (som interstitiell nefritt, tubulær distensjon, basofile tubuli, økt plasmakurea og kreatininkonsentrasjoner) indusert av irbesartan hos rotter og makaker og anses å være sekundære til den hypotensive effekten av stoffet som fører til redusert nyreperfusjon. Videre induserte irbesartan hyperplasi / hypertrofi av juxtaglomerulære celler (hos rotter ≥ 90 mg / kg / dag, hos makaker ≥ 10 mg / kg / dag). Alle disse endringene ble ansett å være forårsaket av den farmakologiske virkningen av irbesartan. Ved terapeutiske doser av irbesartan hos mennesker, synes ikke renal juxtaglomerulær cellehyperplasi / hypertrofi å være relevant.
Ingen mutagenisitet, klastogenisitet eller kreftfremkallende effekter ble påvist.
Fertilitet og reproduksjonsevne ble ikke påvirket i studier på hann- og hunnrotter selv ved doser av irbesartan som forårsaket noen foreldretoksisitet (50 til 650 mg / kg / dag), inkludert dødelighet ved den høyeste dosen. Ingen signifikante effekter ble observert på antall corpora lutei, implantater eller levende fostre. Irbesartan påvirket ikke avkomets overlevelse, utvikling eller reproduksjon. Dyrestudier indikerer at radiomerket Irbesartan er påvist hos fostre til rotter og kaniner.
Irbesartan utskilles i melken til diegivende rotter.
Dyrestudier med irbesartan viser forbigående toksiske effekter (utvidelse av nyrebekken, hydroureter og subkutant ødem) hos rottefostre, som går tilbake etter fødselen. Abort eller tidlig embryoresorpsjon ble rapportert hos kaniner i doser assosiert med signifikant mors toksisitet, inkludert død. Ingen teratogene effekter ble observert verken hos rotter eller kaniner.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Mikrokrystallinsk cellulose
Tverrbundet natriumkarmellose
Laktosemonohydrat
Magnesiumstearat
Kolloidalt silika hydrater
Pregelatinisert maisstivelse
Poloksamer 188
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
3 år.
06.4 Spesielle forholdsregler for lagring
Må ikke oppbevares over 30 ° C.
06.5 Emballasje og innhold i pakningen
Kartonger med 14 tabletter: 1 blister av PVC / PVDC / aluminium med 14 tabletter.
Kartonger med 28 tabletter: 2 PVC / PVDC / aluminiumsblister med 14 tabletter.
Kartonger med 56 tabletter: 4 blister av PVC / PVDC / aluminium med 14 tabletter.
Kartonger med 98 tabletter: 7 PVC / PVDC / aluminiumsblister med 14 tabletter.
Kartonger med 56 x 1 tablett: 7 perforerte endoseblister i PVC / PVDC / aluminium på 8 x 1 tablett.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Det ubrukte produktet og avfallet fra dette legemidlet må kastes i henhold til lokale forskrifter.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
BRISTOL-MYERS SQUIBB PHARMA EEIG
Uxbridge Business Park
Sanderson Road
Uxbridge UB8 1DH - Storbritannia
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
EU/1/97/049/007 - AIC n. 033263070
EU/1/97/049/008 - AIC n.033263082
EU/1/97/049/009 - AIC n.033263094
EU/1/97/049/012
EU/1/97/049/015
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Dato for første godkjenning: 27. august 1997
Dato for siste fornyelse: 27. august 2007
10.0 DATO FOR REVISJON AV TEKSTEN
Juni 2011