Aktive ingredienser: Acetorphane
Tiorfix 100 mg kapsler
Tiorfix pakningsinnsatser er tilgjengelige for pakningsstørrelser:- Tiorfix 10 mg granulat til oral suspensjon
- Tiorfix 30 mg granulat til oral suspensjon
- Tiorfix 100 mg kapsler
Indikasjoner Hvorfor brukes Tiorfix? Hva er den til?
Tiorfix er et legemiddel for behandling av diaré.
Tiorfix brukes til symptomatisk behandling av akutt diaré hos barn over tre måneder. Det må være forbundet med inntak av rikelig væske og med vanlige kostholdstiltak, når disse tiltakene alene ikke er tilstrekkelig effektive for å kontrollere diaré, og når årsakssammenheng ikke er mulig.
Racecadotril kan gis som en komplementær behandling når årsakssammenheng er mulig.
Kontraindikasjoner Når Tiorfix ikke skal brukes
Ikke ta Tiorfix
Dersom du er allergisk (overfølsom) overfor racecadotril eller noen av de andre innholdsstoffene i Tiorfix
Forholdsregler for bruk Hva du trenger å vite før du tar Tiorfix
Snakk med legen din eller apoteket før du tar Tiorfix. Fortell legen din dersom:
- Han finner blod eller pus i avføringen og har feber. Årsaken til diaréen kan være en "bakteriell infeksjon som må behandles av legen.
- Lider av kronisk diaré eller diaré forårsaket av antibiotika,
- Lider av nyresykdom eller nedsatt leverfunksjon,
- Lider av langvarig eller ukontrollert oppkast,
- Du har laktoseintoleranse (se "Viktig informasjon om noen av ingrediensene i Tiorfix").
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Tiorfix
Fortell legen din dersom du bruker eller nylig har brukt andre legemidler, inkludert reseptfrie legemidler.
Advarsler Det er viktig å vite at:
Graviditet, amming og fruktbarhet
Hvis du er gravid, tror du kan være gravid eller ammer, anbefales ikke bruk av Tiorfix.
Rådfør deg med lege eller apotek før du bruker dette legemidlet.
Kjøring og bruk av maskiner
Tiorfix har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner.
Viktig informasjon om noen av ingrediensene i Tiorfix
Tiorfix inneholder laktose (en sukkertype). Hvis legen din har fortalt deg at du ikke tåler noen sukkerarter, må du kontakte legen din før du tar Tiorfix.
Denne medisinen inneholder ikke gluten.
Dose, metode og administrasjonstidspunkt Hvordan bruke Tiorfix: Dosering
Tiorfix leveres i form av kapsler.
Ta alltid dette legemidlet nøyaktig slik legen din har fortalt deg. Rådfør deg med lege eller apotek hvis du er i tvil.
Den vanlige dosen er en kapsel tre ganger om dagen for å svelges med et glass vann.
Tiorfix bør helst tas før hovedmåltider, men ved starten av behandlingen kan du ta en kapsel Tiorfix når som helst på dagen.
Legen din vil fortelle deg hvor lenge du skal fortsette behandlingen med Tiorfix. Det bør fortsette til to normale fekale utslipp er produsert, senest 7 dager.
For å kompensere for væsketap på grunn av diaré, bør dette legemidlet brukes sammen med "tilstrekkelig væske- og salt (elektrolytt) tilskudd. Det beste væske- og salttilskuddet oppnås med en såkalt oral rehydratiseringsløsning (hvis du er i tvil, vennligst kontakt lege). spør legen din eller apoteket).
Ingen dosejustering er nødvendig hos eldre.
Barn
For spedbarn og barn er andre formuleringer av Tiorfix tilgjengelig.
Overdosering Hva du skal gjøre hvis du har tatt for mye Tiorfix
Kontakt lege eller apotek umiddelbart hvis du har tatt mer Tiorfix enn du burde.
Dersom du har glemt å ta Tiorfix
Ikke ta en dobbel dose for å gjøre opp for en glemt dose. Fortsett behandlingen som normalt
Bivirkninger Hva er bivirkningene av Tiorfix
Som alle medisiner kan Tiorfix forårsake bivirkninger, men ikke alle får det.
Den vanligste bivirkningen er hodepine (påvirker 1 til 10 brukere av 100).
Følgende uvanlige bivirkninger er rapportert (de rammer 1 til 10 brukere av 1000): tonsillitt (betennelse i amygdalen), utslett og erytem (rødhet i huden).
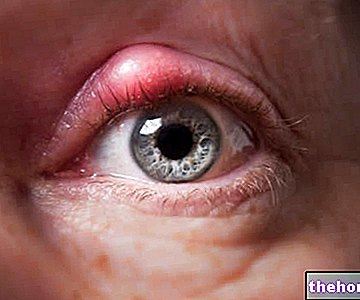
Andre bivirkninger (hvis frekvens ikke kan estimeres ut fra tilgjengelige data) er: erythema multiforme (rosa lesjoner i ekstremiteter og inne i munnen), betennelse i tungen, betennelse i ansiktet, betennelse i leppene, betennelse i øyelokkene, angioødem (subkutan betennelse i forskjellige deler av kroppen), urticaria , erythema nodosum (betennelse i form av en klump under huden), papulær utslett (hudutslett med små, harde, klumpete lesjoner), prurigo (kløende hudskader), kløe (generell kløende følelse).
Slutt å gi Tiorfix til barnet ditt umiddelbart og kontakt legen din umiddelbart hvis barnet ditt viser symptomer på angioødem, for eksempel:
- hovent ansikt, tunge eller svelg
- problemer med å svelge
- elveblest og pustevansker
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Oppbevares utilgjengelig for barn.
Ikke bruk Tiorfix etter utløpsdatoen som er angitt på sekundæremballasjen etter "EXP". Utløpsdatoen refererer til den siste dagen i måneden.
Legemidler skal ikke kastes i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Denne medisinen krever ingen spesielle oppbevaringsbetingelser.
Les pakningsvedlegget før bruk.
Hva inneholder Tiorfix
Den aktive ingrediensen er racecadotril. Hver kapsel inneholder 100 mg racecadotril.
Andre innholdsstoffer er: laktosemonohydrat, pregelatinisert maisstivelse, magnesiumstearat og vannfritt kolloidalt silika. Kapslen inneholder gelatin, gult jernoksid (E 172) og titandioksid (E171).
Beskrivelse av hvordan Tiorfix ser ut og innholdet i pakningen
Tiorfix kommer i form av harde elfenbenskapsler.
Hver pakke inneholder 6, 10, 20, 100 eller 500 harde kapsler. Pakninger med 100 eller 500 kapsler er kun til sykehusbruk.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
TIORFIX 100 MG HARDE KAPSULER
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver kapsel inneholder 100 mg racecadotril.
Hjelpestoffer: Hver kapsel inneholder 41 mg laktosemonohydrat.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Kapsel, hard.
Elfenbensfargede kapsler. Størrelse 2, som inneholder et hvitt pulver med svovellukt.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
TIORFIX 100 mg er indisert for symptomatisk behandling av akutt diaré hos voksne når årsakssammenheng ikke er mulig.
Hvis årsaksbehandling er mulig, kan racekadotril gis som en komplementær behandling.
04.2 Dosering og administrasjonsmåte
For oral bruk.
Voksne:
Opprinnelig en kapsel når som helst på dagen. Deretter en kapsel tre ganger om dagen, helst før hovedmåltider. Behandlingen bør fortsette til to normale fekale utslipp er produsert.
Behandlingen bør ikke overstige 7 dager.
Langtidsbehandling med racecadotril anbefales ikke.
Spesielle populasjoner:
Barn: Spesifikke formuleringer er tilgjengelige for spedbarn, barn og ungdom.
Eldre: Ingen dosejustering er nødvendig for eldre (se pkt. 5.2).
Forsiktighet anbefales hos pasienter med nedsatt lever- eller nyrefunksjon.
04.3 Kontraindikasjoner
Overfølsomhet overfor virkestoffene eller overfor noen av hjelpestoffene.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Forholdsregler for bruk:
Administrering av racecadotril endrer ikke de vanlige rehydreringsregimene.
Tilstedeværelsen av blodig eller purulent avføring og feber kan indikere tilstedeværelsen av invasive bakterier som er ansvarlige for diaré eller tilstedeværelsen av andre alvorlige tilstander. Derfor bør racecadotril ikke administreres i nærvær av slike forhold.
Kronisk diaré er ikke tilstrekkelig studert med dette legemidlet. Videre har racecadotril ikke blitt testet hos pasienter med antibiotikarelatert diaré.
Det er begrensede data om pasienter med nedsatt nyre- eller leverfunksjon. Disse pasientene bør behandles med forsiktighet (se pkt. 5.2).
Redusert tilgjengelighet kan observeres hos pasienter med langvarige episoder med oppkast.
Advarsel:
Dette legemidlet inneholder laktose. Pasienter med sjeldne arvelige problemer med galaktoseintoleranse, Lapp-laktasemangel eller glukose-galaktosemalabsorpsjon bør ikke ta denne medisinen.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Ingen interaksjoner med andre aktive ingredienser hos mennesker har blitt beskrevet hittil.
Hos mennesker endrer ikke samtidig behandling med racecadotril og loperamid eller nifuroxazide kinetikken til racecadotril.
04.6 Graviditet og amming
Fruktbarhet:
Fertilitetsstudier utført med racecadotril hos rotter viser ingen innvirkning på fruktbarheten.
Svangerskap:
Det er ingen tilstrekkelige data fra bruk av racecadotril hos gravide. Dyrestudier har ikke vist direkte eller indirekte skadelige effekter med hensyn til graviditet, fruktbarhet, embryonal fosterutvikling, fødsel eller postnatal utvikling, men på grunn av fravær av noen spesifikke kliniske studier tilgjengelig, skal racecadotril ikke gis til gravide
Foringstid:
På grunn av mangel på informasjon om sekresjon av racecadotril i morsmelk, bør dette legemidlet ikke gis til ammende kvinner.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Racecadotril har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner.
04.8 Bivirkninger
Data er tilgjengelig fra kliniske studier med 2193 voksne pasienter med akutt diaré behandlet med racecadotril og 282 behandlet med placebo.
Bivirkningene som er oppført nedenfor, forekom hyppigere med racecadotril enn med placebo eller ble rapportert under overvåking etter markedsføring. Hyppigheten av bivirkninger er definert ved bruk av følgende konvensjon: svært vanlig (≥ 1/10), vanlig (≥ 1/100 til
Nervesystemet lidelser
Vanlig: hodepine.
Hud- og subkutant vevssykdom
Mindre vanlige: utslett, erytem.
Ikke kjent: erythema multiforme, lingualødem, ansiktsødem, leppeødem, okulært ødem, angioødem, urticaria, erythema nodosum, papulær utslett, prurigo, kløe, giftig hudutslett.
04.9 Overdosering
Det er ikke rapportert tilfeller av overdosering. Enkeltdoser større enn 2 g, tilsvarende 20 ganger den terapeutiske dosen, har blitt administrert til voksne og det er ikke rapportert om noen skadelige effekter.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: Andre antidiarrhealer.
ATC -kode: A07XA04
Racecadotril er et prodrug som må hydrolyseres til dets aktive metabolitt tiorfan, som er en hemmer av encefalinase, et cellemembranpeptidaseenzym som ligger i forskjellige vev, spesielt i tynntarmepitelet. Dette enzymet bidrar til fordøyelsen av peptider. Eksogent og nedbrytning av endogene peptider som enkefaliner Racecadotril beskytter enkefaliner mot enzymatisk nedbrytning ved å forlenge virkningen på nivået av encefalinerge synapser i tynntarmen og redusere hypersekresjon.
Racecadotril er en ren intestinal antisekretorisk aktiv ingrediens. Det bestemmer en reduksjon av intestinal hypersekresjon av vann og elektrolytter indusert av koleratoksin eller av inflammatorisk tilstand, og har ingen effekt på den basale sekretoriske aktiviteten Racecadotril har en rask antidiarrheal aktivitet, uten å endre tarmens transittid.
Racecadotril forårsaker ikke oppblåsthet i magen. I løpet av den kliniske utviklingen forårsaket racecadotril sekundær forstoppelse hos en prosentandel av pasientene som var sammenlignbare med den som ble sett ved placebo -administrering.
Ved oral administrering utføres aktiviteten utelukkende på perifert nivå, uten effekter på sentralnervesystemet.
En randomisert crossover -studie viste at racecadotril 100 mg kapsler ved terapeutisk dose (1 kapsel) eller supraterapeutisk dose (4 kapsler) ikke induserte QT / QTc -intervallforlengelse hos 56 friske frivillige (i motsetning til moxifloxacin, brukt som kontroll).
05.2 Farmakokinetiske egenskaper
Absorpsjon: Racecadotril absorberes raskt etter oral administrering.
Selv om biotilgjengeligheten til racecadotril ikke endres av mat, forsinkes toppaktiviteten med omtrent en og en halv time.
Distribusjon: I plasma, etter en oral dose C-14 merket racecadotril, var den målte radiokarboneksponeringen mer enn 200 ganger større enn blodceller og 3 ganger større enn fullblod. Legemidlet bundet derfor ikke til blodceller på signifikante nivåer. Radiokarbondistribusjonen til andre kroppsvev var moderat, som indikert av gjennomsnittlig tilsynelatende distribusjonsvolum i plasma på 66,4 kg.
Nitti prosent av den aktive metabolitten av racekadotril (tiorfan = (RS) -N- (1-okso-2- (merkaptometyl) -3-fenylpropyl) glycin er bundet til plasmaproteiner, hovedsakelig albumin.
Varigheten og omfanget av effekten av racecadotril er doseavhengig. Topp plasma -encefalinasehemming nås på omtrent 2 timer og tilsvarer 75% inhibering med en dose på 100 mg; varigheten av plasma -encefalinasehemming er omtrent 8 timer.
Metabolisme: Halveringstiden til racekadotril, beregnet som inhibering av plasmaencefalinase, er omtrent 3 timer.
Racecadotril hydrolyseres raskt til tiorfan (RS) -N- (1- okso-2- (merkaptometyl) -3-fenylpropyl) glycin, den aktive metabolitten, som igjen omdannes til inaktive metabolitter identifisert som sulfoksid S.-metyltiorfan, tiorfan S-metyl, propionsyre 2-metansosulfinylmetyl og proprionsyre 2-metylsulfanylmetyl, alle dannet med en systemisk eksponering for morsmidlet større enn 10%.
Andre mindre metabolitter ble påvist og kvantifisert i urin og avføring.
Gjentatt administrering av racecadotril forårsaker ikke akkumulering i kroppen.
Dataen in vitro indikerer at racekadotril / tiorfan og de fire store inaktive metabolittene ikke hemmer de viktigste CYP -enzym isoformene 3A4, 2D6, 2C9, 1A2 og 2C19 på klinisk relevante nivåer.
Dataen in vitro indikerer at racekadotril / tiorfan og de fire store inaktive metabolittene ikke induserer CYP -enzymisoformer (familie 3A, 2A6, 2B6, 2C9 / 2C19, familie 1A, 2E1) og UGT -konjugerte enzymer på klinisk relevante nivåer.
Racecadotril endrer ikke proteinbindingene til aktive ingredienser som er sterkt bundet til proteiner, for eksempel tolbutamid, warfarin, nifluminsyre, digoksin eller fenytoin.
Hos pasienter med leverinsuffisiens [cirrhose, Child-Pugh klasse B] viste den kinetiske profilen til den aktive metabolitten av racecadotril lignende Tmax- og T½- og Cmax (-65%) og AUC (-29%) verdier. friske fag.
Hos pasienter med alvorlig nyreinsuffisiens (kreatininclearance 11-39 ml / min) viste den kinetiske profilen til den aktive metabolitten av racecadotril lavere Cmax (-49%) og AUC (+ 16%) og T½ høyere verdier enn de som finnes hos friske frivillige (kreatininclearance> 70 ml / min).
I den pediatriske populasjonen er de farmakokinetiske resultatene de samme som hos voksne, med Cmax nådd 2 timer og 30 minutter etter dosering. Det er ingen akkumulering etter flere doser administrert hver 8. time i 7 dager.
Utskillelse: Racecadotril elimineres i form av aktive og inaktive metabolitter. Utskillelse skjer hovedsakelig via nyrene (81,4%) og, i mye mindre grad, via fekalveien (ca. 8%). Lungeveien er ikke signifikant (mindre enn 1%av dosen).
05.3 Prekliniske sikkerhetsdata
4-ukers studier av kronisk toksisitet hos aper og hunder, justert for behandlingens varighet hos mennesker, indikerer ingen effekt ved doser opptil 1250 mg / kg / dag og 200 mg / kg, tilsvarende sikkerhetsmarginer på 625 og 62 (mht. "Mann). Racecadotril var ikke immuntoksisk hos mus behandlet med racecadotril i opptil 1 måned. Lengre (1 år) eksponering hos aper viste generaliserte infeksjoner og reduserte antistoffresponser ved vaksinasjon ved en dose på 500 mg / kg / dag og ingen infeksjon / immunsuppresjon i en dose på 120 mg / kg / dag. På samme måte varierte noen infeksjon / immunparametere hos hunden som ble behandlet med 200 mg / kg / dag i 26 uker. Klinisk relevans er ukjent, se pkt.4.8
Ingen mutagene eller klastogene effekter av racecadotril ble funnet i standardtester in vitro Og in vivo.
Kreftfremkallende tester har ikke blitt utført med racecadotril ettersom legemidlet er beregnet på kortvarig behandling.
Reproduksjon og utviklingstoksisitet (studier av fruktbarhet og tidlig embryonal utvikling, prenatal og postnatal utvikling inkludert morsfunksjon, embryonal-fosterutvikling) avslørte ikke spesifikke effekter for racecadotril.
Andre prekliniske effekter (f.eks. Alvorlig anemi, muligens aplastisk, økt diurese, ketonuri, diaré) ble bare observert i tilfeller av eksponering som ble vurdert tilstrekkelig over den maksimale eksponeringen for mennesker. Den kliniske relevansen er ukjent.
Andre farmakologiske sikkerhetsstudier viste ingen skadelige effekter av racecadotril på sentralnervesystemet og på kardiovaskulære og respiratoriske funksjoner.
Hos dyr forårsaket racecadotril en økning i virkningene av butylskopolamin på tarmoverføring og på de antikonvulsive effektene av fenytoin.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Støv
Laktosemonohydrat
Pregelatinisert (mais) stivelse
Magnesiumstearat
Vannfri kolloidal silika
Kapsel
Gult jernoksid (E172)
Titandioksid (E171)
Gelé
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
3 år.
06.4 Spesielle forholdsregler for lagring
Denne medisinen krever ingen spesielle oppbevaringsbetingelser.
06.5 Emballasje og innhold i pakningen
Blisterpakninger av PVC-PVDC / aluminium.
Pakninger med 6, 10, 20 og 100 kapsler (sykehusbruk) og 500 kapsler (sykehusbruk).
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Ingen spesielle instruksjoner for destruksjon.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
BIOPROJET EUROPE LTD
29 Earlsfort Terrace,
2, Dublin
Irland
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
AIC n. 037518014 / M "100 mg harde kapsler" 6 kapsler i PVC / PVDC / AL blister
AIC n. 037518026 / M "100 mg harde kapsler" 20 kapsler i PVC / PVDC / AL blister
AIC n. 037518038 / M "100 mg harde kapsler" 100 (5x20) kapsler i PVC / PVDC / AL blister
AIC n. 037518040 / M "100 mg harde kapsler" 500 kapsler i PVC / PVDC / AL blister
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
10.0 DATO FOR REVISJON AV TEKSTEN
08/03/2013

























.jpg)