Aktive ingredienser: Botulinumtoksin type A
BOTOX® 100 Allergan Units, pulver til injeksjonsvæske, oppløsning
BOTOX® 200 Allergan Units, pulver til injeksjonsvæske, oppløsning
Hvorfor brukes Botox? Hva er den til?
Hva er BOTOX
BOTOX er et muskelavslappende legemiddel som injiseres i musklene, blæreveggen eller under huden. Det virker ved delvis å blokkere nerveimpulser i hver muskel der det injiseres og reduserer overdreven sammentrekning av disse musklene.
Når BOTOX injiseres under huden, virker det på svettekjertlene for å redusere mengden svette som produseres.
Når den injiseres i blæreveggen, virker BOTOX på blærens muskulatur for å redusere urintap (urininkontinens). Når det gjelder kronisk migrene, antas BOTOX å være i stand til å blokkere smertesignaler, som indirekte blokkerer utviklingen av migrene, men hvordan BOTOX fungerer ved kronisk migrene er ikke fullt ut forstått.
Hva er BOTOX til
Hos voksne brukes BOTOX til å kontrollere:
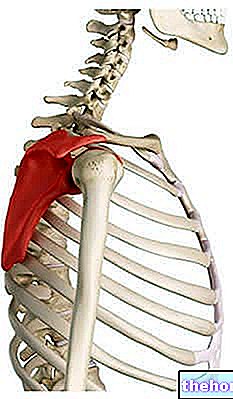
- vedvarende muskelspasmer i øyelokkene og ansiktet
- vedvarende muskelspasmer i nakke og skuldre
- vedvarende muskelspasmer i håndleddet og hånden hos slagpasienter
- overdreven svette i armhulene som forstyrrer normale daglige aktiviteter når andre lokale behandlinger ikke er nyttige
- overaktiv blære med urininkontinens - plutselig trang til å tømme blæren og behovet for å gå på do oftere enn normalt - når andre legemidler (kalt antikolinergika) ikke har hjulpet
- urininkontinens på grunn av blæresykdommer forbundet med ryggmargsskade eller multippel sklerose.
BOTOX brukes til å redusere symptomene på kronisk migrene hos voksne:
- med hodepine i 15 dager eller mer i måneden, hvorav minst 8 dager med migrene og som ikke har fått tilstrekkelig respons eller er intolerante mot legemidler mot migrene gitt for profylakse.
Kronisk migrene er en sykdom som påvirker nervesystemet. Pasienter lider vanligvis av smerter i hodet ofte ledsaget av overdreven følsomhet for lys, høye lyder eller dufter / lukter, samt kvalme og / eller oppkast. Hodet forekommer i 15 dager eller mer pr. måned BOTOX har vist seg å redusere symptomene betydelig og forbedre livskvaliteten til pasienter som lider av kronisk migrene.
BOTOX bør bare foreskrives for deg hvis du har blitt diagnostisert med kronisk migrene av en nevrolog som spesialiserer seg på dette feltet. BOTOX bør administreres under oppsyn av en nevrolog. BOTOX brukes ikke for akutt migrene, hodepine av kronisk spenningstype eller hos pasienter med overdreven bruk av hodepine.
Hos barn i alderen 2 år og over med cerebral parese som ikke er i stand til å gå, brukes BOTOX for å kontrollere:
- fotdeformitet forårsaket av vedvarende benmuskelkramper. BOTOX lindrer vedvarende muskelspasmer i beina.
Kontraindikasjoner Når Botox ikke skal brukes
Ikke bruk BOTOX
- hvis du er allergisk (overfølsom) overfor botulinumtoksin type A eller noen av de andre innholdsstoffene i BOTOX;
- hvis du har en foreslått "infeksjon på injeksjonsstedet";
- hvis du blir behandlet for urininkontinens og utvikler en "urinveisinfeksjon eller opplever" plutselig manglende evne til å tømme blæren (og ikke bruker kateter regelmessig);
- hvis du blir behandlet for urininkontinens og ikke har tenkt å bruke kateter om nødvendig.
Vær spesielt forsiktig med BOTOX
Før du bruker BOTOX
Fortell legen din dersom:
- har hatt problemer med injeksjoner tidligere (som besvimelse);
- du har betennelse i musklene eller i området på huden der legen har tenkt å injisere;
- har betydelig svakhet eller tap av muskeltonus der legen din har til hensikt å injisere;
- noen gang har hatt problemer med å svelge eller med mat eller væske ved et uhell som kommer i kontakt med lungene, spesielt hvis du blir behandlet for vedvarende muskelspasmer i nakke og skuldre;
- lider av andre muskelproblemer eller kroniske sykdommer som påvirker musklene (for eksempel myasthenia gravis eller Eaton Lambert syndrom);
- lider av visse sykdommer i nervesystemet (for eksempel amyotrofisk lateral sklerose eller motorisk nevropati);
- har en øyesykdom som kalles lukket vinkelglaukom (høyt trykk i øyet) eller har blitt fortalt at du er i fare for å utvikle denne typen glaukom;
- har hatt operasjoner eller skader som kan ha endret muskelen som skal injiseres på noen måte;
- blir behandlet for overaktiv blære med urininkontinens og er en mann som har tegn og symptomer på urinobstruksjon, for eksempel problemer med å urinere eller svak eller periodisk strømning
Etter å ha blitt behandlet med BOTOX
Kontakt legen din og få øyeblikkelig oppmerksomhet hvis følgende skjer:
- pustevansker, svelging eller evnen til å snakke;
- elveblest, hevelse inkludert hevelse i ansikt eller svelg, tungpustethet, svimmelhet og kortpustethet (mulige symptomer på alvorlig allergisk reaksjon).
Forholdsregler for bruk Det du trenger å vite før du tar Botox
Hvis du blir behandlet med BOTOX for ofte eller dosen er for høy, kan kroppen begynne å produsere antistoffer som kan redusere effekten av BOTOX.
Hvis du ikke har trent mye fysisk aktivitet på lenge før du mottok BOTOX -behandling, bør enhver aktivitet gradvis gjenopptas etter behandlingene.
Denne medisinen vil neppe forbedre bevegelsesgraden i leddene der muskelen rundt har mistet evnen til å strekke seg.
Når BOTOX brukes til behandling av vedvarende muskelspasmer i øyelokket, kan det redusere blinking og skade overflaten av øynene.For å forhindre dette kan det være nødvendig med behandling med øyedråper, oftalmiske salver, myke kontaktlinser eller til og med beskyttelsesutstyr. beskytte øyet. Legen din vil fortelle deg om dette er nødvendig.
Når du bruker BOTOX for å kontrollere urintap, må legen din gi deg antibiotika før og etter behandling for å forhindre urinveisinfeksjoner.
Legen din vil se deg ca 2 uker etter injeksjonen hvis du ikke har brukt et kateter før injeksjonen. Du blir bedt om å urinere der, og det totale volumet av urin som er igjen i blæren vil deretter bli målt ved ultralyd. Legen din vil avgjøre om du må komme tilbake for den samme testen i løpet av de neste 12 ukene. Snakk med legen din hvis du ikke kan tisse når som helst, da du kanskje må begynne å bruke et kateter. Hos pasienter med urininkontinens på grunn av blæresykdommer assosiert med ryggmargsskade eller multippel sklerose, kan omtrent en tredjedel av de som ikke brukte kateter før behandling, måtte bruke kateter etter behandling. Hos pasienter med urininkontinens på grunn av overaktiv blære, kan omtrent 6 av 100 pasienter måtte bruke kateter etter behandling.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Botox
Fortell legen din eller apoteket hvis:
- tar antibiotika (brukes til å behandle infeksjoner), antikolinesterasemedisiner, hjerterytmemedisiner eller muskelavslappende midler. Noen av disse medisinene kan øke effekten av BOTOX.
- du har nylig mottatt behandling med et legemiddel som inneholder botulinumtoksin (den aktive ingrediensen i BOTOX), da dette kan øke effekten av BOTOX kraftig.
- bruker et antiplatelet middel (produkter som ligner på aspirin) og / eller antikoagulantia (blodfortynnende midler).
Fortell legen din eller apoteket dersom du bruker eller nylig har brukt andre legemidler, inkludert reseptfrie legemidler.
Advarsler Det er viktig å vite at:
Graviditet og amming
BOTOX skal ikke brukes under graviditet og hos kvinner i fertil alder som ikke bruker prevensjon, med mindre det er klart nødvendig. Spør legen din om råd hvis du er gravid, planlegger å bli gravid eller bli gravid under behandlingen. Legen din vil diskutere med deg om du skal fortsette behandlingen.
BOTOX anbefales ikke for ammende kvinner.
Rådfør deg med lege eller apotek før du tar medisiner.
Kjøring og bruk av maskiner
BOTOX kan forårsake svimmelhet, søvnighet, tretthet eller synsproblemer. Hvis du har opplevd noen av disse effektene, må du ikke kjøre bil eller bruke maskiner. Spør legen din om råd hvis du er usikker.
Dose, metode og administrasjonstidspunkt Hvordan bruke Botox: Dosering
BOTOX skal bare injiseres av leger med spesifikke ferdigheter for bruk av medisinen.
Metode og administrasjonsvei
BOTOX injiseres i musklene (intramuskulært), i blæreveggen ved hjelp av et spesifikt instrument (cystoskop) for injeksjon i blæren eller i huden (intradermalt) Det injiseres direkte i det berørte området; legen din vil vanligvis injisere BOTOX på flere steder i hvert berørt område.
Generell informasjon om dosering
- Antall injeksjoner per muskel og dosen varierer i henhold til indikasjonene. Legen din vil imidlertid bestemme hvor mye, hvor ofte og i hvilken eller hvilke muskler du skal injisere BOTOX. Det anbefales at legen bruker den laveste effektive dosen.
- Dosering for eldre er den samme som for voksne.
Dosen av BOTOX og varigheten av effekten varierer avhengig av lidelsen du blir behandlet for. Detaljer om hver lidelse er gitt nedenfor.
Sikkerhet og effekt av BOTOX ved behandling av vedvarende muskelspasmer i øyelokket, ansiktet, nakken og skuldrene hos barn (under 12 år) er ikke påvist Sikkerhet og effekt av BOTOX ved behandling av kronisk migrene hos barn (under 18 år) har ikke blitt studert.
Sikkerhet og effekt av BOTOX ved behandling av overdreven svette i armhulen er ikke undersøkt hos barn under 12 år. Erfaring med bruk av BOTOX i behandling av overdreven svette i armhulen hos ungdom mellom 12 og 17 år er svært begrenset.
Effekten av BOTOX i denne aldersgruppen er ikke bekreftet. For mer informasjon, kontakt legen din.
Sikkerhet og effekt av BOTOX ved behandling av slagrelatert spasticitet i øvre lemmer er ikke fastslått hos barn og ungdom under 18 år.
Sikkerhet og effekt av BOTOX ved behandling av urininkontinens hos pediatriske pasienter under 18 år er ikke fastslått.
For vedvarende muskelspasmer i øyelokket og ansiktet
Dosering
I den første behandlingsøkten kan legen utføre flere injeksjoner i de berørte musklene på 1,25 til 2,5 enheter BOTOX på hvert injeksjonssted.
Maksimal dose for den første behandlingsøkten er 25 enheter per berørt område (f.eks. Per øye). For påfølgende behandlinger kan maksimal total dose økes til 100 enheter om nødvendig.
Varighet av behandlingseffekten
Du vil vanligvis se bedring innen 3 dager etter injeksjonen. Maksimal effekt blir vanligvis lagt merke til 1 til 2 uker etter behandling.
Når effekten begynner å forsvinne, kan behandlingen gjentas om nødvendig, men ikke oftere enn hver tredje måned.
For vedvarende muskelspasmer i nakke og skuldre
Dosering
Legen kan utføre flere injeksjoner i de berørte musklene opptil 50 enheter BOTOX for hvert injeksjonssted.
Maksimal dose for den første behandlingsøkten er 200 enheter. For påfølgende behandlinger kan maksimal dose økes opp til 300 enheter.
Varighet av behandlingseffekten
Du vil vanligvis se bedring innen 2 uker etter injeksjonen.
Maksimal effekt blir vanligvis lagt merke til omtrent 6 uker etter behandling.
Når effekten begynner å avta, kan behandlingen gjentas om nødvendig, men ikke oftere enn hver 10. uke.
For vedvarende muskelspasmer i håndleddet og hendene hos slagpasienter
Dosering
Legen kan utføre flere injeksjoner i de berørte musklene. Dosen og antall injeksjoner varierer basert på en rekke faktorer, inkludert dine behov, musklene som skal behandles, størrelsen på musklene, alvorlighetsgraden av spasmer, etc.
Varighet av behandlingseffekten
Du vil vanligvis se forbedring i løpet av de første 2 ukene etter injeksjonen.
Maksimal effekt blir vanligvis lagt merke til mellom 4 og 6 uker etter behandling.
Når effekten begynner å avta, kan behandlingen gjentas om nødvendig, men ikke oftere enn hver 12. uke.
For overdreven svette i armhulene
Dosering
Legen din kan gi BOTOX -injeksjoner til flere steder i aksillærområdet.Den totale dosen per armhule er 50 enheter BOTOX.
Varighet av behandlingseffekten
Du vil vanligvis se forbedring i løpet av den første uken etter injeksjonen.
Effekten varer vanligvis i gjennomsnitt 7,5 måneder etter den første injeksjonen, og omtrent 1 av 4 pasienter viser fremdeles behandlingseffekten etter ett år.
Når effekten begynner å forsvinne, kan behandlingen gjentas om nødvendig, men ikke oftere enn hver 16. uke.
For vedvarende benmuskelkramper hos barn med cerebral parese
Dosering
Legen kan utføre flere injeksjoner i de berørte musklene. Dosen avhenger av barnets vekt.
Varighet av behandlingseffekten
Du vil vanligvis se forbedring i løpet av de første 2 ukene etter injeksjonen.
Når effekten begynner å forsvinne, er det mulig å gjenta en påfølgende behandling, men ikke oftere enn hver 3. måned.Legen kan finne en dose som begrunner behandlingene med opptil 6 måneders mellomrom.
For urininkontinens på grunn av overaktiv blære
Dosering
Legen vil utføre flere injeksjoner i blæreveggen. Den totale dosen er 100 enheter BOTOX. Du kan få lokalbedøvelse før injeksjonene (blæren din blir fylt med bedøvelsesmiddel for en stund og deretter tømt.) Du kan også få et beroligende middel.
Du må vente 30 minutter etter behandlingen for å se om du klarer å urinere spontant.
Varighet av behandlingseffekten
Det er vanligvis forbedring i løpet av de første 2 ukene med injeksjoner.
Vanligvis varer effekten 5 - 6 måneder etter injeksjon.
Hvis effektene begynner å avta, kan du gå tilbake til behandlingen om nødvendig, men ikke oftere enn hver tredje måned.
For urininkontinens på grunn av blæresykdommer forbundet med ryggmargsskade eller multippel sklerose
Dosering
Legen vil utføre flere injeksjoner i blæreveggen. Den totale dosen er 200 enheter BOTOX. Du kan få lokal eller generell bedøvelse før injeksjonene. Du kan også få et beroligende middel.
Varighet av terapeutisk effekt
Du vil vanligvis se forbedring innen 2 uker etter injeksjonen.
Vanligvis varer effekten 8-10 måneder etter injeksjon.
Når effektene begynner å avta, kan du gå tilbake til behandlingen om nødvendig, men ikke oftere enn hver tredje måned.
For behandling av hodepine hos voksne som lider av kronisk migrene
Dosering
Legen din kan gi flere injeksjoner i visse muskler i ansikt, hode og nakke med opptil 5 enheter BOTOX på hvert injeksjonssted. Injeksjoner skal fordeles på 7 spesifikke muskelområder i hode / nakke med halvparten av injeksjonene gitt til venstre og halvparten på høyre side av hode og nakke.
Det totale doseringsområdet er mellom 155 og 195 enheter per behandlingsøkt.
Varighet av behandlingseffekten
Når effekten begynner å forsvinne, kan behandlingen gjentas, men ikke oftere enn hver 12. uke.
Overdosering Hva du skal gjøre hvis du har tatt for mye Botox
Tegn på overdose av BOTOX kan ikke vises på flere dager etter injeksjon. Hvis du har svelget BOTOX eller injisert det ved et uhell, bør du kontakte legen din som kan overvåke deg i flere uker.
Hvis du har fått en overdose av BOTOX, kan du ha noen av følgende symptomer, og i så fall kontakte legen din umiddelbart som vil avgjøre om du skal gå til sykehuset:
- pustevansker, svelge eller snakke på grunn av muskellammelse;
- mat eller væske ved et uhell kommer i kontakt med lungene som kan forårsake lungebetennelse (infeksjon i lungene) på grunn av muskellammelse;
- hengende øyelokk, dobbeltsyn;
- generell svakhet.
Spør lege eller apotek dersom du har ytterligere spørsmål om bruk av BOTOX.
Bivirkninger Hva er bivirkningene av Botox
Som alle legemidler kan BOTOX forårsake bivirkninger, men ikke alle får det.
Generelt oppstår bivirkninger i løpet av de første dagene etter behandling. Disse varer vanligvis bare en kort stund, men kan vare i flere måneder og i sjeldne tilfeller enda lenger.
HVIS DU HAR NOE VANNLIG VED Å Puste, svelge eller snakke etter å ha mottatt en BOTOX -BEHANDLING, KONTAKT Legen din umiddelbart.
Hvis du opplever elveblest, hevelse inkludert hevelse i ansikt eller svelg, tungpustethet, svimmelhet og kortpustethet, må du kontakte legen din umiddelbart.
Bivirkninger er klassifisert i følgende kategorier, avhengig av hvor ofte de oppstår:
Nedenfor er bivirkningene som varierer avhengig av hvilken del av kroppen BOTOX injiseres:
Injeksjoner i øyelokket og ansiktet
Svært vanlig bivirkning:
- hengende øyelokk.
Vanlige bivirkninger:
- hevelse i ansiktet;
- lokalisert hornhinneskade (klar overflate som dekker øyets front);
- problemer med å lukke øyet helt;
- overdreven rive;
- irritasjon;
- tørt øye, øyeirritasjon og lysfølsomhet;
- blåmerker under huden.
Mindre vanlige bivirkninger:
- svimmelhet;
- synsforstyrrelser;
- tåkesyn;
- dobbeltsyn;
- tretthet;
- betennelse i hornhinnen (klar overflate som dekker øyets forside);
- svakhet i ansiktsmusklene;
- avslapning av musklene på den ene siden av ansiktet;
- utslett;
- unormal bevegelse av øyelokkene innover eller utover.
Sjelden bivirkning:
- hevelse i øyelokket.
Svært sjeldne bivirkninger:
- sår, skade på hornhinnen (klar overflate som dekker øyets front);
- høyt trykk i øyet.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner i nakke og skulder
Svært vanlige bivirkninger:
- problemer med å svelge;
- smerte;
- muskel svakhet.
Vanlige bivirkninger:
- svimmelhet;
- influensa syndrom;
- døsighet
- muskel kramper;
- redusert hudfølsomhet;
- følelse av svakhet;
- følelse av generell ubehag;
- kvalme;
- hodepine;
- stivhet eller ømhet i musklene;
- hevelse og irritasjon i øvre luftveier (rhinitt);
- tett nese eller rennende nese, hoste, ondt i halsen, kiling eller irritasjon i halsen;
- tørr i munnen.
Mindre vanlige bivirkninger:
- kortpustethet;
- dobbeltsyn;
- feber;
- hengende øyelokk;
- endring av stemme.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner i håndleddet og hånden hos slagpasienter
Vanlige bivirkninger:
- muskel svakhet;
- økt muskelspenning;
- blåmerker og blødninger under huden som forårsaker røde områder (blåmerker eller purpura);
- blødning eller svie på injeksjonsstedet;
- smerter i hender og fingre;
- smerte der injeksjonen gis;
- feber;
- influensa syndrom.
Mindre vanlige bivirkninger:
- depresjon;
- redusert blodtrykk ved å stå som forårsaker svimmelhet, svimmelhet eller besvimelse;
- følelse av svimmelhet eller 'spinning' (vertigo);
- mangel på koordinering av bevegelser;
- minnetap;
- generalisert svakhet;
- smerte;
- leddsmerter eller betennelse;
- redusert hudfølsomhet;
- nummenhet eller prikking;
- hevelse i ekstremiteter som hender og føtter;
- betennelse i huden (dermatitt);
- hodepine;
- følelse av generell ubehag;
- kvalme;
- økt følsomhet på injeksjonsstedet;
- utslett;
- nummenhet eller prikking rundt munnen;
- søvnvansker (søvnløshet);
- klø.
Noen av disse uvanlige bivirkningene kan også være relatert til sykdommen din.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner for overdreven svette i armhulene
Svært vanlige bivirkninger:
- smerter på injeksjonsstedet.
Vanlige bivirkninger:
- smerter på injeksjonsstedet;
- hodepine;
- nummenhet eller prikking;
- hetetokter;
- økt svette andre steder enn armhulen;
- unormal hudlukt;
- klø;
- hårtap;
- hevelse under huden;
- smerter i ekstremiteter, for eksempel hender og fingre;
- smerte;
- reaksjoner og hevelse, blødning eller svie og økt følsomhet på injeksjonsstedet.
Mindre vanlige bivirkninger:
- muskel svakhet;
- følelse av svakhet;
- muskelsmerter;
- felles problemer;
- føler seg kvalm.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Beninjeksjoner hos barn med cerebral parese
Svært vanlige bivirkninger:
- virusinfeksjon;
- øreinfeksjon.
Vanlige bivirkninger:
- døsighet;
- muskel svakhet;
- smerter i ekstremiteter, for eksempel hender og fingre;
- problemer i gang;
- nummenhet eller prikking;
- muskelsmerter;
- urininkontinens (manglende evne til å kontrollere tømming av blæren);
- følelse av generell ubehag;
- faller;
- utslett;
- smerter på injeksjonsstedet;
- følelse av svakhet.
Det har vært sjeldne rapporter om død etter BOTOX -behandling noen ganger assosiert med aspirasjonspneumoni hos barn med cerebral parese.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner i blæreveggen for urininkontinens på grunn av overaktiv blære
Svært vanlige bivirkninger:
- urinveisinfeksjon;
- smertefull vannlating etter injeksjon *.
Vanlige bivirkninger:
- bakterier i urinen, hvite blodlegemer i urinen;
- manglende evne til å tømme blæren (urinretensjon);
- ufullstendig tømming av blæren;
- hyppig vannlating i løpet av dagen;
- blod i urinen etter injeksjon **.
* Denne bivirkningen kan også være relatert til injeksjonsprosedyren. ** Denne bivirkningen er bare relatert til injeksjonsprosedyren
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner i blæreveggen for urininkontinens på grunn av blæresykdommer forbundet med ryggmargsskade eller multippel sklerose
Svært vanlige bivirkninger:
- urinveisinfeksjon;
- manglende evne til å tømme blæren (urinretensjon).
Vanlige bivirkninger:
- søvnvansker (søvnløshet);
- forstoppelse;
- muskel svakhet;
- muskelspasme;
- blod i urinen etter injeksjoner *;
- smertefull vannlating etter injeksjoner *;
- hevelse i blæreveggen (diverticulum blære);
- tretthet;
- problemer med å gå (gangforstyrrelser);
- mulig ukontrollert refleksreaksjon av kroppen (som kraftig svette, bankende hodepine eller økt puls) omtrent i forbindelse med injeksjonene (autonom dysrefleksi) *;
- faller.
* Noen av disse vanlige bivirkningene kan også være relatert til injeksjonsprosedyren.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Injeksjoner i hode og nakke for behandling av hodepine hos pasienter som lider av kronisk migrene
Vanlige bivirkninger:
- hodepine;
- migrene;
- utslett;
- klø;
- smerter på injeksjonsstedet;
- nakkesmerter;
- svakhet i ansiktsmusklene;
- hengende øyelokk;
- muskel svakhet;
- muskelsmerter;
- muskelspasme;
- muskel sårhet;
- muskelstivhet.
Mindre vanlige bivirkninger:
- problemer med å svelge;
- hudpine;
- smerter i kjeven;
- hevelse i øyelokkene.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Generell informasjon om andre bivirkninger
Bivirkninger knyttet til spredning av BOTOX fjernt fra injeksjonsstedet har blitt rapportert svært sjelden og inkluderer:
- muskel svakhet;
- forstoppelse;
- problemer med å svelge;
- utilsiktet passering av mat eller væske til lungene som i noen tilfeller kan forårsake lungebetennelse.
Svelgeproblemer kan variere fra mild til alvorlig og krever i noen tilfeller behandling. I sjeldne tilfeller har mennesker dødd på grunn av svelgevansker.
Hjertebivirkninger har blitt rapportert sjelden:
- uregelmessig hjerterytme;
- hjerteinfarkt.
Noen av disse menneskene har gått bort. Noen av disse pasientene hadde imidlertid allerede hjerteproblemer.
Alvorlige eller umiddelbare allergiske reaksjoner er sjelden rapportert, inkludert:
- urticaria;
- hevelse inkludert hevelse i ansikt eller hals;
- skrangle;
- føler seg svak;
- kortpustethet.
Tilfeller av
- anfall eller kramper etter BOTOX -behandling, spesielt hos pasienter som tidligere har opplevd disse symptomene. Disse effektene oppstod hovedsakelig da BOTOX ble brukt til å behandle vedvarende benmuskelkramper hos barn med cerebral parese.
Som med enhver injeksjon kan bivirkninger relatert til inokulum rapporteres:
- smerte, blåmerker, blødninger eller infeksjon på injeksjonsstedet;
- nummenhet eller prikking;
- redusert hudfølsomhet;
- sårhet;
- hevelse / hevelse;
- erytem (rødhet);
- varme i blodtrykket og besvimelse forårsaket av smerte og / eller "angst for" nål. Etter BOTOX -injeksjonen hadde pasientene også:
- feber og influensalignende symptomer.
Følgende liste viser flere uønskede effekter rapportert ved bruk av BOTOX, brukt for enhver medisinsk tilstand siden den ble markedsført:
- allergisk reaksjon;
- tap av innervering til / sammentrekning av den injiserte muskelen;
- pustevansker og / eller respirasjonssvikt;
- aspirasjonspneumoni (lungebetennelse forårsaket av utilsiktet aspirasjon av mat, drikke, spytt eller oppkast);
- kronisk muskelsykdom (myasthenia gravis);
- tåkesyn;
- problemer med å se klart;
- strabismus;
- besvimelse;
- smerte / nummenhet / eller svakhet som starter i ryggraden;
- fall av musklene som påvirker en del av ansiktet;
- svakhet i muskler i ansiktet;
- vanskeligheter med å bevege armer og skuldre;
- redusert hudfølsomhet;
- muskelsmerter;
- magesmerter;
- diaré, oppkast, tap av matlyst;
- feber;
- forskjellige typer røde flekkete utslett;
- følelse av generell ubehag;
- problemer med å snakke;
- klø;
- overdreven svette;
- hårtap;
- redusert hørsel;
- ringer i øret;
- følelse av svimmelhet eller 'spinning' (vertigo);
- nummenhet eller prikking.
Rådfør deg med lege eller apotek dersom noen av bivirkningene blir alvorlige eller du merker noen bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Hold BOTOX utilgjengelig for barn.
Legen din skal ikke bruke BOTOX etter utløpsdatoen som er angitt på etiketten etter Utløpsdatoen refererer til den siste dagen i måneden.
Oppbevares i kjøleskap (2 ° C - 8 ° C), eller i fryser (-5 ° C eller lavere).
Etter rekonstituering anbefales umiddelbar bruk av løsningen; produktet kan imidlertid oppbevares i opptil 24 timer i kjøleskap (2 ° C - 8 ° C).
Sammensetning og farmasøytisk form
Hva BOTOX inneholder
- Den aktive ingrediensen er: Clostridium botulinum botulinum toxin type A. Hvert hetteglass inneholder 50, 100 eller 200 Allergan -enheter av botulinumtoksin type A.
- Andre innholdsstoffer er humant albumin og natriumklorid.
Beskrivelse av utseendet til BOTOX og innholdet i pakken
BOTOX kommer som et hvitt pulver i et hetteglass med klart glass. Før injeksjon må produktet rekonstitueres i en steril injeksjonsvæske, oppløsning av natriumklorid 9 mg / ml (0,9%).
Pakningene kan inneholde 1, 2, 3 og 6 hetteglass. I tillegg finnes BOTOX 50 og 100 Allergan -enheter av Botulinum Toxin type A i pakninger med 10 hetteglass.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
BOTOX 100 ENHETER ALLERGANPULVER FOR INJEKTERbar LØSNING
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Botulinumtoksin * type A, 100 Allergan -enheter per hetteglass.
* fra Clostridium botulinum
Botulinumtoksin -enheter er ikke utskiftbare fra ett produkt til et annet.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Pulver til injeksjonsvæske, oppløsning.
Hvitt pulver.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
BOTOX er indikert for behandlingen:
• blefarospasme, hemifacial spasme og tilhørende fokale dystonier;
• cervikal dystoni (spasmodisk torticollis);
• fokal spastisitet:
- assosiert med dynamisk klubbfoddeformitet på grunn av spastisitet hos gående pediatriske pasienter med cerebral parese, to år eller eldre;
- av håndleddet og hånden hos voksne pasienter med hjerneslag.
• Vedvarende og alvorlig primær hyperhidrose av armhulene som forstyrrer normale daglige aktiviteter og er motstandsdyktig mot lokal behandling.
• Urininkontinens hos voksne pasienter med nevrogen overaktivitet i detrusormusklen i blæren forårsaket av stabilisert lesjon av ryggmargen som starter fra livmorhalsen ned til lavere nivåer eller med multippel sklerose.
• Symptomatisk lindring hos voksne pasienter som oppfyller diagnosekriteriene for kronisk migrene (hodepine som varer ≥15 dager i måneden inkludert minst 8 dager med migrene) og som har vist utilstrekkelig respons eller er intolerante mot medisiner mot migreneprofylakse (se pkt. 4.4) .
04.2 Dosering og administrasjonsmåte
Dosering
Se de spesifikke anbefalingene for hver indikasjon beskrevet nedenfor.
Botulinumtoksin -enheter er ikke utskiftbare fra ett produkt til et annet Anbefalte doser i Allergan -enheter er forskjellige fra andre botulinumtoksinpreparater.
Følgende informasjon er viktig: Hvis pakninger med forskjellige styrker av BOTOX brukes under samme behandling, må du være spesielt forsiktig med å bruke riktig mengde fortynningsmiddel for å rekonstituere det spesifikke antallet enheter per 0,1 ml. Mengden fortynningsmiddel varierer mellom BOTOX 50 Allergan Units, BOTOX 100 Allergan Units og BOTOX 200 Allergan Units. Hver sprøyte må merkes på riktig måte.
BOTOX skal bare rekonstitueres med sterilt natriumklorid 9 mg / ml (0,9%) injeksjonsvæske, oppløsning. Riktig mengde fortynningsmiddel må trekkes opp med en sprøyte (se fortynningstabellen nedenfor).
Fortynningsinstruksjoner for 100 hetteglass med urininkontinens på grunn av nevrogen overaktivitet i blærens detrusormuskel:
• Rekonstituer to 100 enhetsflasker med BOTOX med 6 ml 0,9% salt uten salt, og bland hetteglasset forsiktig.
• Trekk 4 ml fra hvert hetteglass med to forskjellige 10 ml sprøyter.
• Trekk de resterende 2 ml fra hvert hetteglass med en tredje 10 ml sprøyte.
• fullfør rekonstitueringen ved å tilsette 6 ml konserveringsfritt 0,9% saltvann til hver av de tre 10 ml sprøyter og bland forsiktig.
Du får tre 10 ml sprøyter som inneholder totalt 200 enheter rekonstituert BOTOX.
Bruk umiddelbart etter rekonstituering i sprøyten. Kast all ubrukt saltvann.
Fortynningstabell for BOTOX 100 Allergan Unit -pakken for alle andre indikasjoner:
Dette produktet er kun til engangsbruk, og eventuell ubrukt restløsning må kastes.
For instruksjoner om bruk, håndtering og avhending av hetteglassene, se avsnitt 6.6.
Eldre pasienter
Tilstrekkelige doseringsstudier har ikke blitt utført hos eldre pasienter. Det anbefales at den laveste effektive dosen administreres med det lengste klinisk passende intervallet mellom behandlingene. Vær spesielt forsiktig hos eldre pasienter med en betydelig historie og behandlet samtidig med andre medisiner.
Pediatrisk populasjon
Sikkerhet og effekt av BOTOX ved behandling av blefarospasme, hemifacial spasme eller cervikal dystoni er ikke påvist hos barn (under 12 år).
Sikkerhet og effekt av BOTOX ved behandling av urininkontinens på grunn av nevrogen detrusoroveraktivitet er ikke fastslått hos den pediatriske populasjonen (befolkning under 18 år).
Sikkerhet og effekt av BOTOX ved behandling av kronisk migrene er ikke undersøkt hos den pediatriske populasjonen (populasjon under 18 år).
Sikkerhet og effekt av BOTOX ved behandling av primær hyperhidrose i armhulene er ikke undersøkt hos barn under 12 år. Sikkerhet og effekt av BOTOX hos ungdom mellom 12 og 17 år ved behandling av alvorlig aksillær hyperhidrose er ikke fastslått. Tilgjengelige data er beskrevet i avsnitt 4.8 og 5.1, men det kan ikke gis anbefaling om dosering (se pkt. 4.8 og 5.1).
Sikkerhet og effekt av BOTOX ved behandling av spasticitet i øvre lemmer forbundet med hjerneslag er ikke fastslått hos barn og ungdom under 18 år.
Administrasjonsmåte
Se den spesifikke anbefalingen for hver indikasjon beskrevet nedenfor.
BOTOX skal bare administreres av passende kvalifiserte leger med erfaring i håndtering og bruk av nødvendig utstyr.
Optimale nivåer av generell gyldighet er ikke fastslått for alle indikasjoner for dosering og antall injeksjonssteder i hver muskel. I disse tilfellene bør individuelle behandlingsregimer fastsettes av legen. Optimale nivåer for doseringen bør bestemmes ved titrering, men maksimal anbefalt dose bør ikke overskrides.
Blefarospasme / hemifacial spasme
Rekonstituert BOTOX skal injiseres med en steril 27-30 gauge / 0,40-0,30 mm nål. Elektromyografi veiledning er ikke nødvendig. Den anbefalte startdosen er mellom 1,25-2,5 enheter som skal injiseres i den mediale og laterale delen av orbicularis-muskelen i det øvre øyelokket og i den laterale delen av orbicularis-muskelen i det nedre øyelokket. Ytterligere steder kan injiseres i øyenbrynområdet, den laterale orbikulære muskelområdet og det øvre ansiktet hvis spasmer i disse områdene forstyrrer synet. Unngå injeksjoner i nærheten av levatorens øvre øyelokkmuskel kan redusere muligheten for å indusere ptosis Unngå injeksjoner i medial delen av det nedre øyelokket, og dermed redusere diffusjonen i den nedre skrå muskelen, kan redusere komplikasjonen av diplopi.
Generelt observeres den første effekten av injeksjonene innen tre dager og når maksimum 1-2 uker etter behandling. Hver behandling varer omtrent tre måneder, hvoretter prosedyren kan gjentas etter behov. I påfølgende økter kan dosen være økes med opptil det dobbelte hvis respons på første behandling anses som utilstrekkelig.Det ser imidlertid ut til å være liten nytte av å øke dosen utover 5 enheter per sted. Startdosen bør ikke overstige 25 enheter per øye. Normalt oppnås ingen ytterligere fordel. fra behandling oftere enn en gang hver tredje måned.
Ved behandling av blefarospasme bør den totale dosen ikke overstige 100 enheter i løpet av 12 ukers periode.
Pasienter med hemifacial spasme eller syvende nervesykdommer bør behandles på samme måte som pasienter med ensidig blefarospasme, med andre berørte ansiktsmuskler injisert etter behov.
Cervikal dystoni
Rekonstituert BOTOX skal injiseres med en nål av passende størrelse (vanligvis 25 - 30 gauge / 0,50 - 0,30 mm).
I kliniske studier bestod behandling av cervikal dystoni vanligvis av en injeksjon av BOTOX i sternocleidomastoid, levator scapula, scalene, milt i hodet, semispinal, veldig lang og / eller trapezius muskel (er). Denne listen er ikke uttømmende. alle musklene som er ansvarlige for å kontrollere posisjonen til hodet kan være involvert og krever derfor behandling.
Massen og graden av muskelhypertrofi eller atrofi er faktorer som må tas i betraktning når du velger riktig dose. Mønstre for muskelaktivering kan spontant endre seg i livmorhalskystoni uten endring i den kliniske manifestasjonen av dystoni.
Ved vanskeligheter med å isolere enkeltmusklene, må injeksjonene utføres med elektromyografisk veiledning. I de første kontrollerte kliniske studiene for å bestemme produktets sikkerhet og effekt for behandling av cervikal dystoni, varierte dosene av rekonstituert BOTOX fra 140 til 280 enheter. I nyere studier varierte dosene som ble administrert fra 95 til 360 enheter. ( i gjennomsnitt ca 240 enheter.) Som med alle andre legemidler, bør startdosen hos en ubehandlet pasient være den laveste effektive dosen. Ikke mer enn 50 enheter skal administreres på hvert sted. Ikke mer enn 100 enheter skal injiseres i sternocleidomastoid muskel For å minimere forekomsten av dysfagi bør sternocleidomastoid ikke injiseres bilateralt. Ikke mer enn 200 enheter totalt bør injiseres i den første behandlingssyklusen, og foreta passende dosejusteringer i påfølgende sykluser basert på den første responsen.
Den totale dosen på 300 enheter per enkelt økt bør ikke overskrides. Det optimale antallet injeksjonssteder avhenger av størrelsen på muskelen.
Klinisk forbedring er vanligvis sett i løpet av de to første ukene etter injeksjon.Maksimal klinisk fordel oppstår vanligvis omtrent seks uker etter injeksjon. Intervaller i behandling på mindre enn 10 uker anbefales ikke. Varigheten av den gunstige effekten i kliniske studier viste betydelig variasjon (fra 2 til 33 uker) med en typisk varighet på omtrent 12 uker.
Infantil cerebral parese
Rekonstituert BOTOX skal injiseres med en steril 23-26 gauge / 0,60 - 0,45 mm nål. Produktet administreres som en fraksjonert dose ved enkle injeksjoner i medial og lateral topp av den berørte gastrocnemius -muskelen. Ved hemiplegi er den anbefalte startdosen totalt 4 enheter / kg kroppsvekt i det berørte lemmen. Ved diplegi er den første anbefalte totaldosen 6 enheter / kg kroppsvekt fordelt på de berørte lemmene. Den totale dosen bør ikke overstige 200 enheter.
Klinisk forbedring skjer vanligvis i løpet av de to første ukene etter injeksjon.
Ytterligere doser bør gis når den kliniske effekten av forrige injeksjon reduseres, men ikke oftere enn hver tredje måned.Doseringsregimet kan justeres for å oppnå et intervall på minst seks måneder mellom påfølgende behandlingsforløp.
Fokal spastisitet i øvre lem forbundet med slag
Rekonstituert BOTOX skal injiseres med en steril 25, 27 eller 30 gauge nål for overfladiske muskler og en lengre nål for dypere muskler. For lokalisering av de berørte musklene kan det være nyttig å bruke elektromyografiske veiledningsteknikker eller nervestimulering. Flere injeksjonssteder sikrer en mer jevn kontakt med BOTOX med innerveringsområdene i muskelen og er spesielt nyttige ved større muskler.
Riktig dosering og antall injeksjonssteder må tilpasses individuelle behov basert på størrelsen, antallet og plasseringen av musklene som er involvert, alvorlighetsgraden av spastisiteten, eventuell lokal muskelsvakhet og pasientens respons på en tidligere behandling.
Følgende er dosene administrert i kontrollerte kliniske studier:
I kontrollerte og ukontrollerte åpne kliniske studier ble doser mellom 200 og 240 enheter fordelt på utvalgte muskler brukt i en bestemt behandlingssyklus.
I kontrollerte kliniske studier ble pasientene fulgt opp i 12 uker etter en enkelt behandling.
Forbedringer i muskeltonus ble sett innen 2 uker, og den største effekten ble generelt sett innen 4-6 uker.
I en pågående ukontrollert åpen studie ble de fleste pasientene retreated etter et intervall på 12-16 uker da effekten på muskeltonen ble avtagende.
Disse pasientene fikk opptil 4 inokulasjoner med en maksimal kumulativ dose på 960 enheter over 54 uker. Hvis legen finner det hensiktsmessig, kan gjentatte doser gis når effekten av den forrige injeksjonen minker. Behandling bør ikke utføres før 12 uker. Graden og typen muskelspastisitet som var tilstede på tidspunktet for rhinokulasjon kan gjøre det nødvendig med en dosering justering av BOTOX og en variant av musklene som skal behandles.
Den laveste effektive dosen bør brukes.
Primær hyperhidrose av armhulene
Rekonstituert BOTOX (100 enheter / 4 ml) injiseres med en 30 gauge nål.
50 enheter av BOTOX inokuleres intradermalt, fordelt likt på flere steder omtrent 1-2 cm "fra hverandre, i hyperhidrose av hver armhule.
Hyperhidroseområdet kan defineres ved bruk av standard fargeteknikker, for eksempel Minor stivelse-jodat-testen. Doser større enn 50 enheter per armhule kan ikke anbefales.
Klinisk forbedring skjer vanligvis innen den første uken med vaksinasjon.
BOTOX kan inokuleres på nytt når den kliniske effekten av forrige injeksjon reduseres og når behandlende lege anser det nødvendig Inokulasjoner bør ikke gjentas oftere enn hver 16. uke (se pkt. 5.1).
Urininkontinens på grunn av nevrogen overaktivitet av blæren detrusor
Pasienter bør ikke ha urinveisinfeksjoner på behandlingstidspunktet.
Antibiotika bør gis for profylakse 1-3 dager før behandling, på behandlingsdagen og 1-3 dager etter behandling.
Det anbefales at pasienter avbryter blodplatebehandling minst 3 dager før injeksjonsprosedyren. Pasienter på antikoagulant terapi må håndteres på riktig måte for å redusere risikoen for blødning.
Før injeksjonen er det mulig å utføre intravesikal instillasjon av fortynnet bedøvelsesmiddel (med eller uten sedasjon) eller fortsette med "generell anestesi, i henhold til lokal praksis på operasjonshelsetjenesten. Hvis en" lokal instillasjon av bedøvelsesmiddel utføres må blæren tømmes og vaskes med sterilt saltvann før de neste trinnene i injeksjonsprosedyren.
Den anbefalte dosen er 200 enheter BOTOX, dvs. 1 ml injeksjoner (~ 6,7 enheter) i 30 detrusormuskelsteder.
Rekonstituert BOTOX (200 enheter / 30 ml) injiseres i detrusormuskelen via et stivt eller fleksibelt cystoskop, og unngår trinen. Dyp tilstrekkelig saltvann i blæren for å oppnå en "tilstrekkelig visualisering for injeksjonene, men unngå en" overdreven distensjon.
For å fjerne all luft som er tilstede, må injeksjonsnålen fylles med ca. 1 ml oppløsning (avhengig av lengden på nålen) før injeksjonene startes.
Stikk nålen inn i detrusormusklen i ca. 2 mm og utfør 30 injeksjoner på 1 ml hver (totalt volum 30 ml) omtrent 1 cm fra hverandre (se diagram). For den siste injeksjonen, injiser ca. 1 ml fysiologisk løsning normal steril i rekkefølge for å administrere hele dosen. Når injeksjonene er utført, tøm den fysiologiske løsningen som brukes til å visualisere blæreveggen. Observer pasienten i minst 30 minutter etter injeksjonene.
Klinisk forbedring er vanligvis sett innen 2 uker. Vurder muligheten for å gjeninnføre pasienter til et nytt behandlingsforløp hvis den kliniske effekten av tidligere behandling avtar (medianvarigheten i fase III-kliniske studier var 256-295 dager for 200 enheter BOTOX), men ikke før det har gått 3 måneder siden tidligere injeksjoner i blæren.
Kronisk migrene
Diagnose av kronisk migrene og administrering av BOTOX bør bare utføres under oppsyn av nevrologer med erfaring i behandling av kronisk migrene.
Den anbefalte dosen rekonstituert BOTOX for behandling av kronisk migrene er mellom 155 og 195 enheter administrert intramuskulært (IM) via en 0,5 tommer 30 gauge nål med injeksjoner fordelt på 7 spesifikke områder av hode muskler og nakke.
Det kan være nødvendig å bruke en 1 tommers nål i livmorhalsområdet for pasienter med ekstremt tykke livmorhalsmuskler. Med unntak av procerus -muskelen, der bare ett sted (midtlinjen) skal injiseres, må alle andre muskler injiseres bilateralt, med halvparten av injeksjonene gitt til venstre og halvparten på høyre side av hodet og I tilfelle av dominerende eller smertefulle steder, er det mulig å administrere ytterligere injeksjoner på en eller begge sider i maksimalt 3 spesifikke muskelgrupper (occipital, temporal og trapezius), opptil maksimal dose per muskel.
Den anbefalte behandlingsplanen er hver 12. uke.
BOTOX dosering per muskel for kronisk migrene:
For alle indikasjoner
I tilfelle behandlingssvikt etter det første behandlingsforløpet, for eksempel fravær, en måned etter injeksjonen, av en signifikant klinisk forbedring sammenlignet med baseline, er det nødvendig å utføre følgende handlinger:
• klinisk verifisering, som kan omfatte en elektromyografisk undersøkelse i en spesialistkontekst, av toksinets virkning på den eller de injiserte musklene;
• analyse av årsakene til feil, f.eks. et dårlig valg av muskler å injisere, en utilstrekkelig dose, en feil injeksjonsteknikk, utseendet på en fast kontraktur, for svake antagonistmuskler, dannelsen av toksin -nøytraliserende antistoffer;
• revurdere hensiktsmessigheten av behandling med botulinumtoksin type A;
• ved fravær av bivirkninger sekundært til det første behandlingsforløpet, må du sette i gang et annet behandlingsforløp som følger: i) justere dosen, ta hensyn til analysen av tidligere terapisvikt, ii) bruke EMG -teknikk, og iii) observere et intervall på tre måneder mellom de to påfølgende behandlingsforløpene.
Ved terapisvikt eller redusert effekt etter gjentatte injeksjoner, bør alternative terapimetoder brukes.
04.3 Kontraindikasjoner
BOTOX er kontraindisert:
• hos personer med kjent overfølsomhet overfor botulinumtoksin type A, eller overfor noen av hjelpestoffene;
• i nærvær av infeksjon på de foreslåtte injeksjonsstedene.
BOTOX for behandling av urininkontinens på grunn av nevrogen overaktivitet i blæren detrusor er også kontraindisert:
• hos pasienter som har urinveisinfeksjoner på behandlingstidspunktet;
• hos pasienter med akutt urinretensjon på behandlingstidspunktet, som ikke rutinemessig gjennomgår kateterisering;
• hos pasienter som ikke er villige og / eller ikke kan starte kateterisering etter behandling, om nødvendig.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Før administrering av BOTOX er det nødvendig å være oppmerksom på den relative normale anatomi i det berørte området og om unormal anatomisk situasjon på grunn av tidligere kirurgi og inokulering av tidligere skadede anatomiske strukturer. Unngå alvorlige bivirkninger, inkludert dødelige utfall, hos pasienter som hadde mottatt uspesifiserte injeksjoner av BOTOX direkte i spyttkjertlene, orlo-lingual-pharyngeal regionen, spiserøret og magen Noen pasienter hadde allerede eksisterende dysfagi eller betydelig svekkelse.
Anbefalte doser og frekvenser for administrering av BOTOX bør ikke overskrides.
Alvorlige og / eller umiddelbare overfølsomhetsreaksjoner inkludert anafylaksi, serum sykdom, urtikaria, lett vevsødem og dyspné er sjelden rapportert. Noen av disse reaksjonene er rapportert etter bruk av BOTOX alene eller med andre produkter som har funnet å forårsake lignende reaksjoner.
Hvis slike reaksjoner oppstår, unngå å behandle pasienten med en ny injeksjon av BOTOX og start umiddelbart passende medisinsk behandling, for eksempel med epinefrin.Et tilfelle av anafylaksi har blitt rapportert om en pasient som døde etter injeksjon av upassende fortynnet BOTOX. Med 5 ml 1% lidokain (se "Ytterligere informasjon" i avsnitt 4.8).
Bivirkninger er rapportert på grunn av spredning av toksinet fjernt fra administrasjonsstedet (se pkt. 4.8), noen ganger med dødsfall, noen ganger assosiert med dysfagi, lungebetennelse og / eller kraftig asteni.
Pasienter behandlet med terapeutiske doser kan oppleve overdreven muskelsvakhet. Pasienter med underliggende nevrologiske lidelser, inkludert svelgevansker, har økt risiko for disse reaksjonene. Botulinumtoksinproduktet skal brukes hos disse pasientene under spesialisert tilsyn og skal bare brukes hvis fordelen med behandlingen anses å oppveie risikoen. Pasienter med tidligere dysfagi og aspirasjonspneumoni bør behandles med ekstrem forsiktighet.
Pasienter eller omsorgspersoner bør rådes til å søke øyeblikkelig hjelp ved svelging, tale eller pusteforstyrrelser.
Dysfagi er også rapportert etter inokulering på andre steder enn livmorhalsmusklene (se pkt. 4.4 "cervikal dystoni").
Kliniske svingninger ved gjentatt bruk av BOTOX (som med alle botulinumtoksiner) kan skyldes forskjellige rekonstitueringsprosedyrer for hetteglass, injeksjonsintervaller, injiserte muskler og små forskjellige potensverdier gitt av den biologiske testen som ble brukt.
Dannelsen av antistoffer som nøytraliserer botulinumtoksin type A kan redusere effektiviteten av behandling med BOTOX på grunn av inaktivering av toksinets biologiske aktivitet. Resultatene av noen studier tyder på at bruk av BOTOX med hyppigere intervaller eller ved høyere doser kan resultere i en høyere forekomst av antistoffdannelse.Når det er hensiktsmessig, kan den potensielle risikoen for antistoffdannelse minimeres ved å injisere den mest effektive dosen. Lav administrert med et lengre, klinisk passende intervall mellom behandlingene.
Som med enhver behandling som kan gjøre det mulig for pasienter som tidligere led en stillesittende livsstil å gjenoppta sine aktiviteter, bør stillesittende pasient rådes til å gjenoppta aktiviteten gradvis.
Forsiktighet bør utvises ved bruk av BOTOX i nærvær av "betennelse på stedet / stedene som er valgt for injeksjon" eller når det observeres overdreven svakhet eller atrofi i målmusklen. Forsiktighet bør utvises. Også ved bruk av BOTOX for behandling av pasienter med perifer motoriske nevropatiske sykdommer (som lateral amyotrofisk sklerose eller motorisk nevropati).
BOTOX bør brukes med særlig forsiktighet og under nøye tilsyn hos pasienter med kliniske eller subkliniske tegn på nevromuskulær overføringsdefekt, f.eks. Myasthenia gravis eller Lambert-Eaton syndrom; slike pasienter kan ha økt følsomhet overfor midler, for eksempel BOTOX, noe som kan føre til overdreven muskelsvakhet. Pasienter med nevromuskulære lidelser kan ha økt risiko for klinisk signifikante systemiske reaksjoner, inkludert alvorlig dysfagi og nedsatt luftveier med typisk BOTOX -dosering.
Som med enhver injeksjon, kan prosedyrerelatert skade oppstå. En injeksjon kan føre til lokal infeksjon, smerte, betennelse, parestesi, hypoestesi, ømhet, hevelse, erytem og / eller blødning / blåmerker. Smerter knyttet til bruk av nål og / eller angst kan føre til en vasovagal respons, for eksempel synkope, hypotensjon , etc. Vær forsiktig når du injiserer nær svake anatomiske områder.
Pneumothorax assosiert med injeksjonsprosedyren er rapportert etter administrering av BOTOX nær brystet. Vær forsiktig når du injiserer nær lungene, spesielt i det apikale området.
Pediatrisk bruk
Sikkerhet og effekt av BOTOX ved andre indikasjoner enn de som er beskrevet i pkt. 4.1 for den pediatriske populasjonen er ikke fastslått.Postmarkedsføringsrapporter om mulig fjern spredning av toksinet hos pediatriske pasienter med komorbiditet, hovedsakelig med lammelse, har blitt rapportert svært sjelden. Generelt var dosen som ble brukt i disse tilfellene over den anbefalte dosen (se pkt. 4.8).
Det har vært sjeldne rapporter om spontane dødsfall noen ganger assosiert med aspirasjonspneumoni hos barn med alvorlig cerebral parese etter behandling med botulinumtoksin, inkludert tilfeller av off-indikasjoner (f.eks. Nakkeområde) bruk. Ekstrem forsiktighet bør utvises ved behandling av pasienter som har betydelig nevrologisk svakhet, dysfagi eller nylig har hatt aspirasjonspneumoni eller lungesykdom. Behandling hos pasienter med dårlig underliggende helsetilstand bør bare utføres hvis den potensielle fordelen for pasienten anses å oppveie risikoen.
Blefarospasme
Reduksjonen i blinking forårsaket av injeksjon av botulinumtoksin i orbicularis -muskelen kan føre til eksponering av hornhinnen, vedvarende epiteldefekt og hornhinnesår, spesielt hos pasienter med 7. nervesykdom. Det er tilrådelig å utføre en grundig undersøkelse av hornhinnenes følsomhet i tidligere opererte øyne, for å unngå injeksjon i det nedre øyelokket for å unngå ektropion, og for å vedta en effektiv forebyggende behandling av eventuelle epitelfeil. Dette kan kreve bruk av øyedråper, oftalmiske salver, myke terapeutiske kontaktlinser eller lukke øyet med bandasje eller andre midler.
Blåmerker kan lett forekomme i øyelokkets bløtvev. Dette kan minimeres ved forsiktig å klemme på injeksjonsstedet umiddelbart etter injeksjonen.
På grunn av den antikolinerge aktiviteten til botulinumtoksin, bør det utvises særlig forsiktighet ved behandling av pasienter med risiko for trangvinklet glaukom, inkludert pasienter med anatomisk trange vinkler.
Cervikal dystoni
Pasienter med cervikal dystoni bør informeres om muligheten for dysfagi som kan være veldig mild, men også alvorlig. Dysfagi kan vedvare i opptil 2-3 uker etter injeksjon, men har blitt beskrevet å vare i opptil 5 måneder etter injeksjon.
Som en konsekvens av dysfagi er det mulighet for aspirasjon, dyspné og noen ganger behov for sondefôring.I sjeldne tilfeller har dysfagi etterfulgt av aspirasjonspneumoni og død blitt rapportert.
Begrensning av dosen injisert i sternocleidomastoid -muskelen til en dose under 100 enheter kan redusere forekomsten av dysfagi. Pasienter med mindre muskelmasse i nakken eller pasienter som får injeksjoner på begge sider av sternocleidomastoid -muskelen er beskrevet som økt risiko for dysfagi. Dysfagi skyldes spredning av toksinet til spiserørets muskulatur.Injeksjoner i levator scapulae -muskelen kan være forbundet med økt risiko for infeksjon i øvre luftveier og dysfagi.
Dysfagi kan bidra til å redusere mat- og vanninntak som resulterer i vekttap og dehydrering. Pasienter med subklinisk dysfagi kan ha økt risiko for alvorlig dysfagi etter BOTOX -injeksjon.
Fokal spastisitet assosiert med infantil cerebral parese og spasticitet i hånd og håndledd hos voksne pasienter etter hjerneslag
BOTOX er en behandling for fokal spastisitet som bare er studert i forbindelse med andre standardbehandlinger, og er ikke ment som en erstatning for slike terapimetoder. BOTOX vil sannsynligvis ikke være effektivt for å forbedre bevegelsesområdet i en ledd som er påvirket av vedvarende patologisk kontraktur.
Rapporter etter markedsføring av mulig spredning av toksinet hos pediatriske pasienter med komorbiditet, hovedsakelig med cerebral parese, har blitt rapportert sjelden. Generelt var dosen som ble brukt i disse tilfellene høyere enn den anbefalte (se pkt. 4.8).
Sjeldne spontane dødsrapporter som noen ganger er forbundet med aspirasjonspneumoni hos barn med alvorlig cerebral parese er rapportert etter behandling med botulinumtoksin. Spesiell forsiktighet bør utvises ved behandling av pediatriske pasienter med betydelig nevrologisk svikt, dysfagi eller en nylig historie med aspirasjonspneumoni eller lungesykdom.
Primær hyperhidrose av armhulene
Medisinsk historie og fysisk undersøkelse av pasienten, samt ytterligere undersøkelser som kan anses nødvendige, bør utføres for å utelukke mulige årsaker til sekundær hyperhidrose (f.eks. Hypertyreose, feokromocytom). Dette vil unngå symptomatiske behandlinger av hyperhidrose uten diagnose og / eller behandling av underliggende sykdommer.
Urininkontinens på grunn av neurogen detrusor -overaktivitet
Leger bør være forsiktige når de utfører cystoskopi.
Hos pasienter som ikke gjennomgår kateterisering, bør det resterende urinvolumet etter tomrom vurderes innen 2 uker etter behandling og periodisk i henhold til legens mening i opptil 12 uker. Rådfør pasienter om å konsultere legen sin hvis de opplever vannlating, ettersom kateterisering kan være nødvendig.
Autonom dysrefleksi forbundet med prosedyren kan forekomme. En øyeblikkelig kontroll av pasienten som behandles kan være nødvendig.
Kronisk migrene
Sikkerhet og effekt er ikke fastslått ved profylakse av hodepine hos pasienter med episodisk migrene (hodepine for kronisk hodepine av spenningstype. Sikkerhet og effekt av BOTOX hos pasienter med hodepine ved overdreven bruk (sekundær hodepine) er ikke undersøkt.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Teoretisk sett kan effekten av botulinumtoksin forsterkes av aminoglykosidantibiotika eller spektinomycin, eller av andre legemidler som forstyrrer nevromuskulær overføring (f.eks. Nevromuskulære blokkeringsmidler).
Effekten av samtidig administrering eller innen flere måneder etter forskjellige serotyper av botulinumneurotoksin er ikke kjent Administrering av et annet botulinumtoksin før effekten av et tidligere administrert botulinumtoksin er fullført, kan føre til forverring av nevromuskulær svakhet.
Ingen interaksjonsstudier er utført. Ingen interaksjoner av klinisk betydning ble rapportert.
04.6 Graviditet og amming
Svangerskap
Det er ingen tilstrekkelige data om bruk av botulinumtoksin type A hos gravide. Studier på dyr har vist reproduksjonstoksisitet (se pkt. 5.3). Den potensielle risikoen for mennesker er ukjent. BOTOX skal ikke brukes under graviditet og hos kvinner i fertil alder. alder som ikke bruker prevensjonsmidler med mindre det er helt nødvendig.
Foringstid
Det er ingen informasjon om utskillelse av BOTOX i melk. Bruk av BOTOX under amming anbefales ikke.
Fruktbarhet
Det er ingen tilstrekkelige data om effekten på fruktbarhet som følge av bruk av botulinumtoksin type A. hos fertile kvinner. Studier på rotter av begge kjønn har vist redusert fruktbarhet (se pkt. 5.3).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Det er ikke utført studier på evnen til å kjøre bil og bruke maskiner, men BOTOX kan imidlertid forårsake asteni, muskelsvakhet, svimmelhet og synsforstyrrelser som kan påvirke kjøring og bruk av maskiner.
04.8 Bivirkninger
Generell
I kontrollerte kliniske studier ble det rapportert om bivirkninger som forskerne trodde var relatert til BOTOX hos 35% av pasientene med blefarospasme, hos 28% av pasientene med cervikal dystoni, hos 17% av pasientene med infantil cerebral parese, hos 11% av pasientene med primær aksillær hyperhidrose og hos 16% av pasientene med fokal spastisitet i øvre lemmer assosiert med hjerneslag.I kliniske studier for urininkontinens på grunn av nevrogen overaktivitet av blæren detrusor, var forekomsten 32% med den første behandlingen og ble redusert til 18% med en andre behandling. I kliniske studier for kronisk migrene var forekomsten 26% med den første behandlingen og redusert til 11% med den andre behandlingen.
Generelt forekommer bivirkninger i løpet av de første dagene etter injeksjon, og vanligvis forbigående kan vare i flere måneder eller i sjeldne tilfeller lenger.
Lokalisert muskelsvakhet representerer den forventede farmakologiske effekten av botulinumtoksin i muskelvev.
Som forventet for enhver injeksjonsprosedyre har lokal smerte, betennelse, parestesi, hypoestesi, ømhet, hevelse / ødem, erytem, lokal infeksjon, blødning og / eller blåmerker vært assosiert med injeksjonen. Nålesmerter og / eller angst kan føre til vasovagal respons, inkludert forbigående symptomatisk hypotensjon og synkope Feber og influensasyndrom er også rapportert etter inokulering av botulinumtoksin.
Bivirkninger - frekvens etter indikasjon
Hyppigheten av bivirkninger ved indikasjon, dokumentert under kliniske studier, er gitt nedenfor.
Frekvens er definert som følger: veldig vanlig (> 1/10); vanlig (> 1/100 til 1/1000 til 1/10 000 til
Blefarospasme / hemifacial spasme
Nervesystemet lidelser
Uvanlig: svimmelhet, ansiktsparese og ansiktslammelse.
Øyesykdommer
Svært vanlig: ptosis i øyelokket.
Vanlig: punktert keratitt, lagoftalmos, tørre øyne, fotofobi, øyeirritasjon og økt tårer.
Mindre vanlige: keratitt, ektropion, diplopi, entropion, synsforstyrrelser og tåkesyn.
Sjelden: ødem i øyelokket.
Svært sjeldne: ulcerøs keratitt, endring av hornhinneepitelet, perforering av hornhinnen.
Hud og subkutant vev
Vanlige: blåmerker.
Mindre vanlige: utslett / dermatitt.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlige: ansiktsirritasjon og ødem.
Uvanlig: utmattelse.
Cervikal dystoni
Infeksjoner og angrep
Vanlig: rhinitt og infeksjon i øvre luftveier.
Nervesystemet lidelser
Vanlige: svimmelhet, hypertoni, hypoestesi, søvnighet og hodepine.
Øyesykdommer
Mindre vanlige: diplopi og øyelokkptose.
Sykdommer i luftveiene, thorax og mediastinum
Mindre vanlige: dyspné og dysfoni.
Gastrointestinale lidelser
Svært vanlige: dysfagi (se avsnittet "Ytterligere informasjon").
Vanlige: munntørrhet og kvalme.
Muskel -skjelett- og bindevevssykdommer
Svært vanlig: muskelsvakhet.
Vanlig: stivhet i muskuloskeletalen og ømhet.
Generelle lidelser og tilstander på administrasjonsstedet
Svært vanlige: smerter.
Vanlige: asteni, influensalignende symptomer og ubehag.
Mindre vanlige: feber.
Infantil cerebral parese
Infeksjoner og angrep
Svært vanlige: virusinfeksjon og ørebetennelse.
Nervesystemet lidelser
Vanlige: søvnighet, ukoordinert gange og parestesi.
Hud og subkutant vev
Vanlige: hudutslett.
Muskel -skjelett- og bindevevssykdommer
Vanlig: myalgi, muskelsvakhet og smerter i ekstremiteter.
Nyrer og urinveier
Vanlig: urininkontinens.
Skade, forgiftning og prosedyrekomplikasjoner
Vanlig: fall.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlige: ubehag, smerter på injeksjonsstedet og asteni.
Fokal spastisitet i øvre lem forbundet med slag
Psykiatriske lidelser
Mindre vanlige: depresjon og søvnløshet.
Nervesystemet lidelser
Vanlig: hypertoni.
Mindre vanlige: hypoestesi, hodepine, parestesi, mangel på koordinering og hukommelsestap.
Øre- og labyrintforstyrrelser
Mindre vanlige: svimmelhet.
Vaskulære patologier
Mindre vanlige: ortostatisk hypotensjon.
Gastrointestinale lidelser
Mindre vanlige: oral kvalme og parestesi.
Hud og subkutant vev
Vanlig: ekkymose og purpura.
Mindre vanlige: dermatitt, kløe og utslett.
Muskel -skjelett- og bindevevssykdommer
Vanlig: smerter i ekstremiteter og muskelsvakhet.
Mindre vanlige: artralgi og bursitt.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlige: smerter på injeksjonsstedet, feber, influensasyndrom, blødning og irritasjon på injeksjonsstedet.
Mindre vanlige: asteni, smerte, overfølsomhet på injeksjonsstedet, ubehag og perifert ødem.
Noen av de uvanlige hendelsene kan være relatert til sykdommen.
Primær hyperhidrose av armhulene
Nervesystemet lidelser
Vanlige: hodepine og parestesi.
Vaskulære patologier
Vanlig: hetetokter.
Gastrointestinale lidelser
Mindre vanlige: kvalme.
Hud og subkutant vev
Vanlige: hyperhidrose (ikke-aksillær svette), unormal lukt i huden, kløe, subkutan klump og alopecia.
Muskel -skjelett- og bindevevssykdommer
Vanlig: smerter i ekstremiteter.
Mindre vanlige: muskelsvakhet, myalgi og artropati.
Generelle lidelser og tilstander på administrasjonsstedet
Svært vanlige: smerter på injeksjonsstedet.
Vanlige: smerter, ødem på injeksjonsstedet, blødning på injeksjonsstedet, overfølsomhet på injeksjonsstedet, irritasjon på injeksjonsstedet, asteni og reaksjoner på injeksjonsstedet.
Ved behandling av primær aksillær hyperhidrose ble det rapportert om økt ikke-aksillær svette hos 4,5% av pasientene innen 1 måned etter inokulering, uten direkte referanse til de involverte anatomiske stedene.
Denne effekten forsvant hos omtrent 30% av pasientene innen 4 måneder.
Svakhet i øvre lemmer ble også rapportert som uvanlig (0,7%), mild, forbigående, som ikke krever behandling og løser seg uten følgetilstander. Denne bivirkningen kan være relatert til behandlingen, injeksjonsteknikken eller begge deler.I det uvanlige tilfellet med muskelsvakhet rapportert etter behandling, kan det være nødvendig med en nevrologisk undersøkelse.
Videre kan det være nødvendig å revurdere inokuleringsteknikken i påfølgende behandlinger for å sikre en intradermal posisjonering av inokulumet.
I en ukontrollert sikkerhetsstudie med BOTOX (50 U per armhule) hos pediatriske pasienter 12 til 17 år (N = 144), inkluderte bivirkninger som oppstod hos mer enn en enkelt pasient (annenhver pasient) smerter på injeksjonsstedet og hyperhidrose ( ikke-aksillær svette).
Urininkontinens på grunn av nevrogen overaktivitet av blæren detrusor
Infeksjoner og angrep
Svært vanlige: urinveisinfeksjoner.
Psykiatriske lidelser
Vanlige: søvnløshet.
Gastrointestinale lidelser
Vanlig: forstoppelse.
Muskel -skjelett- og bindevevssykdommer
Vanlig: muskelsvakhet, muskelspasmer.
Nyrer og urinveier
Svært vanlig: urinretensjon.
Vanlige: hematuri *, dysuri *, blære divertikulum.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlig: tretthet, gåforstyrrelser.
Skade, forgiftning og prosedyrekomplikasjoner
Vanlig: autonom dysrefleksi *, fall.
* prosedyrerelaterte bivirkninger
I kliniske studier ble urinveisinfeksjoner rapportert hos 49,2% av pasientene behandlet med 200 U BOTOX og hos 35,7% av pasientene behandlet med placebo (53,0% av pasientene med multippel sklerose behandlet med 200 U mot 29,3% behandlet med placebo; 45,4 % av pasientene med ryggmargsskade behandlet med 200 U sammenlignet med 41,7% behandlet med placebo). Urinretensjon ble rapportert hos 17,2% av pasientene behandlet med 200 U BOTOX og 2,9% av pasientene behandlet med placebo (28,8% av pasientene med multippel sklerose behandlet med 200 U sammenlignet med 4,5% behandlet med placebo; 5,4% av pasientene med ryggmargsskade behandlet med 200 U mot 1,4% behandlet med placebo).
Ingen endring i typen bivirkninger ble observert ved gjentatt dosering.
Det var ingen forskjell i den årlige frekvensen av multippel sklerose (MS) oppblussing (dvs. antall MS-oppblussinger per pasientår) (BOTOX = 0,23, placebo = 0,20) hos MS-pasienter i de sentrale studiene.
Blant pasienter som ikke ble kateterisert ved baseline før behandling, ble kateterisering påbegynt hos 38,9% etter behandling med 200 enheter BOTOX sammenlignet med 17,3% med placebo.
Kronisk migrene
Nervesystemet lidelser
Vanlige: hodepine, migrene, ansiktsparese.
Øyesykdommer
Vanlig: ptosis i øyelokket.
Hud og subkutant vev
Vanlige: kløe, utslett.
Mindre vanlige: Hudsmerter.
Muskel -skjelett- og bindevevssykdommer
Vanlige: nakkesmerter, myalgi, muskuloskeletale smerter, artralgi, muskuloskeletale smerter, muskelspasmer, muskelstivhet og muskelsvakhet.
Mindre vanlige: smerter i kjeven.
Generelle lidelser og tilstander på administrasjonsstedet
Vanlige: smerter på injeksjonsstedet.
Gastrointestinale lidelser
Mindre vanlige: dysfagi.
Avbrytelsesgraden på grunn av bivirkninger i disse fase III -studiene var 3,8% for BOTOX og 1,2% for placebo.
Mer informasjon
Dysfagi varierer fra mild til alvorlig, med aspirasjonspotensial som av og til krever medisinsk hjelp (se pkt. 4.4).
Bivirkninger (overdreven muskelsvakhet, dysfagi, forstoppelse, aspirasjon / aspirasjonspneumoni, med dødelig utfall i noen tilfeller) relatert til diffusjon av toksin fjernt fra administrasjonsstedet har blitt rapportert sjelden (se pkt. 4.4).
Siden medisinen har vært på markedet, har følgende andre bivirkninger blitt rapportert: muskeldenervering / atrofi; respirasjonsdepresjon og / eller respirasjonssvikt; aspirasjon lungebetennelse; dysartri; strabismus, perifer nevropati; magesmerter; tåkesyn; synsforstyrrelser; feber; lammelse i ansiktet; ansikts parese; hypoestesi; ubehag; myalgi; klø; hyperhidrose; alopecia (inkludert madarose); diaré; anoreksi; hørselstap; tinnitus; svimmelhet; radikulopati; synkope; myasthenia gravis; parestesi; erythema multiforme; psoriasiform dermatitt; oppkast og brachial plexopati.
Det har også vært sjeldne rapporter om bivirkninger som påvirker det kardiovaskulære systemet, inkludert arytmier og hjerteinfarkt, hvorav noen var dødelige. Noen av disse pasientene hadde risikofaktorer, inkludert kardiovaskulær sykdom.
Alvorlige og / eller umiddelbare overfølsomhetsreaksjoner, som anafylaksi og serum sykdom, samt andre manifestasjoner av overfølsomhet inkludert urtikaria, ødem i bløtvev og dyspné er rapportert sjelden Noen av disse reaksjonene er rapportert etter bruk av BOTOX alene eller med andre midler kjent for å forårsake lignende reaksjoner.
Lukket vinkelglaukom er rapportert svært sjelden etter botulinumtoksinbehandling for blefarospasme.
Det har vært rapporter om første eller tilbakevendende anfall, spesielt hos pasienter som er disponert for denne typen reaksjoner. Det eksakte forholdet mellom disse hendelsene og botulinumtoksininjeksjoner er ikke fastslått.
Hos barn har disse reaksjonene hovedsakelig blitt rapportert hos personer med cerebral parese behandlet for spastisitet.
Smerter forbundet med bruk av nålen og / eller angst kan forårsake en vasovagal respons.
04.9 Overdosering
Konseptet med BOTOX overdose er relativt og avhenger av dosen, injeksjonsstedet og bakgrunnskarakteristikkene til vevet. Det er ikke observert tilfeller av systemisk toksisitet etter utilsiktet inokulering av BOTOX. Overdrevne doser kan resultere i lokal eller fjern, generalisert og dyp nevromuskulær lammelse.
Det er ikke observert tilfeller av BOTOX -inntak.
Tegn og symptomer på overdosering er ikke synlige umiddelbart etter injeksjon. Ved utilsiktet injeksjon eller svelging eller mistanke om overdosering, bør pasienten overvåkes klinisk i flere uker for eventuelle tegn og symptomer på muskelsvakhet som kan være lokal eller fjernt fra injeksjonssted som kan omfatte ptosis, diplopi, dysfagi, dysartri, generalisert asteni eller respirasjonssvikt Disse pasientene bør gjennomgå ytterligere medisinsk evaluering og passende medisinsk behandling opprettes umiddelbart, noe som også kan kreve sykehusinnleggelse.
Hvis musklene i oropharynx og esophagus påvirkes, kan det oppstå aspirasjon som kan føre til utvikling av aspirasjonspneumoni. Ved lammelse av respirasjonsmuskulaturen eller tilstrekkelig svekkelse, vil det være nødvendig å ty til intubasjon og assistert pust, inntil restitusjon og også innebære behovet for trecheostomi og langvarig mekanisk ventilasjon i tillegg til annen generell støttebehandling.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: andre perifer virkende muskelavslappende midler.
ATC -kode M03A X01
Botulinumtoksin type A blokkerer den perifere frigjøringen av acetylkolin ved de presynaptiske kolinerge nerveender ved å forstyrre frigjøringen av SNAP-25, et protein som utfyller vellykket oppsamling og frigjøring av acetylkolin fra vesikler i nerveender.
Etter injeksjon oppstår en innledende rask høyaffinitetsbinding av toksinet til spesifikke celleoverflatereseptorer Dette etterfølges av overføring av toksinet over plasmamembranen ved reseptormediert endocytose Til slutt frigjøres toksinet i cytosolen.
Denne sistnevnte prosessen ledsages av en progressiv inhibering av acetylkolinfrigivelse, og kliniske tegn forekommer innen 2-3 dager med maksimal effekt observert innen 5-6 uker etter injeksjon.
Gjenoppretting, etter intramuskulær inokulasjon, skjer vanligvis innen 12 uker etter injeksjon ettersom nerveendene regenererer og kobles til terminalplatene igjen. Etter intradermal inokulasjon, hvor målet er de eksokrine svettekjertlene, varte effekten i gjennomsnitt 7,5 måneder etter den første injeksjonen. hos pasienter behandlet med 50 enheter per axilla Imidlertid var effekten hos 27,5% av pasientene 1 år eller mer. Restaurering av sympatiske nerveender i svettekjertlene etter intradermal inokulering med BOTOX er ikke undersøkt.
BOTOX, etter intradetrusorial injeksjon, har effekter på efferente veier for selve detrusoraktiviteten ved å hemme frigjøringen av acetylkolin. Videre kan BOTOX hemme frigjøring av afferente nevrotransmittere og følsomhetsveier.
KLINISKE STUDIER
Primær hyperhidrose av armhulene
En dobbeltblind, multisenter klinisk studie ble utført på pasienter som hadde vedvarende bilateral primær aksillær hyperhidrose, etablert ved baseline, ved gravimetrisk måling, lik minst 50 mg spontan svette produsert av hver armhule i mer enn 5 minutter ved romtemperatur, å hvile. Tre hundre og tjue pasienter ble randomisert til å motta 50 enheter BOTOX (N = 242) eller placebo (N = 78). Responderpasienter ble definert som å ha en reduksjon fra baseline på minst 50% i aksillær svette.
Ved det primære endepunktet, 4 uker etter injeksjon, var responsraten i gruppen BOTOX-behandlet 93,8%, sammenlignet med 35,9% hos de placebobehandlede pasientene (p
Forekomsten av responderende pasienter blant de som ble behandlet med BOTOX fortsatte å være betydelig høyere (s
I en åpen oppfølgingsklinisk studie ble det registrert 207 kvalifiserte pasienter som mottok opptil 3 behandlinger med BOTOX. Nærmere bestemt fullførte 174 pasienter hele 16-måneders varigheten av de 2 samlede studiene (4-måneders dobbeltblind studie og 12-måneders oppfølging av åpen studie). Forekomsten av klinisk respons i uke 16 etter den første ( n = 287), andre (n = 123) og tredje (n = 30) behandling var henholdsvis 85,0%, 86,2% og 80%. Gjennomsnittlig varighet av effekten basert på den kombinerte enkeltdose-fortsettelsesstudien og den åpne studien var 7,5 måneder fra den første behandlingen; i tillegg varte effekten hos 27,5% av pasientene i 1 år eller mer.
Det er begrenset erfaring fra kliniske studier med bruk av BOTOX ved aksillær hyperhidrose hos barn mellom 12 og 18 år.
En enkelt, ettårig, ukontrollert, gjentatt doseringssikkerhetsstudie ble utført i USA hos pediatriske pasienter i alderen 12-17 år (N = 144) med alvorlig primær hyperhidrose av aksillene. Pasientene var hovedsakelig kvinner (86,1%) og kaukasiere (82,6%). Pasientene ble behandlet med en dose på 50 U per armhule for totalt 100 U per pasient per behandling. Imidlertid er det ikke utført doseringsstudier hos ungdom, og derfor kan det ikke gis anbefalinger om dosering. Effekten og sikkerheten til BOTOX i denne pasientgruppen er ikke definitivt fastslått.
Urininkontinens på grunn av neurogen detrusor -overaktivitet
To multisenter, randomiserte, dobbeltblindede, placebokontrollerte fase III-kliniske studier ble utført på pasienter med urininkontinens på grunn av nevrogen detrusoroveraktivitet, i stand til spontan vannlating eller bruk av kateter. Totalt 691 pasienter med ryggmargsskade eller multippel sklerose, utilstrekkelig behandlet med minst ett antikolinerge middel, ble registrert. Disse pasientene ble randomisert til å motta 200 enheter BOTOX (n = 227), 300 enheter BOTOX (n = 223) eller placebo (n = 241).
I begge fase III -studiene ble det observert betydelige forbedringer til fordel for BOTOX (200 enheter og 300 enheter) i forhold til placebo i den primære effektvariabelen for endring fra baseline i ukentlig inkontinensfrekvens på tidspunktet for primær effektpåvisning. I uke 6, inkludert prosent av pasientene uten inkontinensepisoder. Det ble observert betydelige forbedringer i urodynamiske parametere, inkludert økning i maksimal cystometrisk kapasitet og reduksjon i topp detrusortrykk under den første ufrivillige detrusorkontraksjonen. Forbedringer ble også observert. Signifikant, sammenlignet med placebo, i pasientrapporterte score av helserelatert og inkontinensspesifikk livskvalitet målt ved spørreskjemaet Inkontinence Quality of Life (I-QOL) (inkludert begrensende unngåelsesatferd, "psykososial innvirkning og" sosial forlegenhet). Ingen ytterligere fordeler ble vist med 300 enheter BOTOX sammenlignet med 200 enheter, og en mer gunstig sikkerhetsprofil ble observert med 200 enheter BOTOX.
Resultatene av de sentrale studiene med sammendragsdata er vist nedenfor:
Primære og sekundære endepunkter ved baseline og endring fra baseline i samlede sentrale studier:
Median varighet av responsen i de to sentrale studiene, basert på forespørsel om behandling, var 256-295 dager (36-42 uker) for gruppen 200 dosenheter, sammenlignet med 92 dager (13 uker) med placebo.
For alle effektpunktene hadde pasientene svar som var i samsvar med ny behandling.
I de sentrale studiene utviklet ingen av de 475 pasientene med nevrogen overaktivitet av detrusoren nøytraliserende antistoffer i prøvene som ble analysert.
Kronisk migrene
BOTOX blokkerer frigjøring av nevrotransmittere assosiert med patogenesen av smerte.Virkningsmekanismen til BOTOX ved symptomatisk lindring ved kronisk migrene er ikke fullt ut forstått.
Kliniske og prekliniske farmakodynamiske studier tyder på at BOTOX undertrykker perifer sensibilisering, og derfor sannsynligvis også hemmer sentral sensibilisering.
Tabellen nedenfor viser hovedresultatene oppnådd fra den samlede effektanalysen etter to behandlinger med BOTOX gitt med 12 ukers mellomrom i to kliniske fase III-studier med pasienter med kronisk migrene, som i løpet av baseline perioden på 28 dager opplevde minst 4 episoder og led av hodepine i ≥ 15 dager (med minst 4 timer med kontinuerlig hodepine), med minst 50% hodepine dager for både migrene og sannsynlig migrene.
Selv om studiene ikke hadde tilstrekkelig betydning for å påvise forskjeller i undergrupper, så behandlingseffekten mindre ut i den mannlige (N = 188) og ikke-kaukasiske (N = 137) pasientgruppen enn i hele studiepopulasjonen.
05.2 Farmakokinetiske egenskaper
Generelle egenskaper til den aktive ingrediensen
Distribusjonsstudier utført på rotter indikerte langsom muskeldiffusjon av 125I-botulinum nevrotoksinkompleks type A i gastrocnemius-muskelen etter injeksjon, etterfulgt av rask systemisk metabolisme og eliminering i urinen. Mengden radiomerket materiale i muskelen avtok med en halveringstid på ca. 10 timer. På injeksjonsstedet var radioaktiviteten bundet til store proteinmolekyler, mens den i plasma ble bundet til små molekyler, noe som tyder på en rask systemisk substratmetabolisme. Innen 24 timer etter administrering ble 60% av radioaktiviteten utskilt i urinen. Sannsynligvis metaboliseres toksinet av proteaser og molekylkomponentene resirkuleres gjennom de normale metabolske veiene.
På grunn av produktets natur har de klassiske studiene om absorpsjon, distribusjon, biotransformasjon og eliminering av det aktive prinsippet ikke blitt utført.
Egenskaper hos pasienter
Det antas at terapeutiske doser av BOTOX forårsaker dårlig systemisk fordeling. Kliniske studier utført med enkeltfiberelektromyografiteknikker har vist økt nevromuskulær elektrofysiologisk aktivitet i muskler fjernt fra injeksjonsstedet, ikke ledsaget av kliniske tegn eller symptomer.
05.3 Prekliniske sikkerhetsdata
Reproduksjonsstudier
Ved å utsette gravide mus, rotter og kaniner for intramuskulære injeksjoner av BOTOX i løpet av organogenesen, var No Observable Adverse Effect Level (NOAEL) på utvikling henholdsvis 4, 1 og 0,125 enheter / kg. Høyere doser var assosiert. fetal kroppsvekt og / eller forsinket ossifikasjon og abort ble observert hos kaniner.
Fruktbarhet og reproduksjon
Ved å utsette hann- og hunnrotter for intramuskulære injeksjoner av BOTOX, var den reproduktive NOEL henholdsvis 4 og 8 enheter / kg. Høyere doser var assosiert med doseavhengige reduksjoner i fruktbarhet.
Når befruktningen hadde skjedd, var det ingen negative effekter på antall eller levedyktighet av embryoer som ønsket eller ble unnfanget fra behandlede hann- og hunnrotter.
Andre studier
I tillegg til reproduksjonstoksikologiske studier ble følgende prekliniske sikkerhetsstudier utført for BOTOX: akutt toksisitet, toksisitet ved gjentatt dosering, lokal toleranse, mutagenisitet, antigenisitet, kompatibilitet med humant blod. Disse studiene avdekket ikke noen spesiell risiko for mennesker ved klinisk relevante doser. Maksimal anbefalt dose for en behandlingsøkt er 300 enheter (tilsvarende 6 enheter / kg hos en 50 kg person). Den publiserte intramuskulære LD50 hos unge aper er 39 enheter / kg.
Ingen systemisk toksisitet ble observert etter en enkelt intradetrusorial injeksjon av prostata urinrøret og proksimal endetarm, sædblære og urinblærevegg eller ape livmor (~ 3 enheter / kg) uten bivirkninger. 9 måneder med gjentatte doser injisert i detrusormuskelen (4 injeksjoner), ble ptosis observert med 24 enheter / kg og dødelighet ved doser ≥24 enheter / kg. Muskelfiberdegenerasjon / regenerering ble observert i skjelettmuskulaturen til dyr der det ble gitt en dose på minst 24 enheter / kg. Disse myopatiske endringene ble ansett som sekundære effekter av systemisk eksponering. Videre ble degenerering av muskelfibre observert hos ett dyr som ble utsatt for en dose på 12 enheter / kg. Lesjonen hos dette dyret var av minimal alvorlighetsgrad og ble ansett som ikke forbundet med noen kliniske manifestasjoner. Det var ikke mulig å fastslå med sikkerhet om det var relatert til BOTOX -behandling. Dosen på 12 enheter / kg tilsvarer en 3 ganger større eksponering for BOTOX enn den anbefalte kliniske dosen på 200 enheter for urininkontinens på grunn av nevrogen overaktivitet av detrusormuskelen (hos en 50 kg person).
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Menneskelig albumin
Natriumklorid
06.2 Uforlikelighet
I mangel av kompatibilitetsstudier, må dette legemidlet ikke blandes med andre produkter.
06.3 Gyldighetsperiode
3 år.
Mikrobiologiske og potensstudier har vist at produktet kan lagres i opptil 5 dager ved 2 ° -8 ° C etter rekonstituering.
Oppbevaringstid og -betingelser før bruk er brukerens ansvar og bør ikke være lenger enn 24 timer ved 2 ° C - 8 ° C.
Etter rekonstituering i hetteglasset har produktet vist stabilitet i 24 timer ved 2 ° C - 8 ° C.
06.4 Spesielle forholdsregler for lagring
Oppbevares i kjøleskap (2 ° C - 8 ° C), eller i fryser (-5 ° C eller lavere).
For oppbevaringsbetingelser for det rekonstituerte legemidlet, se pkt. 6.3.
06.5 Emballasje og innhold i pakningen
Type I fargeløs hetteglass, nominell kapasitet på 10 ml, utstyrt med en klorobutyl gummipropp og en sabotasjefri aluminiumsforsegling.
Pakningene kan inneholde 1, 2, 3, 6 eller 10 hetteglass.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Det er god praksis å rekonstituere hetteglasset og klargjøre sprøyten på toppen av det plastiserte, absorberende papiret for å samle opp sølt produkt.
BOTOX skal bare rekonstitueres med sterilt natriumklorid 9 mg / ml (0,9%) injeksjonsvæske, oppløsning. Den riktige mengden fortynningsmiddel bør tas ut med en sprøyte (se pkt.4.2 for fortynningsinstruksjoner for urininkontinens på grunn av nevrogen overaktivitet i detrusormuskelen).
Fortynningstabell for BOTOX 100 Allergan Unit -pakken for alle andre indikasjoner:
Hvis pakninger med forskjellige styrker av BOTOX brukes under samme behandling, må du være spesielt forsiktig med å bruke riktig mengde fortynningsmiddel for å rekonstituere det spesifikke antallet enheter per 0,1 ml. Mengden fortynningsmiddel varierer mellom BOTOX 100 Allergan Units og BOTOX 200 Allergan Units. Hver sprøyte må merkes på riktig måte.
Siden BOTOX er denaturert ved brusning eller kraftig omrøring, bør fortynningsmiddelet injiseres sakte i hetteglasset. Hetteglasset skal kastes hvis styrken i vakuumet ikke er slik at det trekker fortynningsmiddelet inn i hetteglasset. Rekonstituert BOTOX skal være en klar fargeløs eller lysegul løsning uten partikler. Den rekonstituerte løsningen må kontrolleres visuelt før bruk for klarhet og fravær av partikler. Etter rekonstituering i hetteglasset, kan BOTOX oppbevares i kjøleskap (2-8 ° C) i opptil 24 timer før bruk. Dato og klokkeslett for rekonstituering bør angis i plassen på etiketten.
Ved ytterligere fortynning av BOTOX for urininkontinens i en sprøyte, må den brukes umiddelbart.Dette produktet er kun til engangsbruk og eventuell gjenværende ubrukt løsning skal kastes.
For sikkerhets skyld bør ubrukte hetteglass rekonstitueres med en liten mengde vann og deretter autoklaveres. Ubrukte hetteglass, sprøyter og sølt materiale skal autoklaveres, eller eventuell gjenværende BOTOX skal gjøres inaktiv ved bruk av en natriumhypoklorittoppløsning (0,5%) i 5 minutter.
Ubrukte medisiner og avfall fra denne medisinen må kastes i henhold til lokale forskrifter.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
Allergan Pharmaceuticals Ireland
Castlebar Road
Westport
County Mayo
Irland
Salgsrepresentant i Italia
Allergan SpA, Via Salvatore Quasimodo n ° 134/138, Roma
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
AIC n. 034883013 / M "100 enheter Allergan pulver til injeksjonsvæske, oppløsning" 1 hetteglass inneholder 100 Allergan enheter
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Første autorisasjon: 4. august 2000
Fornyelse: 28. februar 2009
10.0 DATO FOR REVISJON AV TEKSTEN
AIFA -fastsettelse av 23. januar 2013