Hva er Azarga?
Azarga er en øyedråpe, suspensjon, som inneholder to virkestoffer, brinzolamid og timolol.
Hva brukes Azarga til?
Azarga brukes til å redusere intraokulært trykk (IOP, indre trykk i øyet). Det brukes hos voksne pasienter med åpenvinklet glaukom (en sykdom der det indre trykket i øyet øker fordi væske ikke kan renne ut av øyet. " øye) eller okulær hypertensjon (når øyets indre trykk er høyere enn normalt). Azarga brukes når behandling med et legemiddel som inneholder bare ett aktivt stoff ikke har redusert IOP tilstrekkelig.
Medisinen kan bare fås på resept.
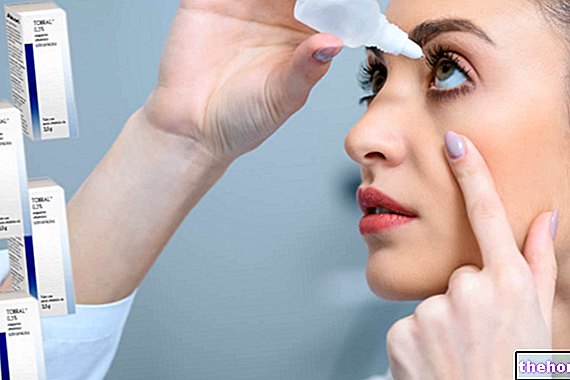
Hvordan brukes Azarga?
Azarga gis som en dråpe i det / de berørte øynene to ganger daglig. Suspensjonen må ristes godt før bruk.
Hvordan fungerer Azarga?
Forhøyelsen av IOP forårsaker skade på netthinnen (den lysfølsomme overflaten på baksiden av øyet) og til synsnerven som overfører signaler fra øyet til hjernen. Alvorlig synstap og til og med blindhet kan oppstå. Ved å senke trykk, reduserer Azarga risikoen for skade.
Azarga inneholder to aktive ingredienser, brinzolamid og timolol. De to stoffene virker ved å redusere produksjonen av vandig humor (den vandige væsken inne i øyet) på forskjellige måter. Brinzolamid er en karbonsyreanhydrasehemmer som virker ved å blokkere et enzym som kalles karbonsyreanhydrase, som produserer bikarbonationer i kroppen. Bikarbonat er nødvendig for produksjon av vandig humor. Brinzolamid har blitt godkjent i EU (EU) under merkenavnet Azopt siden 2000. Timolol er en betablokker som vanligvis har blitt brukt til behandling av glaukom siden 1970-tallet.
Den kombinerte virkningen av de to stoffene er bedre enn enkeltstoffene som brukes alene.
Hvordan har Azarga blitt studert?
Effekten av Azarga ble først testet i eksperimentelle modeller før den ble studert hos mennesker.
Azarga har blitt studert i to hovedstudier med totalt 960 voksne med åpenvinklet glaukom eller okulær hypertensjon. Den første var en seks måneders studie som sammenlignet Azarga med brinzolamid og timolol brukt alene hos 523 pasienter. Den andre var en 12-måneders studie som sammenlignet Azarga med kombinasjonen av timolol og dorzolamid (en annen karbonsyreanhydrasinhibitor) hos 437 pasienter.I begge studiene var det viktigste mål for effektivitet endringen i IOP i de første seks månedene av behandlingen. IOP ble målt i "millimeter kvikksølv" (mmHg).
Hvilken fordel har Azarga vist under studiene?
Azarga var mer effektiv enn de enkelte virkestoffene som ble brukt alene og viste tilsvarende effekt som kombinasjonen av timolol og dorzolamid. I den første studien ble IOP redusert fra omtrent 21 mmHg til 8,0 - 8,7 mmHg. Hos pasienter som brukte Azarga. Disse reduksjonene sammenlignet med 5,1 - 5,6 mmHg for de som bruker brinzolamid og 5,7 - 6,9 mmHg for de som bruker timolol.I den andre studien falt IOP fra omtrent 26 mmHg på omtrent 8,3 mmHg etter seks måneder i begge pasientgruppene.
Hva er risikoen forbundet med Azarga?
De vanligste bivirkningene med Azarga (funnet hos mellom 1 og 10 pasienter av 100) er dysgeusi (bitter eller merkelig smak i munnen), tåkesyn, øyesmerter, øyeirritasjon og fremmedlegemefølelse i øyet. Den fullstendige listen over bivirkninger rapportert for Azarga, se pakningsvedlegget.
Azarga må ikke brukes til personer som kan være overfølsomme (allergiske) overfor virkestoffene, noen av de andre stoffene, andre betablokkere (f.eks. Noen hjertemedisiner) eller sulfonamider (f.eks. Noen antibiotika). Legemidlet bør ikke brukes av pasienter som:
- har hatt astma;
- lider av alvorlig kronisk obstruktiv lungesykdom (en sykdom som forårsaker innsnevring av luftveiene);
- har visse hjerteproblemer;
- har en alvorlig allergi som involverer nese og luftveier;
- har hyperkloremisk acidose (overflødig surhet i blodet forårsaket av for mye klorid);
- har alvorlige nyreproblemer.
For fullstendig liste over begrensninger for bruk, se pakningsvedlegget.
Azarga inneholder benzalkoniumklorid, noe som forårsaker misfarging av myke kontaktlinser. Derfor må folk som bruker myke kontaktlinser være forsiktige.
Hvorfor har Azarga blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) bemerket at kombinasjonen av de to virkestoffene i Azarga forenkler behandlingen og hjelper pasientene til å holde seg til behandlingen. Komiteen bestemte at fordelene ved Azarga er større enn risikoen for IOP -reduksjon hos voksne pasienter med åpen vinkelglaukom eller okulær hypertensjon for hvem monoterapi ikke sikrer tilstrekkelig IOP -reduksjon Komiteen anbefalte at Azarga ble gitt markedsføringstillatelse.
Mer informasjon om Azarga:
25. november 2008 ga EU -kommisjonen Alcon Laboratories (UK) Ltd. en "markedsføringstillatelse" for Azarga gyldig i hele EU.
For hele versjonen av Azargas EPAR, klikk her.
Siste oppdatering av denne oppsummeringen: 10-2008.
Informasjonen om Azarga - øyedråper som er publisert på denne siden, kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.