Generellitet
Behandling av kronisk myeloid leukemi (CML) inkluderer flere terapeutiske alternativer som kan holde sykdommen under kontroll i lengre perioder. Rutinemessige blod- og benmargstester og hyppig evaluering av en hematolog eller onkolog kan overvåke utviklingen av kreften.

Fra resultatene av medisinske undersøkelser (blodtelling, cytogenetiske og molekylære tester) er det mulig å forstå:
- Graden av effektivitet av behandlingen over tid og utviklingen av responsen på terapi;
- Hvis sykdommen ikke lenger reagerer på medisiner (motstand mot terapi).
Overvåking og respons på terapi
Korrekt overvåking av sykdomsforløpet er avgjørende for å verifisere terapiens effekt og følgelig for å kunne gripe inn raskt hvis behandlingen mislykkes.
Cytogenetisk analyse og molekylærbiologiske undersøkelser brukes, så vel som for diagnostiske formål, også for å vurdere graden av respons på den terapeutiske protokollen og for å markere enhver vedvarende sykdom etter behandling (studie av minimal residual sykdom):
- Fullstendig hematologisk respons: Når behandlingen begynner å ha effekt, reduseres antallet leukemiceller. Hematologiske tester er ikke lenger i stand til å oppdage avvikende kloner, men dette er mulig med cytogenetisk analyse.
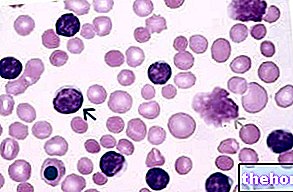
- Komplett cytogenetisk respons: oppnådd når tilstedeværelsen av Philadelphia -kromosomet (Ph) ikke lenger fremheves ved konvensjonell cytogenetisk analyse (standard tilnærming for å overvåke responsen på behandlingen) eller ved fluorescerende in situ -hybridisering (FISH), en teknikk som evaluerer prosentandelen av Ph + benmargsceller. Den cytogenetiske analysen, utført på en finnåls aspirert beinmargsprøve, er også den eneste metoden for å bestemme tilstedeværelsen av eventuelle kromosomale endringer, i tillegg til Philadelphia-kromosomet, med en prognostisk rolle.
- Fullstendig molekylær respons: den oppnås når molekylæranalysen ikke er i stand til å påvise ekspresjonen av hybridgenet BCR / ABL. Terapien har vist seg effektiv og de molekylære signalene, som fremmer produksjonen av bcr-abl-proteinene, er så lave at de ikke kan oppdages selv med svært sensitive tester, for eksempel molekylære. Økte utskriftsnivåer, som overvåkes, kan indikere tap av respons på behandling.
Oppnåelsen av disse resultatene representerer et veldig viktig resultat: mange studier viser at pasienter, med fullstendig cytogenetisk og molekylær respons, har en veldig stor sannsynlighet for å overleve i lang tid, uten at sykdommen utvikler seg til den akselererte og / eller blastfasen .
Mange faktorer kan påvirke effekten av behandlingen, og derfor anbefales det i de første stadiene å fortsette med tester etter 3, 6, 12 og 18 måneder.
Informasjonen som er innhentet så langt fra kliniske studier, som definerer optimal respons og svikt ved forskjellige behandlingstider, har ført til utforming av et overvåkingsopplegg, som må følges for riktig behandling av pasienten (indikasjoner foreslått av European Leukemia-Net):
Hematologen (eller onkologen) vil være i stand til å etablere noen mål og verifisere terapiens effekt i det spesifikke kliniske tilfellet, ettersom pasientene reagerer forskjellig på behandlingen og ikke alle er i stand til å nå de optimale terapeutiske milepælene innen den forventede tidsperioden ...
Terapeutiske alternativer
Hovedmålet med behandlingen for CML er å "oppnå fullstendig molekylær remisjon: sykdommen styres av behandlingen (selv om den ikke forsvinner helt) og antallet produserte patologiske kloner er tilstrekkelig begrenset til ikke å forårsake symptomer. De fleste kan ikke bli kvitt leukemiceller helt, kan behandling bidra til å oppnå langsiktig remisjon av sykdommen.
Terapeutiske mål kan omfatte:
- Begrens manifestasjonen av symptomer på kronisk myeloid leukemi;
- Gjenopprett normale parametere relatert til antall blodceller;
- Reduser antallet Philadelphia -kromosompositive leukemiceller (Ph +) og molekylære signaler (BCR / ABL -transkripsjoner);
- Sikt på at Philadelphia + -kromosomene forsvinner (fullstendig cytogenetisk respons).
Konvensjonelle antiblastiske legemidler
Noen antiblastiske legemidler, som f.eks busulfan (alkylering) og l "hydroksyurea (spesifikk hemmer av DNA -syntese), har blitt brukt, spesielt tidligere, for å oppnå cytoreduksjon og kontroll av sykdommen i den kroniske fasen. Konvensjonell behandling resulterte i en forbedring av livskvaliteten, men klarte ikke å signifikant endre sykdommens naturlige historie eller forhindre progresjon til akselerert / eksplosjonsfasen.
Rekombinant interferon-alfa
Fra begynnelsen av 1980 -tallet ble introduksjonen av interferoner tillatt å observere, i tillegg til reduksjon og normalisering av granulocyttandelen, oppnåelse av negativisering av cytogenetiske og molekylære tester, noe som induserer en lengre varighet av den kroniske fasen, med påfølgende reduksjon av utviklingen i akselerert og / eller blastfase. Interferon -alfa har redusert rollen som konvensjonell CML -terapi: dette legemidlet er i stand til å indusere en fullstendig cytogenetisk respons hos 20-30% av pasientene, noe som spesielt forstyrrer translasjonen av proliferative signaler i Ph + -celler og hemmer cellemultiplikasjonstumorforløpere. Interferon-alfa virker også med en indirekte mekanisme for overlevelse av leukemiceller, reduserer celleadhesjonen og forsterker aktiviteten til cellene i immunsystemet.
En begrensning for bruken av dette legemidlet er gitt av dets ikke-ubetydelige toksisitet. Bivirkningene av interferon inkluderer tretthet, feber og vekttap. For å forbedre de oppnådde resultatene, har interferon blitt kombinert med andre cytotoksiske midler. Kun interferon-forbindelsen med cytosin arabinosid (ARA-C) har vist seg å gi bedre resultater enn interferon alene, men uten en åpenbar overlevelsesfordel.
Allogen benmargstransplantasjon
Transplantasjon av stamceller fra en frisk donor som er kompatibel med mottakeren (allogen transplantasjon) har i årevis representert den hyppigste terapeutiske indikasjonen, og fremdeles i dag er den eneste behandlingen som er i stand til å definitivt utrydde neoplasma.
Denne prosedyren, når den utføres i den kroniske fasen, kan resultere i en femårig sykdomsfri overlevelse i omtrent 50% av tilfellene.
Allogen benmargstransplantasjon innebærer en første fase av ødeleggelse av alle (eller nesten alle) Ph + -celler gjennom kondisjoneringsterapi (kjemoterapi i kombinasjon med total kroppsbestråling), etterfulgt av rekonstituering av den hematopoietiske margen av de infunderte donorstamcellene. I tillegg bidrar donormarglymfocytter til å kontrollere og / eller eliminere eventuelle Ph + -celler med en immunmediert effekt kalt "transplantat versus leukemi" (transplantat versus leukemi) effekt. Responsen på terapien kan overvåkes ved å vurdere om de molekylære endringene som er typiske for kronisk myeloid leukemi, har forsvunnet. Den allogene benmargstransplantasjonen representerer den terapeutiske behandlingen som er i stand til å "kurere" CML, men involverer dessverre en feil på grunn av dødelig toksisitet og / eller tilbakefall. Denne prosedyren er faktisk veldig krevende og kan påvirkes av alder på pasient. pasient og for tidlig transplantasjon (måneder eller år etter diagnosen av den kroniske fasen): på grunn av den potensielle faren, er det praktisk mulig bare hos pasienter under 55 år, uten ytterligere samtidige patologier. Derfor utgjør allogen transplantasjon en reell terapeutisk mulighet for bare et mindretall av pasientene med CML (også med tanke på vanskeligheter med å finne en kompatibel stamcelledonor).
Mer nylig, hos personer med kronisk myeloid leukemi som ikke er kvalifisert for allograft (alder, mangel på donor, avslag, etc.), ble autotransplantasjon foreslått. Pasientens benmarg, som ble infisert på nytt etter en "forsettlig adekvat cytocidbehandling for Ph + -celler (med antiblastisk + interferon), ville rekonstituere seg selv med en utbredt re-ekspansjon av Ph-celler.
Imatinib mesylat (Glivec ®)
Historien om behandlinger med kronisk myeloid leukemi har blitt revolusjonert ved introduksjonen av den første tyrosinkinasehemmeren (Imatinib mesylat), som har bidratt sterkt til å forbedre pasienters livskvalitet.
Imatinib er en spesifikk hemmer av BCR / ABL, designet etter å ha forstått sykdommens molekylære biologi og brukt i behandlingen av Ph + kronisk myeloid leukemi.
Legemidlet er i stand til å indusere fullstendig molekylær cytogenetisk remisjon hos 80-90% av pasientene og er også aktivt i myeloide neoplasmer med eosinofili og involvering av PDGRF (blodplateavledet vekstfaktor, serum mitogen involvert i mange patologiske tilstander, som fremmer kjemotaksi og proliferativ kapasitet).
Imatinib blokkerer selektivt tyrosinkinaseaktiviteten til BCR / ABL gjennom en hemmende mekanisme for ATP: stoffet binder høyenergimolekylet (ATP) som er tilgjengelig i det spesifikke domenet til BCR / ABL -kinasen, forhindrer fosforylering av andre substrater og blokkerer kaskaden reaksjoner som ville være ansvarlig for genereringsprosessen av Ph + leukemiske kloner. Dosen som brukes av dette molekylet (imatinibmetysilat) varierer fra 400 mg / dag til 800 mg / dag i forhold til sykdomsfasen og responsen. For tiden er det det foretrukne stoffet for behandling av CML på grunn av dets bemerkelsesverdige effekt. Bivirkningene, reversible med suspensjon og / eller reduksjon av dosen, kan være forskjellige (økte transaminaser, kvalme, hudutslett, væskeretensjon, etc.).
Tilfeller som viser resistens mot stoffet over tid har blitt observert (for eksempel pasienter med avansert sykdom) og biologisk-kliniske kriterier er identifisert for å definere typen respons på behandling. Mekanismene som er ansvarlige for denne motstanden ser ut til å være flere (mutasjoner av kinasedomenet, amplifikasjon / overuttrykk av BCR / ABL, klonal evolusjon ...). I disse tilfellene er det ikke lenger hensiktsmessig å fortsette behandlingen med Imatinib.
For pasienter med disse tilstandene er de mulige alternativene:
- Den allogene transplantasjonen;
- Konvensjonell terapi (hydroksyurea, busulfan, etc.);
- L "interferon;
- Eksperimentell terapi (med 2. generasjon tyrosinkinasehemmere).
2. generasjon tyrosinkinasehemmere
Mislykket behandling med Imatinib er assosiert med progresjon av akselerert og / eller blastfase kronisk myeloid leukemi og har en spesielt dårlig prognose. I de siste årene har farmakologisk forskning tillatt bruk i klinisk praksis av andre generasjon tyrosinkinasehemmere, aktive hos pasienter som har utviklet resistens mot Imatinib: Dasatinib (Sprycel ®) og Nilotinib (Tasigna ®) brukes hos pasienter med kronisk fase og / eller progresjon CML ildfast for Glivec ® og er i stand til å reindusere komplette og vedvarende hematologiske, cytogenetiske og molekylære responser. Mange studier har imidlertid vist at Ph + -klonen - på grunn av sin genetiske ustabilitet - kan utvikle mutasjoner av BCR / ABL -kinasedomenet og viser seg å være resistente mot forskjellige hemmende legemidler. Andre molekyler i eksperimentfasen (3. generasjons hemmere) er rettet mot spesifikke mål for kronisk myeloid leukemi; spesielt er de i stand til å sensitivisere leukemiske celler Ph + med spesifikke mutasjoner (eksempel: Mk-0457 for resistent CML og med T315I-mutasjon, som direkte påvirker t bindingsstedet for imatinib).
Andre artikler om "Kronisk myeloid leukemi terapi"
- Kronisk myeloid leukemi: Kronisk myeloid leukemi: Diagnose
- Kronisk myeloid leukemi: definisjon, årsaker, symptomer