Aktive ingredienser: Terbinafine
LAMISILMONO 1% kutan løsning
Hvorfor brukes Lamisilmono? Hva er den til?
LAMISILMONO er en enkeltdose behandling for tinea pedis (fotsopp).
LAMISILMONO virker ved å drepe soppene som forårsaker tinea pedis (fotsopp) Når den påføres føttene, etterlater den en glatt, knapt synlig film som blir igjen på huden og frigjør den aktive ingrediensen i huden.
Hvordan vet du om du har tinea pedis (fotsopp)
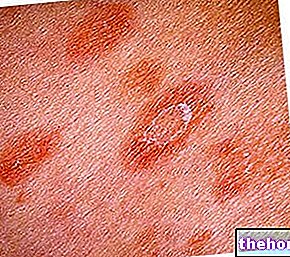
Tinea pedis (fotsopp) vises bare på føttene, ofte mellom tærne, men kan spre seg til sålene og sidene av føttene.
Den vanligste typen tinea pedis (fotsopp) forårsaker sprekker eller peeling av huden. Du kan også ha mild hevelse, blemmer eller våte sår. Dette kan ofte være forbundet med kløe eller brennende følelser.
Hvis du ikke er sikker på om symptomene dine egentlig skyldes tinea pedis (fotsopp), må du kontakte lege eller apotek før du bruker LAMISILMONO.
Kontraindikasjoner Når Lamisilmono ikke skal brukes
Ikke bruk LAMISILMONO
Hvis du er allergisk mot terbinafin eller noen av de andre innholdsstoffene i dette legemidlet
Fortell legen din eller apoteket hvis dette gjelder deg og du ikke bruker LAMISILMONO.
Forholdsregler for bruk Hva du trenger å vite før du bruker Lamisilmono
Rådfør deg med lege eller apotek før du bruker LAMISILMONO
- Ikke bruk dette legemidlet hvis du lider av langvarige soppinfeksjoner i såler og hæler på føttene med tilhørende fortykning og / eller uttalt hudskall. Hvis du tror du kan ha denne tilstanden, bør du kontakte legen din, da du kan trenge en annen medisin.
- LAMISILMONO er kun til ekstern bruk. Ikke bruk den i munnen og ikke svelg den.
- Unngå kontakt med ansikt, øyne eller skadet hud, da alkohol kan være irriterende.
- Hvis løsningen ved et uhell kommer i øynene, skyll grundig med rennende vann. Se legen din hvis noen problemer vedvarer.
- LAMISILMONO inneholder alkohol. Holdes vekk fra åpen ild.
Barn og ungdom
Barn og ungdom under 18 år bør ikke bruke LAMISILMONO.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Lamisilmono
Fortell legen din eller apoteket dersom du bruker, nylig har brukt eller kanskje bruker andre legemidler.
Ikke bruk andre medisiner eller behandlinger på foten din (inkludert de du kan ha kjøpt uten resept) samtidig med LAMISILMONO.
Advarsler Det er viktig å vite at:
Graviditet, amming og fruktbarhet
- Rådfør deg med lege eller apotek før du bruker dette legemidlet hvis du er gravid, tror at du kan være gravid eller planlegger å bli gravid. LAMISILMONO skal ikke brukes under graviditet med mindre det er strengt nødvendig.
- Ikke bruk LAMISILMONO mens du ammer. Ikke la spedbarn komme i kontakt med et behandlet område, inkludert brystene.
Kjøring og bruk av maskiner
- Bruk av LAMISILMONO påvirker ikke evnen til å kjøre bil og bruke maskiner.
Dose, metode og administrasjonstidspunkt Hvordan bruke Lamisilmono: Dosering
Bruk dette legemidlet nøyaktig som beskrevet i dette pakningsvedlegget eller som legen din har fortalt deg. Rådfør deg med lege eller apotek hvis du er i tvil.
Den anbefalte dosen er å bruke løsningen en gang, som angitt nedenfor
Instruksjoner for bruk:
Voksne
- Det er best å påføre LAMISILMONO etter dusj eller badekar.
- Dette er en engangsbehandling.
- Vask begge føttene og tørk dem grundig.
- Vask og tørk hendene.
- Fjern hetten fra røret.
- Du bruker den på begge føttene - du bruker omtrent halvparten av røret for hver fot, etter behov for å dekke huden. Fullfør den ene foten før du behandler den andre.
- Påfør med tærne på hver fot som vist nedenfor. Spred jevnt på huden mellom fingrene, under og rundt. Påfør deretter på sålen og sidene av foten.
- Ikke gni eller masser.
- Behandle den andre foten på samme måte, selv om huden ser sunn ut. Dette er for å sikre at du blir kvitt soppen helt - denne kan være tilstede på den andre foten selv uten merker.
- La produktet tørke i 1-2 minutter før du tar på deg vanlige fottøy.
- Vask hendene med varmt såpevann etter påføring.
- Ikke vask eller fukt føttene i 24 timer etter påføring av LAMISILMONO. Bank lett på føttene for å tørke dem etter å ha vasket dem forsiktig.
- Ikke påfør huden en gang til.
Hvor ofte og hvor lenge skal jeg bruke LAMISILMONO
Påfør bare en gang. Ikke påfør andre gang.
LAMISILMONO begynner å drepe soppen umiddelbart. Filmen som dannes indikerer at den aktive ingrediensen trenger inn i huden hans der den fortsetter å virke i flere dager.
Huden din bør begynne å forbedre seg i løpet av få dager, men det kan ta opptil 4 uker før huden din er helt helbredet.
Rådfør deg med lege eller apotek som vil anbefale deg hvis du ikke merker tegn på bedring innen en uke etter påføring av LAMISILMONO.
Ikke bruk produktet en gang til under den samme fotsepisoden hvis det ikke har fungert etter den første applikasjonen.
Du må bruke LAMISILMONO på begge føttene, selv om merkene bare er synlige på den ene foten. Dette sikrer fullstendig eliminering av soppen: den kan være tilstede i andre deler av foten, selv om ingen lesjoner er synlige.
Etter påføring på føttene tørker medisinen raskt og blir en gjennomsiktig film.
- Røret inneholder nok medisin til å behandle begge føttene
LAMISILMONO slipper ut den aktive ingrediensen i huden der den forblir i et antall dager for å eliminere soppen som forårsaker fotsopp. For best resultat bør føttene ikke vaskes eller våte i 24 timer etter påføring.
For å fremme behandling
Hold det berørte området rent ved å vaske det regelmessig etter de første 24 timene. Tørk det grundig uten å massere. Prøv å ikke klø området selv om det er kløende, da dette kan forårsake ytterligere skade og bremse helbredelsesprosessen eller spre infeksjonen.
Siden disse infeksjonene kan overføres til andre mennesker, må du huske å bare holde håndkleet og klærne for deg selv og ikke dele dem med andre. Vask klærne og håndklærne ofte for å beskytte deg mot reinfeksjon.
Overdosering Hva du skal gjøre hvis du har tatt for mye Lamisilmono
Hvis du ved et uhell svelger et produkt
Kontakt legen din som vil gi deg råd om hva du skal gjøre. Alkoholinnholdet må tas i betraktning
Hvis produktet kommer i kontakt med ansikt eller øyne
Skyll ansiktet eller øynene med rennende vann. Gå til legen din hvis du fortsatt har ubehag.
[Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette legemidlet.]
Bivirkninger Hva er bivirkningene av Lamisilmono
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Noen mennesker kan være allergiske mot LAMISILMONO, som kan forårsake hevelse og smerte, hudutslett eller elveblest. Dette har blitt rapportert svært sjelden (kan forekomme hos opptil 1 av 100 personer).
Hvis du opplever en allergisk reaksjon eller noen av symptomene ovenfor når du bruker dette produktet, fjern folien med denaturert alkohol (kan kjøpes på apoteket), vask føttene med varmt såpevann, skyll og tørk dem og kontakt lege eller apotek. .
Følgende bivirkninger er rapportert:
uvanlig (de kan ramme opptil 1 av 100 mennesker)
Reaksjoner på applikasjonsstedet som kan omfatte tørr hud, hudirritasjon eller en brennende følelse.
Disse reaksjonene er vanligvis milde og forbigående.
Rådfør deg med lege eller apotek dersom du får bivirkninger. Dette inkluderer eventuelle bivirkninger som ikke er nevnt i dette pakningsvedlegget.
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Bruk ikke LAMISILMONO etter utløpsdatoen som er angitt på esken og røret. Utløpsdatoen refererer til den siste dagen i måneden som er angitt.
Oppbevares i originalpakningen for å beskytte mot lys. Må ikke oppbevares over 30 ° C.
Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
LAMISILMONO inneholder
- Den aktive ingrediensen er terbinafin (som hydroklorid). Hvert gram kutan løsning inneholder 10 mg terbinafin (som hydroklorid).
- Andre innholdsstoffer er: akrylater / oktylakrylamid -kopolymer, hydroksypropylcellulose, mellomkjede mettede triglyserider og etanol.
Beskrivelse av utseendet til LAMISILMONO og innholdet i pakningen
LAMISILMONO er en klar eller lett ugjennomsiktig viskøs løsning. Den er tilgjengelig i 4g rør.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
LAMISILMONO 1% HUDLØSNING
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hvert gram kutan løsning inneholder 10 mg terbinafin (som hydroklorid).
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Hudløsning.
Klar eller lett ugjennomsiktig viskøs løsning.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Behandling av tinea pedis (fotsopp) (se pkt. 4.4).
04.2 Dosering og administrasjonsmåte
Kutan bruk.
Dosering
Voksne: en enkelt applikasjon.
Lamisilmono trenger bare påføres én gang på begge føttene, selv om lesjonene bare er synlige på den ene foten. Dette sikrer eliminering av sopp (dermatofytter) som kan være tilstede i områder av foten der ingen lesjoner er synlige.
Administrasjonsmåte
Pasienter bør vaske og tørke både føtter og hender før de påfører medisinen. De må behandle den ene foten, deretter den andre.
Fra og med tærne, bør pasientene legge et tynt lag mellom og rundt tærne jevnt, samt dekke sålen og sidene av foten med opptil 1,5 cm. Legemidlet skal påføres på samme måte på den andre foten, selv om huden ser sunn ut. Legemidlet skal tørke i 1-2 minutter til det dannes en film. Pasienter bør deretter vaske hendene. Lamisilmono skal ikke massert inn i huden.
For best resultat bør behandlede områder ikke vaskes i 24 timer etter påføring. Det anbefales derfor å påføre Lamisilmono etter dusj eller badekar og vente til samme tid neste dag før du forsiktig vasker føttene igjen.; Etter vask, føttene bør tørkes ved å dyppe forsiktig.
Pasienter bør bruke den nødvendige mengden for å dekke begge føttene som vist ovenfor. Eventuell gjenværende medisin skal kastes.
Lindring av kliniske symptomer ses vanligvis innen få dager.
Hvis det ikke er tegn til bedring etter en uke, bør diagnosen gjennomgås, og pasienter bør deretter kontakte lege. Det er ingen data om gjentatt behandling med Lamisilmono. Derfor kan en annen behandling ikke anbefales under den samme fotsepisoden.
Dosering i spesielle populasjoner:
Pediatrisk populasjon
Lamisilmono har ikke blitt studert i den pediatriske populasjonen. Derfor er bruken ikke anbefalt hos pasienter under 18 år.
Eldre pasienter
Ingen dosejustering er nødvendig.
04.3 Kontraindikasjoner
Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene listet opp i pkt.6.1.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Lamisilmono bør brukes med forsiktighet hos pasienter med skader der alkohol kan være irriterende, og det skal ikke brukes i ansiktet.
Lamisilmono er kun til ekstern bruk. Det kan være irriterende for øynene.
Skyll øynene grundig med rennende vann ved tilfeldig kontakt med øynene.
Lamisilmono må oppbevares utilgjengelig for barn.
Lamisilmono anbefales ikke for behandling av kronisk hyperkeratotisk ("moccasin" type) plantar tinea pedis.
Ved en allergisk reaksjon bør filmen fjernes med et organisk løsningsmiddel som denaturert alkohol og føttene vaskes med varmt såpevann.
Informasjon om hjelpestoffer
Lamisilmon inneholder etanol; hold deg unna åpen ild.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Det er ingen kjente legemiddelinteraksjoner med Lamisilmono.
04.6 Graviditet og amming
Svangerskap
Det er ingen klinisk erfaring med terbinafin hos gravide.
Fostertoksisitetsstudier på dyr indikerer ikke bivirkninger (se pkt. 5.3) Lamisilmono skal ikke brukes under graviditet med mindre det er nødvendig.
Foringstid
Terbinafin skilles ut i morsmelk. Lamisilmono skal ikke brukes mens du ammer.
Fruktbarhet
Dyrestudier viste ingen effekt av terbinafin på fruktbarhet (se pkt. 5.3).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Lamisilmono påvirker ikke evnen til å kjøre bil og bruke maskiner.
04.8 Bivirkninger
Bivirkninger inkluderer milde og forbigående reaksjoner på applikasjonsstedet. I svært sjeldne tilfeller kan allergiske reaksjoner oppstå.
Hud og subkutant vev:
Svært sjelden (kløe, bullous dermatitt og urticaria.
Generelle lidelser og tilstander på administrasjonsstedet:
Mindre vanlige (> 1/1000,
04.9 Overdosering
Ved utilsiktet inntak må alkoholinnholdet (81,05 vekt / vekt) av Lamisilmono tas i betraktning.
En overdose er svært lite sannsynlig, ettersom medisinen er til engangsbruk, til kutan bruk og røret inneholder bare den mengden som trengs for en applikasjon. Utilsiktet inntak av produktet i et 4 g rør som inneholder 40 mg terbinafin er mye redusert sammenlignet med å ta en 250 mg Lamisil tablett (oral doseringsenhet for voksne). Skulle imidlertid flere rør med Lamisilmono inntas utilsiktet, må det forventes bivirkninger som ligner dem som ble sett etter overdose med Lamisil -tabletter. Disse inkluderer hodepine, kvalme, epigastriske smerter og svimmelhet.
Behandling av overdose
Ved utilsiktet inntak er den anbefalte behandlingen av overdosering å eliminere virkestoffet, hovedsakelig ved administrering av aktivt kull, og om nødvendig for å gi symptomatisk støttende behandling.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: andre soppdrepende midler for lokal bruk.
ATC -kode: D01AE15.
Terbinafine er et allylamin som spesifikt forstyrrer biosyntesen av soppsteroler i et innledende trinn.Dette fører til mangel på ergosterol og en intracellulær opphopning av squalen, noe som resulterer i soppcellens død. Terbinafin virker ved å hemme soppcellen. Squalenepoksidase i soppcellemembranen. Enzymet squalenepoksidase er ikke bundet til cytokrom P450 -systemet. Terbinafin påvirker ikke metabolismen av hormoner eller andre legemidler.
Terbinafine har et bredt spekter av soppdrepende aktivitet ved sopphudinfeksjoner forårsaket av dermatofytter som f.eks Trichophyton (f.eks.T. rubrum, T. mentagrophytes, T. verrucosum, T. violaceum), Microsporum canis og Epidermophyton floccosum. Ved lave konsentrasjoner er terbinafin soppdrepende middel mot dermatofytter.
Pasientstudier har vist at påføring av en enkelt dose Lamisilmono 1% kutan oppløsning på begge føtter har vist seg å være effektiv hos pasienter med tinea pedis (fotsopp) som hadde interdigitale lesjoner, og som strakte seg til tilstøtende områder. sider og fotsåler.
Imidlertid har det ikke blitt utført en direkte sammenligning av effekt med andre topiske former for Lamisil, derfor kan det for øyeblikket ikke vurderes om den relative effekten av Lamisilmono 1% kutan løsning sammenlignet med andre topiske former.
05.2 Farmakokinetiske egenskaper
Etter påføring på huden danner Lamisilmono 1% kutan løsning en film på huden. Terbinafin vil sannsynligvis bli bundet eller beholdt i lipidkomponentene i stratum corneum, noe som kan spille en rolle i den lange eliminasjonshalveringstiden for dette legemidlet fra stratum corneum. Terbinafin forblir i stratum corneum i opptil 13 dager, på nivåer som overstiger minimum in vitro inhiberende konsentrasjon av terbinafin på dermatofytter.
Vasking av filmen reduserer terbinafininnholdet i stratum corneum, og derfor bør vask unngås de første 24 timene etter påføring for å tillate maksimal penetrering av terbinafinet i stratum corneum.
Okklusjon, som sannsynligvis vil bli vurdert ved terapeutisk bruk, vil resultere i en 2,7 ganger økning i stratum corneum-eksponering for terbinafin etter en enkelt påføring av Lamisilmon 1% kutan oppløsning. pasienter med tinea pedis enn hos friske frivillige på ryggen. Dette skyldes den okklusive effekten som finnes i de interdigitale mellomrommene, som sannsynligvis økes ved "bruk av sko, snarere enn noen effekt forårsaket av svekket" integritet av stratum corneum.
Systemisk biotilgjengelighet er veldig lav hos både friske frivillige og pasienter.
En "påføring av Lamisilmono 1% kutan løsning på ryggen, over et" område 3 ganger større enn arealet på begge føtter, resulterte i en "estimert eksponering for terbinafin på mindre enn 0,5% av eksponeringen etter administrering per oralt en tablett på 250 mg.
05.3 Prekliniske sikkerhetsdata
I langtidsstudier (opptil 1 år) på rotter og hunder ble det ikke sett noen markante toksiske effekter hos noen av artene opp til orale doser på omtrent 100 mg / kg per dag. Ved høye orale doser har leveren og muligens også nyrene blitt identifisert som potensielle målorganer.
I en 2-årig oral karsinogenitetsstudie hos mus var det ingen neoplastiske eller andre unormale funn som kan tilskrives behandling med doser på opptil 130 (hanner) og 156 (hunner) mg / kg per dag. I en 2-årig oral karsinogenisitetsstudie hos rotter med den høyeste dosen, 69 mg / kg per dag, ble det observert en økt forekomst av levertumorer hos hanner. Endringene, som kan være forbundet med spredning av peroksisomer, har vist seg å være artsspesifikke siden de ikke ble observert i karsinogenitetsstudien på mus eller i andre studier på mus, hunder eller aper.
Under studier med høye orale doser terbinafin hos aper, ble det observert brytningsregelmessigheter i netthinnen ved høyere doser (det giftfrie nivået var 50 mg / kg). Disse uregelmessighetene var forbundet med tilstedeværelsen av en terbinafinmetabolitt i okulært vev og forsvant etter seponering av legemidlet. De var ikke forbundet med histologiske endringer.
Et standard sett med tester å evaluere in vitro Og in vivo gentoksisitet viste ikke noe mutagent eller klastogent potensial for stoffet.
Ingen negative effekter på fruktbarhet eller andre reproduktive parametere ble observert i studier på rotter og kaniner.
Gjentatt påføring på huden av Lamisilmono 1% kutan løsning på rotter og miniatyrgriser gir plasmanivåer av terbinafin som er minst 50-100 ganger lavere enn de som er fastslått som ingen bivirkningsnivåer i terbinafindyretoksisitetsstudier, derfor bruk av legemidlet forventes ikke å gi noen systemiske bivirkninger.
Lamisilmon 1% kutan løsning ble godt tolerert i mange tolerabilitetsstudier og induserte ikke sensibilisering.
Sikkerheten til akrylat / oktylakrylamid -kopolymeren, et nylig brukt hjelpestoff i aktuelle dermatologiske legemidler, er etablert basert på konvensjonelle studier av enkelt- og gjentatt dosetoksisitet, gentoksisitet og lokal toleranse.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Akrylater / oktylakrylamid -kopolymer; hydroksypropylcellulose; mettede triglyserider med middels kjede; etanol.
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
3 år.
06.4 Spesielle forholdsregler for lagring
Oppbevares i originalpakningen for å beskytte mot lys. Må ikke oppbevares over 30 ° C.
06.5 Emballasje og innhold i pakningen
4 g laminerte aluminiumsrør (polyetylen-aluminium-polyetylen) med skruehette av polyetylen.
06.6 Bruksanvisning og håndtering
Ingen spesielle instruksjoner.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
Novartis Farma S.p.A., Largo U. Boccioni 1 - Origgio (VA).
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
4 g rør - A.I.C. n. 038282012 / M.
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Første autorisasjon: januar 2008.
Fornyelse: 4. november 2010.
10.0 DATO FOR REVISJON AV TEKSTEN
20. januar 2013.