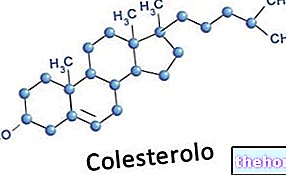
Glykogen er et makromolekyl (molekylmasse på omtrent 400 millioner dalton) av α-glukose der det hovedsakelig er α-1,4 glykosidbindinger og forgreninger i et forhold på 1:10, på grunn av α-1,6 glykosidbindinger.
Glykogen utgjør reservemateriale og nedbrytes og rekonstitueres kontinuerlig; i hele kroppens cellemasse er det omtrent 100 g glykogen: det meste er i leveren der det er mobilt og kan derfor brukes som reserve for andre organer (glykogen i muskler er ikke mobilt).
Enzymene som katalyserer nedbrytningen og syntesen av glykogen er alle i cytoplasmaet, derfor er det nødvendig med et reguleringssystem som gjør den ene banen inaktiv når den andre er aktiv: hvis det er glukose tilgjengelig, omdannes sistnevnte til glykogen (anabolisme) som er en reserve, omvendt, hvis c "er nødvendig for glukose, nedbrytes glykogenet (katabolisme).

Enzymet som hovedsakelig er involvert i nedbrytningen av glykogen er glykogenfosforylase; dette enzymet er i stand til å spalte en glykosidisk α-1,4-binding ved bruk av et uorganisk ortofosfat som lytisk middel: spaltningen skjer på fosforolytisk måte og glukose 1-fosfat oppnås.
Ved fem eller seks enheter fra et forgreningspunkt er glykogenfosforylase -enzymet ikke lenger i stand til å virke, derfor løsner det fra glykogenet og erstattes av et deramifiserende enzym som er et transferase: i det katalytiske stedet for dette enzymet c "er et" histidin som tillater overføring av tre sakkaridenheter til nærmeste glykosidkjede (histidin angriper det første karbonet i et glukosemolekyl). Enzymet som nettopp er nevnt er glykosyltransferase; på slutten av virkningen av dette enzymet er det bare én glukoseenhet igjen på sidekjeden med det første karbonet bundet til det sjette karbonet i en glukose i hovedkjeden Den siste glukosenheten i sidekjeden frigjøres ved virkningen av "enzym α-1,6 glykosidase (dette enzymet utgjør den andre delen av det deramifiserende enzymet); gitt at grenene i glykogen er i et forhold på 1:10, fra fullstendig nedbrytning av makromolekylet får vi omtrent 90% glukose 1-fosfat og omtrent 10% av glukose.
Virkningen av de nevnte enzymer tillater eliminering av en sidekjede fra glykogenmolekylet; aktiviteten til disse enzymene kan gjentas til fullstendig nedbrytning av kjeden skjer.
La oss vurdere en hepatocytt; glukose (assimilert gjennom dietten), når den kommer inn i cellen omdannes til glukose 6-fosfat og aktiveres dermed. Glukose 6-fosfat, ved virkningen av fosfoglukomutase, transformeres til glukose 1-fosfat: sistnevnte er en ikke-umiddelbar forløper for biosyntese; i biosyntese brukes en aktivert form av sukker som er representert ved sukker knyttet til et difosfat: vanligvis uridyldifosfat (UDP). Glukose 1- fosfat er deretter omdannet til UDP-glukose, denne metabolitten under virkningen av glykogensyntase som er i stand til å binde UDP-glukose til en ikke-reduserende ende av det voksende glykogenet: Langstrakt glykogen fra en glukosidisk enhet og UDP oppnås UDP omdannes av det nukleosiderte difosfokinase-enzymet til UTP som går tilbake til sirkulasjonen.
Nedbrytningen av glykogen skjer ved virkningen av glykogenfosforylase som frigjør et molekyl av glukose og omdanner det til glukose 1-fosfat. Deretter omdanner fosfoglukomutase glukose 1-fosfat til glukose 6-fosfat.
Glykogen syntetiseres fremfor alt i lever og muskler: i organismen er det 1-1,2 hektar glykogen fordelt gjennom muskelmassen.
Glykogenet til en myocytt representerer bare en energireserve for denne cellen, mens glykogenet i leveren også er en reserve for andre vev, det vil si at det kan sendes som glukose til andre celler.
Glukose 6-fosfatet oppnådd i musklene fra nedbrytningen av glykogen sendes deretter, i tilfelle av energibehov, til glykolyse; i leveren omdannes glukose 6-fosfat til glukose ved virkningen av glukose 6-fosfatfosfatase (karakteristisk enzym for hepatocytter) og overføres til blodet.
Glykogensyntase og glykogenfosforylase virker begge på de ikke-reduserende enhetene av glykogen, så det må være et hormonalt signal som kommanderer aktivering av den ene veien og blokkering av den andre (eller omvendt).
I laboratoriet var det mulig å forlenge glykogenkjeden ved å utnytte glykogenfosforylase og bruke glukose 1-fosfat i en meget høy konsentrasjon.
I celler katalyserer glykogenfosforylase bare nedbrytningsreaksjonen fordi konsentrasjonene av metabolittene er slik at de flytter likevekten til den følgende reaksjonen til høyre (dvs. mot nedbrytning av glykogen):

La oss se virkningsmekanismen for glykogenfosforylasen: Acetal oksygen (som fungerer som en bro mellom glukoseenhetene) binder seg til fosforylets hydrogen: et reaksjonsmellomprodukt dannes gitt av en karbokasjon (på glukosen som er alt " ekstremiteter) som fosforyl (Pi) binder seg veldig raskt til.
Glykogenfosforylase krever en kofaktor som er pyridoksalfosfat (dette molekylet er også en kofaktor for transaminaser): den har en delvis protonert fosforyl (pyridoksalfosfat er omgitt av et hydrofobt miljø som begrunner tilstedeværelsen av protoner bundet til det). Fosforyl (Pi) er i stand til å overføre et proton til glykogenet fordi dette fosforylet deretter henter protonen tilbake fra det delvis protonerte fosforylet til pyridoksalfosfatet. Sannsynligheten for at fosforyl ved fysiologisk pH mister protonen og forblir fullstendig deprotonert er veldig lav.
La oss nå se hvordan fosfoglukomutase fungerer. Dette enzymet presenterer i det katalytiske setet en rest av fosforylert serin; serin gir fosforyl til glukose 1-fosfat (i posisjon seks): glukose 1,6-bisfosfat dannes i kort tid, deretter refosforyleres serin og tar fosforylet i posisjon ett. Phosphogluco mutase kan virke i begge retninger, dvs. konvertere glukose 1-fosfat til glukose 6-fosfat eller omvendt; Hvis glukose 6-fosfat produseres, kan det sendes direkte til glykolyse, i musklene, eller omdannes til glukose i leveren.
Enzymet uridylfosfogluco -transferase (eller UDP -glukosepyrofosforylase) katalyserer glukose 1-fosfatoverføringsreaksjonen til UTP ved binding til fosforyl a.
Enzymet som nettopp er beskrevet er en pyrofosforylase: dette navnet skyldes at den motsatte reaksjonen til den som nettopp er beskrevet er en pyrofosforylering.
UDP -glukose, oppnådd som beskrevet, er i stand til å forlenge glykogenkjeden med en monosakkaridenhet.
Det er mulig å få reaksjonen til å utvikle seg mot dannelsen av UDP -glukose ved å eliminere et produkt som er pyrofosfat; enzymet pyrofosfatase omdanner pyrofosfat til to molekyler ortofosfat (hydrolyse av et anhydrid) og holder på den måten konsentrasjonen av pyrofosfat så lav at prosessen med dannelse av UDP -glukose blir termodynamisk favorisert.
Som nevnt er UDP -glukose, takket være virkningen av glykogensyntase, i stand til å forlenge glykogenkjeden.
Forklaringene (i et forhold på 1:10) skyldes det faktum at når et glykogenkjede består av 20-25 enheter, griper et forgreningsenzym (som har et "histidin på det katalytiske stedet) i stand til å overføre en rekke 7-8 glykosidiske enheter lenger nedstrøms 5-6 enheter: dermed genereres en ny forgrening.
Av årsaker til nervøs opprinnelse eller hvis det er behov for energi på grunn av fysisk anstrengelse, skilles adrenalin ut fra binyrene.
Målcellene til adrenalin (og noradrenalin) er lever, muskler og fettvev (i sistnevnte er det nedbrytning av triglyserider og sirkulasjon av fettsyrer: følgelig produseres glukose i mitokondriene 6 -fosfat, som skal sendes til glykolyse, mens glukose 6-fosfat i adipocytter transformeres til glukose ved virkningen av enzymet glukose 6-fosfatfosfatase og eksporteres til vevet).
La oss se, nå virkemåten for adrenalin. Adrenalin binder seg til en reseptor plassert på cellemembranen (av myocytter og hepatocytter) og dette bestemmer translasjonen av signalet fra utsiden til innsiden av cellen. Proteinkinasen aktiveres som virker samtidig på systemene som regulerer syntese og nedbrytning av glykogen:
Glykogensyntase eksisterer i to former: en defosforylert (aktiv) form og en fosforylert (inaktiv) form; proteinkinase fosforylerer glykogensyntase og blokkerer virkningen.
Glykogenfosforylase kan eksistere i to former: en aktiv form der en fosforyleret serin er tilstede og en inaktiv form der serin defosforyleres. Glykogenfosforylase kan aktiveres av enzymet glykogenfosforylase kinase. Glykogenfosforylasekinase er aktiv hvis den fosforyleres og inaktiv hvis den defosforyleres; proteinkinasen har som substrat glykogenfosforylasekinasen, det vil si at den er i stand til å fosforylere (og derfor aktivere) sistnevnte som igjen aktiverer glykogenfosforylasen.
Når adrenalinsignalet er over, må effekten det har på cellen også ta slutt: fosfataseenzymer griper deretter inn på proteinartene.