Struktur og funksjoner
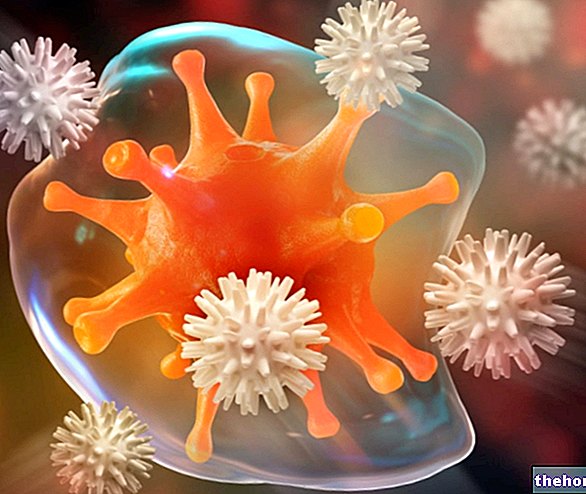
Hemoglobin er et metalloprotein som finnes i røde blodlegemer, som er ansvarlig for å transportere oksygen i blodet. Faktisk er oksygen bare moderat løselig i vann; Derfor er mengdene oppløst i blodet (mindre enn 2% av totalen) ikke tilstrekkelige til å tilfredsstille stoffskiftet i vevet. Behovet for en spesifikk transportør er derfor tydelig.
I blodet kan oksygen ikke binde seg direkte og reversibelt til proteiner, slik det forekommer i stedet for metaller som kobber og jern. Ikke overraskende finner vi i midten av hver proteinunderenhet av hemoglobin, innpakket i et proteinskall, den såkalte protesen gruppe EME, med et metallisk hjerte representert av et jernatom i Fe2 + oksidasjonstilstanden (redusert tilstand), som binder oksygen på en reversibel måte.
Blodanalyse
- Normale hemoglobinverdier i blodet: 13-17 g / 100 ml
Hos kvinner er verdiene i gjennomsnitt 5-10% lavere enn hos menn.
Mulige årsaker til høyt hemoglobin
- Polycytemi
- Forlenget opphold på høy bakken
- Kroniske lungesykdommer
- Hjertesykdom
- Bloddoping (bruk av erytropoietin og derivater eller stoffer som etterligner virkningen)
Mulige årsaker til lavt hemoglobin
- Anemier
- Jernmangel (jernmangel)
- Rikelig blødning
- Karsinomer
- Svangerskap
- Thalassemias
- Burns
Oksygeninnholdet i blodet er derfor gitt ved summering av den lille mengden oppløst i plasma med fraksjonen bundet til hemoglobinjern.
Mer enn 98% av oksygenet i blodet er bundet til hemoglobin, som igjen sirkulerer i blodet som er tilordnet i de røde blodcellene. Uten hemoglobin kunne derfor erytrocytter ikke utføre sin oppgave som oksygen transportører i blodet.
Gitt dette metallets sentrale rolle, krever syntesen av hemoglobin et tilstrekkelig inntak av jern i kosten. Omtrent 70% av jernet som finnes i kroppen er faktisk inneholdt i hemgruppene av hemoglobin.
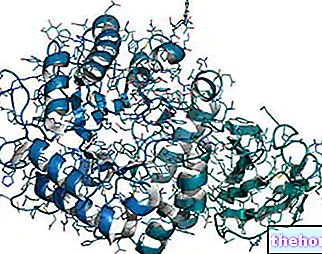
Hemoglobin består av 4 underenheter som strukturelt ligner myoglobin *.
* Mens hemoglobin transporterer oksygen fra lungene til vevet, transporterer myoglobin oksygenet som frigjøres av hemoglobin til de forskjellige cellulære organellene som bruker det (f.eks. Mitokondrier).

Hemoglobin er et stort og komplekst metalloprotein, preget av henholdsvis fire kuleformede proteinkjeder viklet rundt en hemegruppe som inneholder Fe2 +.
For hvert hemoglobinmolekyl finner vi derfor fire hemgrupper pakket inn i den relative globulære proteinkjeden. Siden det er fire jernatomer i hvert hemoglobinmolekyl, kan hvert hemoglobinmolekyl binde fire oksygenatomer til seg selv, i henhold til den reversible reaksjonen:
Hb + 4O2 ← → Hb (O2) 4
Som de fleste vet, er hemoglobins oppgave å ta oksygen i lungene, frigjøre det til cellene som trenger det, ta karbondioksid fra dem og slippe det ut i lungene der chiloen begynner igjen.
Under blodpassasjen i kapillærene i lungealveolene binder hemoglobin oksygen til seg selv, som deretter frigjøres til vevet i den perifere sirkulasjonen. Denne utvekslingen skjer fordi oksygenbindingene med jernet i EME -gruppen er labile og følsomme for mange faktorer, hvorav den viktigste er spenningen eller delvis trykk av oksygen.
Binding av oksygen til hemoglobin og Bohr -effekten
I lungene øker oksygenspenningen i plasma på grunn av diffusjon av gass fra alveolene til blodet (↑ PO2); denne økningen får hemoglobin til å binde ivrig til oksygen; det motsatte skjer i det perifere vevet, hvor konsentrasjonen av oppløst oksygen i blodet synker (↓ PO2) og partialtrykket av karbondioksid øker (↑ CO2); dette får hemoglobin til å frigjøre oksygen og bli ladet med CO2. Forenkle konseptet så mye som mulig, jo mer karbondioksid som er tilstede i blodet, jo mindre oksygen forblir bundet til hemoglobin.
Selv om mengden oksygen fysisk oppløst i blodet er veldig lav, spiller det derfor en grunnleggende rolle. Faktisk påvirker denne mengden sterkt bindingsstyrken mellom oksygen og hemoglobin (i tillegg til at den representerer en "viktig referanseverdi for regulering av lungeventilasjon).
Oppsummerer alt med en graf, øker mengden oksygen knyttet til hemoglobin i forhold til pO2 etter en sigmoidkurve:

Det faktum at plateu -regionen er så stor, plasserer en viktig sikkerhetsmargin ved maksimal metning av hemoglobin under passasjen til lungene. Selv om pO2 på alveolært nivå normalt er lik 100 mm Hg, observerer vi figuren faktisk hvordan Selv et delvis oksygentrykk lik 70 mmHg (typisk forekomst av noen sykdommer eller opphold i store høyder), forblir prosentandelen av mettet hemoglobin nær 100%.
I området med maksimal skråning, når oksygen delvis spenning faller under 40 mmHg, faller hemoglobins evne til å binde oksygen plutselig.
Under hvileforhold er PO2 i intracellulære væsker omtrent 40 mmHg; på dette stedet, på grunn av gasslovene, diffunderer oksygenet som er oppløst i plasmaet mot det dårligere vevet av O2, og krysser kapillærmembranen. Følgelig synker plasmaspenningen til O2 ytterligere, og dette favoriserer frigjøring av oksygen fra hemoglobinet. . Under intens fysisk anstrengelse faller derimot oksygenspenningen i vevene til 15 mmHg eller mindre, noe som resulterer i at blodet er sterkt tømt for oksygen.
For det som er sagt, i hvileforhold forlater en viktig mengde oksygenert hemoglobin vevet, og forblir tilgjengelig ved behov (for eksempel for å håndtere en plutselig økning i metabolisme i noen celler).
Den heltrukne linjen vist på bildet ovenfor kalles hemoglobindissosiasjonskurven; det bestemmes vanligvis in vitro ved pH 7,4 og ved en temperatur på 37 ° C.
Bohr -effekten har konsekvenser både for inntak av O2 på lungenivå og for frigjøring på vevsnivå.
Der det er mer oppløst karbondioksid i form av bikarbonat, frigjør hemoglobin lettere oksygen og blir ladet med karbondioksid (i form av bikarbonat).

Den samme effekten oppnås ved å forsure blodet: jo mer blodets pH synker og jo mindre oksygen forblir bundet til hemoglobinet; ikke overraskende oppløses karbondioksid i blodet hovedsakelig i form av karbonsyre, som dissosierer.



Til ære for oppdageren er effekten av pH eller karbondioksid på oksygendissosiasjon kjent som Bohr -effekten.
Som forventet frigjør hemoglobin i et surt miljø lettere oksygen, mens bindingen med oksygen i et grunnleggende miljø er sterkere.

Andre faktorer som er i stand til å endre hemoglobins affinitet for oksygen inkluderer temperatur. Spesielt reduseres affiniteten til hemoglobin for oksygen med økende kroppstemperatur. Dette er spesielt fordelaktig i vinter- og vårmånedene, siden temperaturen i lungeblodet (i kontakt med luften i det ytre miljøet) er lavere enn det som nås i vevet, der frigjøring av oksygen derfor er lettere.

2.3 difosfoglyserat er et mellomprodukt i glykolyse som påvirker hemoglobins affinitet for oksygen. Hvis konsentrasjonene i de røde blodcellene øker, reduseres affiniteten til hemoglobin for oksygen, og letter frigjøring av oksygen til vevet. Ikke overraskende erytrocytkonsentrasjonene av 2,3 difosfoglyserat øker for eksempel i anemi, hjerte-lungeinsuffisiens og under oppholdet i stor høyde.
Generelt er effekten av 2,3 bisfosfoglyserat relativt treg, spesielt sammenlignet med den raske responsen på endringer i pH, temperatur og delvis trykk av karbondioksid.

Bohr -effekten er veldig viktig under intens muskelarbeid; under slike forhold er det faktisk en økning i temperaturen og trykket av karbondioksid, derfor i blodets surhet, i de vevene som er mest utsatt for stress. Som forklart ovenfor, favoriserer alt dette frigjøring av oksygen til vevet, og forskyver hemoglobindissosiasjonskurven til høyre.
























.jpg)