For toksikodynamikk, på godt og vondt, blir konseptene sett for farmakodynamikk tatt opp. Konseptene interaksjon med en reseptor på en uspesifikk og spesifikk måte, substrat (toksiske) reseptorinteraksjoner, affiniteten til det toksiske på reseptoren, styrken og til slutt antagonismen må være godt kjent. Disse begrepene tas ikke opp fordi de er de samme som er illustrert for stoffet; men vi vil gå i detalj på noen typiske virkningsmekanismer for giftige stoffer.
Det giftige, i likhet med stoffet, virker med målmolekylet, som vil være det første studiepunktet.
HVA ER GIFTENS MÅL? Målet for det giftige er cellen, som består av proteiner, lipider, nukleinsyrer og andre komponenter.
Det andre studiepunktet er typen kobling mellom det giftige og målcellen, en viktig faktor for den alvorlige effekten av det giftige. Som vi vet, kan koblingen være reversibel og irreversibel.
Hvis giftstoffet er reversibelt bundet, kan det løsne og effekten er mindre alvorlig enn når den binder seg til målet med en kovalent binding, derfor irreversibel.

Det tredje studiepunktet består i konsekvensene av samspillet mellom det giftige og målcellen.
Hva endrer det giftige ved å binde seg til et målmolekyl?
Det kan være en endring av energiproduksjonen, slik at cellen ikke produserer ATP og går mot døden; det kan være en modifikasjon av homeostase av intracellulært kalsium, som er en av de viktigste andre budbringerne, eller endelig kan det være en endring av plasmamembranen.
Dette er alle eksempler på mobilfunksjoner som endres av giftstoffet ved binding til målstedet.
MÅLMOLEKYLENE
Som nevnt tidligere består cellen av proteiner, lipider, nukleinsyrer og andre komponenter.
De mulige målmolekylene er derfor:
- PROTEINER (membran, enzymer ...);
- LIPIDS (membranfosfolipider);
- GRUPPER -SH (cytoskjelettproteiner);
- NUCLEIC ACIDS (vil bli forklart i en artikkel om karsinogenese og DNA -skade).
1) PROTEINMÅL
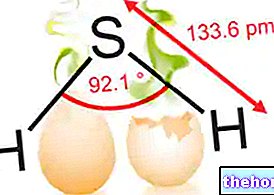
Her er noen eksempler på proteinmål. I det første eksemplet vurderer vi et "hemoprotein som er hemoglobin", og en veldig lignende giftig, som er karbonmonoksid (CO). Kullmonoksid, som er 250 ganger mye mer lik oksygen, binder seg til -EME -gruppen av hemoglobin, og forhindrer dermed transport av oksygen.Vevscellene dør av ANEMISK HYPOXIA fordi de ikke mottar nødvendig oksygen for cellulær respirasjon.
I det andre eksemplet blir det tatt i betraktning et enzymatisk proteinmolekyl, som er Cyt C -oksidase, og det relaterte giftige cyanidet. Cyt C oxidase er et enzym som tilhører elektrontransportkjeden. Cellulær respirasjon skjer på nivået av mitokondrion og Cyt C -oksidasen utnytter oksygen for å sikre at fire H + -ioner blir utvist fra mitokondrien; denne utstøtingen av hydrogenioner danner den potensielle forskjellen som er nødvendig for syntesen av ATP. Enzymet er blokkert av cyanid , Cyt C -oksidase bruker ikke lenger molekylært oksygen, den optimale protongradienten dannes ikke utenfor mitokondrien; følgelig syntetiserer ikke cellen ATP. Også i dette tilfellet går cellene mot døden på grunn av hypoksi; vi snakker spesielt om CYTOTOXIC HYPOXIA.
Blant alle proteinmålene finner vi reseptorene som er forklart i generell farmakologi. De viktigste toksinene, som nikotin og stryknin, kan samhandle med forskjellige reseptorer.
2) FETTE MÅL
Lipidene som er mest påvirket av frie radikaler er membranen. Frie radikaler, fra kjemisk synspunkt, dannes fordi det ikke er noen "heterolyse" mellom to atomer, derfor dannes ikke to ioner med en homogen ladning, men det er en "homolyse".
Homolyse er preget av en ujevn fordeling av ladningene.

Frie radikaler dannes av eksterne stoffer (xenobiotika), men også inne i organismen vår (oksygenfrie radikaler). Vi kan derfor si at frie radikaler kan dannes både utenfra og fra innsiden av organismen vår.
Hvordan dannes disse radikalene?
Frie oksygenradikaler kan dannes når det er en endring i oksygenpartialspenningen i cellen, så det er plutselige endringer i oksygenpresset. Disse plutselige oksygenmangel favoriserer dannelsen av radikale arter i iskemisk (hjerne) eller hjertevev. De radikale oksygenartene er hovedsakelig SUPEROXIDE ANION og OXIDRILE. Mangelen på antioksidanter (vitamin A, C og E), cellulær aldring, xenobiotika og til slutt de akutte og / eller kroniske inflammatoriske tilstandene er alle fenomener som de kan føre til dannelse av frie radikaler.

Cellen kan reagere på disse mulige skadene på grunn av begynnelsen av oksygenfrie radikaler, fordi den har spesielle enzymer som motvirker aktiviteten til radikalene.

Andre artikler om "Toxicodynamics"
- Paracetamol og levernekrose
- Giftighet og toksikologi
- Målmolekyler av giftige stoffer