Se videoen
- Se videoen på youtube
Se også: typer bacon og helse
Generellitet
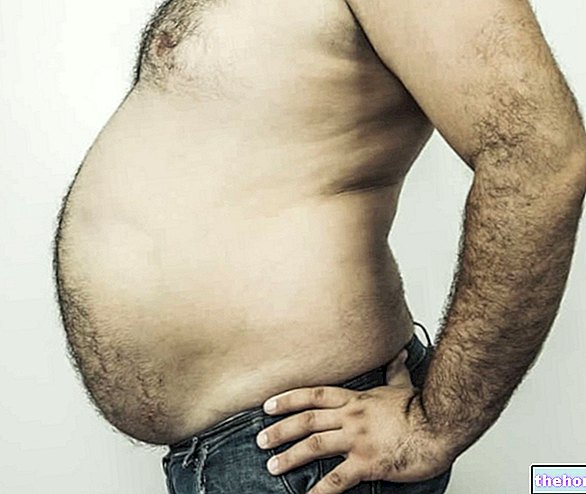
Visceralt fett - også kjent som magefett - er den delen av fettvev som er konsentrert i bukhulen og fordelt mellom de indre organene og stammen.
Visceralt fett skiller seg fra subkutant fett - konsentrert i hypodermis (det dypeste laget av huden) - og fra intramuskulært fett, som i stedet fordeles mellom muskelfibrene (sistnevnte ser også ut til å være signifikant korrelert med insulin. Resistens).
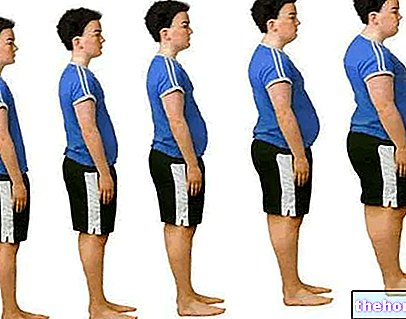
Abdominal fedme
"Overskudd av magefett er definert av begrepene" sentral fedme "," abdominal fedme "og" android fedme ". Med denne siste termen ønsker vi å understreke den typiske sammenhengen mellom visceralt fett med mannlig kjønn og hans hormoner (kalt nøyaktig androgener).
Behovet for å differensiere denne formen for fedme fra den gynoidale - typisk for det kvinnelige kjønn og preget av fettakkumuleringer konsentrert i den nedre delen av magen, i gluteal og i femoralregionene - stammer fra den forskjellige påvirkningen av de to fenotypene på kardiovaskulær risiko.Det er derfor en enkel topografisk differensiering, men snarere et skille med stor fysiopatologisk betydning.

Helsefarer
Av de to typene fedme har abdominal fedme tydelig vist seg å være farligere, så mye at den regnes som en av de viktigste risikofaktorene for hjerte- og karsykdommer og dødelighet, samt en av de viktigste risikofaktorene for type II diabetes. Den overdrevne akkumuleringen av sentralt fett er også forbundet med de metabolske og kardiovaskulære komplikasjonene som er typiske for det metabolske syndromet (hypertensjon, hyperlipidemi, hepatisk steatose, aterosklerose og den nevnte type II diabetes).
Det epidemiologiske beviset på farligheten av visceralt fett har blitt bekreftet i nyere tid, takket være den økende mengden studier på vevets endokrine funksjon, eller rettere sagt av fettorganet. Det har særlig blitt sett at magefett har andre egenskaper enn den subkutane, både under den cellulære profilen og under aspektet av effektene som disse cellene har på den endokrine-metabolske balansen i organismen. Faktisk har det blitt vist at de hvite adipocytter av visceralt fett er spesielt aktive i frigjøring av adipokiner, stoffer med lokale (parakrin), sentrale og perifere (endokrine) effekter. Gjennom direkte eller indirekte frigjøring av disse stoffene, visceralt fett styrer "appetitt og energibalanse, immunitet, angiogenese, insulinfølsomhet og lipidmetabolisme."
En av de mest kjente adipokinene, adiponectin, forbedrer insulinfølsomheten og har antiinflammatorisk aktivitet; dens nivåer, i motsetning til mange andre adipokines, er lavere hos de fete enn i normalvekten. På den annen side øker overskuddet av visceralt fett frigjøring av stoffer som interleukin 6 (IL-6), resistin og TNF-α (cytokiner med pro-inflammatorisk aktivitet), PAI-1 (pro-trombotisk effekt) og ASP (stimulerende aktivitet ved syntese av triglyserider og hemmende for oksidasjon av fettsyrer).
Den overdrevne volumetriske økningen av adipocyttene, forårsaket av den iøynefallende akkumuleringen av triglyserider, bestemmer deres død og den påfølgende lyse av makrofager, som angriper lipidvakuolene med en ytterligere økning i organismenes inflammatoriske tilstand (nivåene av protein C også stigning. reaktiv, for tiden ansett som en viktig kardiovaskulær risikofaktor).
Antall makrofager tilstede i fettvevet er proporsjonalt med graden av fedme, eller rettere sagt til hypertrofi av adipocyttene som vanligvis er forbundet med fedme. Dermed er det en slags fremmedlegeme -reaksjon, med påfølgende kronisk betennelse som, hvis den videreføres over tid, disponerer for viktige metabolske sykdommer.
Reduksjon i syntese og frigjøring av nitrogenoksid, en gass med en kraftig vasodilatorisk virkning, bidrar til ytterligere å øke den aterosklerotiske risikoen.Denne gassen fremmer lipolyse og er en stimulans for spredning av brune fettceller, som, i motsetning til de hvite, ikke akkumulerer lipider, men brenner dem, enten for å opprettholde kroppstemperaturen i kalde miljøer, eller for å kvitte seg med matoverskudd som kan endre seg den "metabolske balansen. Syntesen av nitrogenoksid, også aktiv i angiogenese og i lokal mitokondrionese (som sannsynligvis ville forhindre den nevnte død av adipocytter på grunn av hypoksi fra overdreven lipidakkumulering), hemmes av TNF-α, et adipokin som frigjøres stort mengder fra det hypertrofiske viscerale hvite fettvevet og makrofager som angriper det.
Den spesielle anatomiske plasseringen av det viscerale fettet sikrer at adipokinene og andre stoffer som frigjøres flyter direkte inn i portalvenesystemet, som transporterer dem til leveren. Den fremtredende metabolske rollen som denne kjertelen spiller, hjelper til med å forklare den store innflytelsen av visceralt fett på helsen til hele organismen.
Et typisk trekk ved visceralt fett er større følsomhet for lipolytiske stimuli, siden virkningen av omental lipoproteinlipase er 50% større enn subkutant fett. Dette betyr at i tilfelle vekttap er det første fettet som skal "brennes" bare den viscerale.
Overskuddet av magefett er direkte relatert til livets omkrets. Spesielt blir kardiovaskulær risiko klinisk relevant når terskelverdiene på 102 cm omkrets på navlestrengen hos menn og 88 cm hos kvinner er nådd.
For å prøve å forklare sammenhengen mellom overflødig omalt fett og type II diabetes, har det vist seg at den høye strømmen av fettsyrer, som kommer fra viscerale adipocytter og går til leveren, øker produksjonen av VLDL (som, som vi vet, kan bli senere omdannet til det farlige LDL - dårlig kolesterol, som disponerer for atheromatøs prosess.) Det fremmer også glukoneogenese og reduserer hepatisk clearance av insulin, med en påfølgende økning i nivået av dette hormonet i sirkulasjonen. I tillegg til fettsyrer fra viscerale fettavsetninger, må vi også og i alle fall ta hensyn til virkningen av adipokinene selv. Interleukin-6, for eksempel, i leveren stimulerer glukoneogenese og triglyseridsekresjon, med kompenserende hyperinsulinemi.
Den høye tilstedeværelsen av frie fettsyrer i sirkulasjonen får disse næringsstoffene til å "konkurrere" med glukose for å komme inn i celler, spesielt i muskelceller. Som et resultat oppstår en økning i blodsukkeret, som respons på bukspyttkjertelen som øker frigjøringen av insulin. Det doble hepatopankrea-bidraget til hyperinsulinemi betyr at til tross for de høye glykemiske verdiene, er store mengder insulin tilstede i sirkulasjonen; i disse tilfellene snakker vi om insulinresistens, det er en tilstand preget av redusert biologisk respons fra vevet til "insulinvirkning. Ikke overraskende er kirurgisk fjerning av visceralt fettvev hos moderat overvektige rotter i stand til å normalisere insulinresistens.
Insulinresistens og hyperinsulinemi er ansvarlige for alle disse endringene i glukosemetabolismen, alt fra nedsatt fastende glykemi til nedsatt glukosetoleranse og åpen diabetes. Disse endringene, sammen med de som er like negative på lipidmetabolismen, står for den større kardiovaskulære risikoen for individet med visceral fedme sammenlignet med normalvekten.